Hand- en polsklachten
Niet-traumatische klachten
Naar Volledige tekst ›Diagnostiek algemeen
Naar Volledige tekst ›Verricht een gestructureerde anamnese en lichamelijk onderzoek, passend bij de gepresenteerde symptomen.
Evaluatie van niet-traumatische klachten
Naar Volledige tekst ›Zie tabel 1 voor de meest voorkomende niet-traumatische aandoeningen.
| Lokalisatie | Aandoening | Belangrijkste symptomen |
|---|---|---|
| Pols en/of vingers | Carpaletunnelsyndroom | (Nachtelijke) paresthesieën in voornamelijk dig. I-III en de radiale zijde van dig. IV en de aansluitende handpalmregio. Wapperen met de hand kan verlichting geven (zie ook Diagnostiek bij carpaletunnelsyndroom) |
| Ganglion | Gladde ronde, meestal pijnloze en vast-elastische zwelling, gefixeerd aan de onderlaag, vaak aan de dorsale zijde van de pols of bij de DIP-gewrichten. Er kan drukpijn zijn ter plaatse, of ter hoogte van de overgang van het scafoïd en het lunatum (zie ook Diagnostiek bij ganglion) | |
| Vingers | Artrose van de PIP- en DIP-gewrichten | Pijn, zwelling, stijfheid en/of bewegingsbeperking van PIP- en DIP-gewrichten (zie ook Diagnostiek bij handartrose) |
| Triggervinger of triggerduim | ‘Hokken’ bij strekken van de vinger of duim vanuit diepe flexie, pijn bij buigen en/of drukpijn en zwelling palmair ter plaatse van het MCP-gewricht en de A1-pulley (zie ook Diagnostiek bij triggervinger) | |
| Handpalm | Contractuur van Dupuytren | Vast-elastische, soms pijnlijke verdikkingen en/of strengen in de handpalm met geleidelijk progressieve flexiecontractuur van de vingers (zie ook Diagnostiek bij contractuur van Dupuytren) |
| Radiale zijde pols | Tendovaginitis van De Quervain | Lokale (druk)pijn en/of zwelling aan radiale zijde van de pols, met name over de m. abductor pollicis longus en m. extensor pollicis brevis (zie ook Diagnostiek bij tendovaginitis van De Quervain) |
| Radiale zijde pols/duimbasis | Artrose van het CMC1-gewricht | Pijn, zwelling, stijfheid en/of bewegingsbeperking van het carpometacarpale gewricht (zie ook Diagnostiek bij handartrose) |
| Midcarpaal/pols | Ligamentaire hyperlaxiteit, carpale instabiliteit, scafolunaire disfunctie, posttraumatisch letsel | Pijnklachten midcarpaal en rond de pols, eventueel met giving way en klikken; mogelijk trauma in het verleden (val op de uitgestrekte hand) (zie ook Meer aspecifieke midcarpale hand- en polsklachten) |
Carpaletunnelsyndroom
Naar Volledige tekst ›Diagnostiek bij carpaletunnelsyndroom
Naar Volledige tekst ›- Bij ‘klassiek CTS’ is aanvullend onderzoek niet noodzakelijk(zie Evaluatie CTS).
- Bij ‘mogelijk CTS’ en behandelwens: consultatie en/of diagnostiek (EMG of een zenuwecho) afhankelijk van de lokale afspraken
Beleid bij carpaletunnelsyndroom
Naar Volledige tekst ›- De behandelopties verschillen duidelijk in invasiviteit en voor- en nadelen
- Bespreek de voor- en nadelen en maak samen een keuze op basis van de waarden en voorkeuren van de patiënt
- De prognose en de behandelopties zijn hetzelfde voor zwangeren
- Bij milde tot matige of kort bestaande pijn en/of beperkingen:
- Overweeg kortdurend (4-6 weken) afwachtend beleid met voorlichting en adviezen
- Adviseer zo nodig pijnmedicatie conform het beleid bij acute nociceptieve pijn in de NHG-Standaard Pijn (paracetamol en/of een (dermaal) NSAID).
- Bij matige tot ernstige pijn en/of beperkingen:
- Adviseer zo nodig pijnmedicatie conform het beleid bij acute nociceptieve pijn in de NHG-Standaard Pijn (paracetamol en/of een (dermaal) NSAID).
- Overweeg spalkbehandeling of een corticosteroïdinjectie in de carpale tunnel. Dit zijn gelijkwaardige behandelopties. Eerste keus bij injectie is 10 mg triamcinolonacetonide 10 mg/ml (zie Tabel 3).
- Bespreek als alternatief verwijzing voor eventuele chirurgische decompressie, met name bij atrofie of spierzwakte van de duimmuis en wens tot operatieve behandeling
Ganglion
Naar Volledige tekst ›Diagnostiek bij ganglion
Naar Volledige tekst ›Gebruik bij twijfel over de diagnose diafanoscopie en vraag zo nodig een echografie aan
Beleid bij ganglion
Naar Volledige tekst ›- Wacht af als er geen of weinig klachten zijn
- Verricht geen aspiratie als behandeling, omdat het beloop hierbij niet anders is dan een afwachtend beleid
- Overweeg (verwijzing voor) excisie bij ernstige klachten en een (duidelijke) behandelwens; na excisie is de recidiefkans kleiner dan bij afwachtend beleid
Handartrose
Naar Volledige tekst ›Diagnostiek bij handartrose
Naar Volledige tekst ›We bevelen röntgenonderzoek voor de stadiering van artrose niet aan vanwege de discrepantie tussen radiologische kenmerken van artrose van de hand of pols en de klinische symptomen
Beleid bij handartrose
Naar Volledige tekst ›- Behandel zo lang mogelijk conservatief, bij voorkeur met een combinatie van behandelingen (pijnstilling volgens NHG-Standaard Pijn, handtherapie met oefentherapie en eventueel spalkbehandeling)
- Wees terughoudend met een corticosteroïdinjectie bij CMC1-artrose
Triggervinger
Naar Volledige tekst ›Beleid bij triggervinger
Naar Volledige tekst ›- Overweeg een corticosteroïdinjectie in de peesschede bij een symptomatische triggervinger en behandelwens; eerste keus bij injectie is 5 mg triamcinolonacetonide 10 mg/ml (zie Tabel 3).
- Overweeg verwijzing voor een eventuele operatie:
- bij duidelijke functionele beperkingen
- als een corticosteroïdinjectie niet gewenst is of onvoldoende effectief is
- bij een gefixeerde triggervinger met wens tot correctie
Contractuur van Dupuytren
Naar Volledige tekst ›Beleid bij contractuur van Dupuytren
Naar Volledige tekst ›- Orale medicatie, spalkbehandeling, fysiotherapie of (corticosteroïd)injecties worden niet aanbevolen vanwege gebrek aan bewijs
- Overweeg verwijzing voor een eventuele operatieve correctie bij een patiënt met een behandelwens en:
- functionele belemmering van de hand, of
- snelle progressie van de flexiecontractuur van een vinger, of
- pijn
- Verwijs PIP-contracturen tijdig, omdat deze sneller irreversibel worden door contractuur van het kapsel
Tendovaginitis van De Quervain
Naar Volledige tekst ›Beleid bij tendovaginitis van De Quervain
Naar Volledige tekst ›- Wacht tot 6 weken af bij kort bestaande klachten
- Geef Voorlichting en advies.
- Schrijf zo nodig pijnstilling voor volgens de NHG-Standaard Pijn (paracetamol en/of NSAID)
- Overweeg spalkbehandeling en/of een corticosteroïdinjectie in de peesschede. Eerste keus bij injectie is 10 mg triamcinolonacetonide 10 mg/ml (zie Tabel 3) Een combinatie van spalk en corticosteroïdinjectie heeft de voorkeur
Traumatische klachten
Naar Volledige tekst ›Diagnostiek bij traumatische klachten
Naar Volledige tekst ›- Ga na of er sprake kan zijn van pathologie die directe behandeling en/of verwijzing behoeft (zie tabel 2)
- Gebruik hierbij zo nodig de Handletselkaart
- Laat bij verdenking op ossaal letsel röntgenfoto’s maken
- Vraag geen aanvullend onderzoek aan bij (vermoeden van) pees- of zenuwletsel
Beleid bij traumatische klachten
Naar Volledige tekst ›- Overweeg consultatie of verwijzing indien er een verdenking is op pees- of zenuwletsel, of als dit niet goed te beoordelen is
- Schrijf zo nodig pijnstilling voor volgens de NHG-Standaard Pijn (paracetamol en/of NSAID)
| Lokalisatie | Aandoening | Belangrijkste symptomen |
|---|---|---|
| Acute klachten | ||
| Tabatière anatomique (anatomische snuifdoos) | Scafoïdfractuur |
|
| MCP1 | Skiduim (letsel aan de ulnaire collaterale band) |
|
| Vingers | Malletvinger (letsel aan de extensorpees van de distale falanx) |
|
| Vingers | Jersey finger (letsel aan de flexorpees van de distale falanx) |
|
|
Persisterende posttraumatische klachten (zie Meer aspecifieke midcarpale hand- en polsklachten) |
||
| Pols | Carpale instabiliteit (SL-letsel) |
|
| Tabatière anatomique (anatomische snuifdoos) | (Oude) scafoïdfractuur |
|
Malletvinger
Naar Volledige tekst ›Diagnostiek bij malletvinger
Naar Volledige tekst ›- Vraag (uitgesteld) röntgenonderzoek aan om onderscheid te maken tussen een conservatief behandelbare malletvinger en een mogelijke operatie indicatie
- Conservatief behandelbare malletvinger:
- tendinogene malletvinger (ruptuur van de pees)
- ossale malletvinger met avulsiefractuur <30% van het gewrichtsoppervlak van het DIP-gewricht
- Mogelijke operatie indicatie: ossale malletvinger met avulsiefragment >30% van het gewrichtsoppervlak van het DIP-gewricht
Beleid bij malletvinger
Naar Volledige tekst ›- Volg bij een tendinogene malletvinger of malletvinger met avulsiefractuur < 30% het Behandelschema
- Draag zorg voor een adequate, goed sluitende spalk (zie Praktische aanwijzingen)
- Geef goede instructies om inadequate behandeling en huidproblemen te voorkomen (zie Praktische aanwijzingen)
Belangrijkste wijzigingen
Naar Samenvatting ›- Gezamenlijke besluitvorming speelt een grote rol bij de behandeling van een patiënt met carpaletunnelsyndroom, de behandelopties zijn in essentie ongewijzigd.
- De behandeling van carpaletunnelsyndroom bij zwangeren is niet anders dan bij niet-zwangeren.
- Bij een ganglion wordt aspiratie pro diagnosi ontraden, omdat het beloop na deze behandeling niet anders is dan bij afwachtend beleid. Gebruik diafanie bij diafanoscopie bij twijfel over de diagnose en vraag zo nodig echografie aan.
- Als verwijsindicaties bij een contractuur van Dupuytren zijn toegevoegd: functionele beperkingen, pijn en snelle progressie van de flexiecontractuur van een vinger.
- Het behandelschema van een malletvinger (hamervinger) is aangepast.
- Handvatten voor de diagnostiek van acute trauma’s van hand en pols zijn toegevoegd.
Kernboodschappen
Naar Samenvatting ›- Voor diagnostiek bij hand- en polsaandoeningen in de eerste lijn zijn in de regel anamnese en gericht lichamelijk onderzoek voldoende. Overweeg alleen aanvullend onderzoek als dit consequenties heeft voor het beleid. Overweeg verwijzing of consultatie bij twijfel over de diagnose.
- Gezamenlijke besluitvorming speelt een grote rol bij de behandeling van carpaletunnelsyndroom. Kies eerst voor een periode van afwachten bij klachten die mild tot matig zijn of slechts enkele weken bestaan. Overweeg bij matige tot ernstige klachten spalkbehandeling, corticosteroïdinjectie(s) of verwijzing voor eventuele chirurgische decompressie.
- Behandel handartrose zo lang mogelijk conservatief, kies bij voorkeur voor een combinatie van behandelingen. Wees terughoudend met het aanbieden van een corticosteroïdinjectie bij patiënten met CMC1-artrose.
- Overweeg een corticosteroïdinjectie bij patiënten met een symptomatische triggervinger en behandelwens.
- Er is geen bewijs voor de effectiviteit van spalken of injecties bij een contractuur van Dupuytren. Overweeg verwijzing voor operatie bij patiënten met een behandelwens en functionele belemmering van de hand, pijn of snelle progressie van de flexiecontractuur van een vinger.
- Overweeg spalkbehandeling en een corticosteroïdinjectie bij patiënten met een tendovaginitis van De Quervain die niet verbeteren bij afwachtend beleid of die > circa 6 weken klachten hebben. Overweeg een combinatiebehandeling.
- Verricht röntgendiagnostiek bij een malletvinger om te differentiëren tussen een tendinogene of ossale malletvinger, en om een eventuele operatie-indicatie (ossale malletvinger met avulsiefragment > 30% van het gewrichtsoppervlak) uit te sluiten.
Inleiding
Naar Samenvatting ›Scope
Naar Samenvatting ›- Algemene diagnostiek van hand- en polsklachten bij volwassenen in de huisartsenpraktijk.
- Diagnostiek en behandeling van de volgende veelvoorkomende niet-traumatische hand- en polsklachten die de huisarts zelf (initieel) kan behandelen:
- carpaletunnelsyndroom (CTS)
- ganglion
- artrose van de hand
- triggervinger en triggerduim
- contractuur van Dupuytren
- tendovaginitis van De Quervain
- Acute beoordeling, algemene diagnostiek en verwijscriteria bij veelvoorkomende traumatische aandoeningen van hand en pols, met aandacht voor aandoeningen die minder vaak voorkomen maar een hoog risico hebben op langdurige klachten en/of beperkingen.
- Conservatieve behandeling van malletvinger.
Keuze van de elementen
Om de praktische bruikbaarheid te verbeteren besteedt de huidige versie van de standaard aandacht aan de volgende punten:
- algemene diagnostiek vanuit de ingangsklacht van de patiënt
- aandachtspunten bij de beoordeling van acuut traumatische aandoeningen en de verwijzingscriteria, omdat het van groot belang is dat de primaire zorgverlener de ernst van het handletsel kan onderkennen en weet wanneer doorverwijzing noodzakelijk is
De beschreven aandoeningen zijn dezelfde gebleven. Bij de selectie is een afweging gemaakt op basis van de incidentie in de huisartsenpraktijk en de aanwezigheid van behandelopties in de eerste lijn.
Terminologie
In deze standaard is gekozen voor een terminologie die past bij de huisartsenpraktijk en analoog is aan die van andere nationale en internationale richtlijnen en consensusafspraken: de richtlijn Ziekte van Dupuytren, de richtlijn Handelen van de bedrijfsarts bij werknemers met klachten aan arm, nek of schouder (KANS), de richtlijn Primaire artrose duimbasis, de Richtlijn Carpaletunnelsyndroom, de Richtlijn Handfracturen, de International Classification of Functioning, Disability and Health en de Guideline Osteoarthritis.
Adequate zorgverlening bij hand- en polsklachten
Zowel in de eerste als in de tweede lijn blijken hand- en polsklachten moeilijk te herkennen en te diagnosticeren door de relatieve zeldzaamheid, de complexiteit van de anatomie en het scala aan klachten en aandoeningen. De potentiële gevolgen van suboptimale diagnostiek en behandeling zijn voor de patiënt echter groot. Het is van belang dat de huisarts zich bewust is van de eigen bekwaamheid om een juiste inschatting te kunnen maken van de diagnostiek en behandeling. Laagdrempelige consultatie van een collega (kader)arts of verwijzing zijn goede alternatieven.
Er is in de praktijk onduidelijkheid over naar wie het beste verwezen kan worden, dit is in de standaard geadresseerd. Daarnaast was er behoefte aan praktische adviezen omtrent het adequaat voorschrijven van braces. Hiervoor zijn nu online de Praktische aanwijzingen orthesen bij hand- en polsklachten beschikbaar.
Buiten de scope
Naar Samenvatting ›- Aanvullend onderzoek en verder beleid bij minder vaak voorkomende acute trauma’s van de hand en pols (zie de multidisciplinaire Richtlijn Handfracturen).
- Aanvullend onderzoek en verder beleid bij posttraumatisch letsel van hand en pols.
- Aandoeningen die zich niet beperken tot de hand- en polsregio, zoals:
- complex regionaal pijnsyndroom (CRPS), voorheen bekend als südeckdystrofie of sympathische reflexdystrofie (zie de multidisciplinaire richtlijn Complex Regionaal Pijn Syndroom type 1)
- ziekte van Raynaud (zie NHG-Behandelrichtlijn Fenomeen van Raynaud)
- huidaandoeningen (zoals huidinfecties, eczeem, epitheelcyste)
- bottumoren
- reumatoïde artritis (zie NHG-Standaard Artritis)
- Hand- en polsklachten die hun oorsprong elders in het lichaam hebben (zoals uitstralende klachten bij een cervicale hernia).
Achtergronden
Naar Samenvatting ›Algemeen
Naar Samenvatting ›Begrippen
Naar Samenvatting ›Carpaletunnelsyndroom
Naar Samenvatting ›Het carpaletunnelsyndroom (CTS) bestaat uit een verzameling klachten veroorzaakt door compressie van de n. medianus in het verloop van de carpale tunnel. Uiteindelijk kan compressie van de n. medianus leiden tot thenaratrofie en spierzwakte. Er is geen gouden standaard voor de diagnose, maar men spreekt wel van ‘klassiek CTS’ bij volwassenen met tintelingen in het verdelingsgebied van de n. medianus, waar de patiënt ’s nachts wakker van wordt en die verbeteren of verergeren bij bepaalde houdingen of bewegingen.
Ganglion
Naar Samenvatting ›Een ganglion is een uitstulping van een gewrichtskapsel of peesschede, gevuld met synoviale vloeistof. Een ganglion kan groeien, maar ook resorberen en eventueel later opnieuw opkomen. Meestal geeft een ganglion geen klachten, soms zijn er pijnklachten bij bepaalde bewegingen, functionele beperkingen of cosmetische bezwaren.
Artrose van de hand
Naar Samenvatting ›Artrose is een klinisch syndroom gekenmerkt door activiteitgerelateerde gewrichtspijn, stijfheid en functiebeperking. Pijnklachten bij artrose treden vaak op in exacerbaties (flares). Artrose in de hand komt meestal voor aan de duimbasis in het carpometacarpale gewricht (CMC1) of het scafotrapeziotrapezoïdale gewricht (STT), en in de proximale (PIP) of distale (DIP) vingergewrichten. Kenmerkend is de vorming van benige verdikkingen bij de PIP-gewrichten (noduli van Bouchard) of bij de DIP-gewrichten (noduli van Heberden). Artrose in de pols of de handwortelbeentjes komt minder vaak voor (soms in het radiocarpale gewricht of in het distale radio-ulnaire gewricht).
Triggervinger
Naar Samenvatting ›Een triggervinger of triggerduim (andere benamingen zijn springvinger, springduim, hokkende vinger of hokkende duim) is een tendovaginitis van de flexorpezen van de vingers of de duim. Het normale en soepele glijden van de flexorpees tijdens buigen en strekken van de vinger wordt belemmerd ter hoogte van de A1-pulley, wat kan leiden tot pijn bij buigen, ‘hokken’ van de vinger bij strekken, of beperkingen bij buigen en strekken van de vinger.
Contractuur van Dupuytren
Naar Samenvatting ›Een contractuur van Dupuytren is een fibromatose van de aponeurosis palmaris. Kenmerkend is het ontstaan van zeer vaste en soms pijnlijke knobbels (noduli) en bindweefselstrengen in de handpalm en vingers, vooral in de straal van de pink en ringvinger. Op langere termijn kan dit leiden tot een permanente flexiecontractuur.
Tendovaginitis van De Quervain
Naar Samenvatting ›Tendovaginitis van De Quervain is een irritatie van de pezen van de m. abductor pollicis longus en/of de m. extensor pollicis brevis. Kenmerkend zijn pijn aan de radiale zijde van de pols (vooral bij grijpbewegingen en bij ulnaire deviatie van de pols), functiebeperking van de duim en soms zwelling aan de dorsoradiale zijde van de pols.
Malletvinger
Naar Samenvatting ›De malletvinger (hamervinger) ontstaat door letsel van de pees of peesaanhechting van de vingerextensor ter hoogte van de eindfalanx. Men onderscheidt de tendinogene malletvinger (ruptuur van de pees) en de ossale malletvinger (avulsiefractuur van de distale falanx). Kenmerkend is de flexiestand van de vinger in het DIP-gewricht en de onmogelijkheid van actieve extensie.
Epidemiologie
Naar Samenvatting ›- In de algemene Nederlandse bevolking bedraagt de prevalentie van hand- en polsklachten ongeveer 125 per 1000 personen; deze stijgt met de leeftijd.
- In de Nederlandse huisartsenpraktijk is de prevalentie van hand- en vingerklachten 20,6 per 1000 patiënten en van polsklachten ongeveer 8,8 per 1000 patiënten.
- De incidentie hand- en vingerklachten in de Nederlandse huisartsenpraktijk is ongeveer 24,1 nieuwe episoden per 1000 patiënten per jaar; die van polsklachten is ongeveer 10,3 episoden per 1000 patiënten per jaar.
- Hand- en polsklachten komen in de huisartsenpraktijk vaker voor bij vrouwen dan bij mannen.
Algemene bevolking
In een onderzoek onder de Nederlandse bevolking > 25 jaar (n = 3664) wordt de puntprevalentie van hand- en polsklachten geschat op 125 per 1000 personen (86 voor mannen en 163 voor vrouwen). De puntprevalentie neemt toe met de leeftijd: van 95 per 1000 personen in de leeftijd 25-44 jaar tot 161 per 1000 personen in de leeftijd ≥ 65 jaar.
Huisartsenpraktijk
- Uit de gegevens van het Nivel over 2018 blijkt de incidentie van hand- en vingerklachten (ICPC-code L12) ongeveer 24,1 nieuwe episoden per 1000 patiënten per jaar en van polsklachten (ICPC-code L11) ongeveer 10,3 episoden per 1000 patiënten per jaar.
- De prevalentie van hand- en vingerklachten is 20,6 per 1000 patiënten, die van polsklachten ongeveer 8,8 per 1000 patiënten.
- De incidentie en prevalentie van zowel hand- als polsklachten in de huisartsenpraktijk zijn hoger voor vrouwen dan voor mannen (de incidentie van polsklachten is 12,3 respectievelijk 8,4 per 1000 patiënten; de incidentie van hand- en vingerklachten is 27,8 respectievelijk 20,5 per 1000 patiënten).
- De huidige incidentie- en prevalentiecijfers zijn beduidend hoger dan in de vorige versie van deze standaard. Dit komt waarschijnlijk grotendeels door de verschillen in registratie en rapportage tussen 2001 en 2018. In 2001 werden gegevens gebruikt uit een onderzoek bij 198 huisartsen die gebruik maakten van digitale registratie. In 2018 zijn de cijfers gebaseerd op gegevens van ongeveer 419 huisartsenpraktijken met in totaal ongeveer 1,7 miljoen ingeschreven patiënten. Daarnaast is de digitale registratie verbeterd en algemeen geïntroduceerd (zie Cijfers zorgverlening huisartsen - Nivel Zorgregistraties Eerste Lijn).
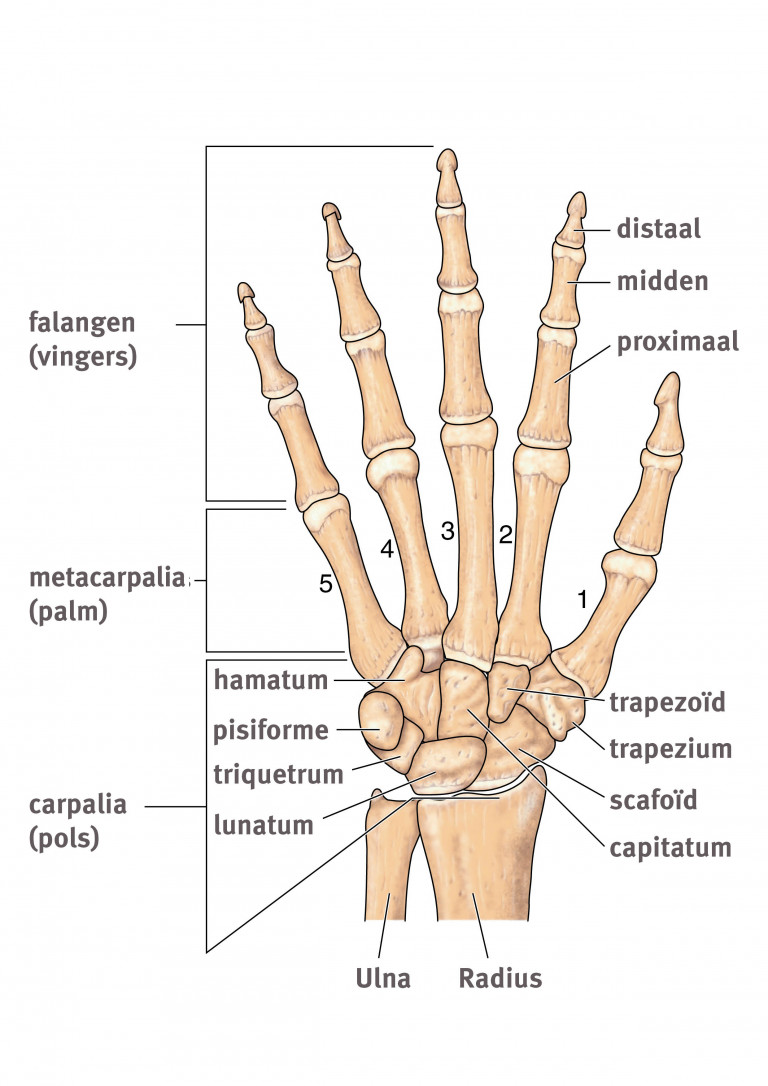
Relevante anatomie
Naar Samenvatting ›De anatomie van de hand en pols is complex.
Het onderstaande overzicht behandelt alleen de structuren die relevant zijn voor aandoeningen binnen de scope van deze standaard.
Gewrichten en ossale verbindingen
- De carpalia zijn te verdelen in een proximale en een distale rij en worden door intrinsieke ligamenten verbonden.
- In het radio-ulnaire gewricht roteert de radius om de ulna.
- De volaire plaat en de collaterale ligamenten stabiliseren de MCP-en IP-gewrichten.
- Het triangulaire fibrocartilagineuze complex (TFCC) bestaat uit een kraakbeenschijf in het ulnocarpale gewricht, een ligament tussen het ulnakopje en de radius, en een ligament tussen het ulnakopje en de carpalia. Het TFCC heeft een belangrijke functie voor de stabiliteit van de pols en krachtenoverdracht.
- Het scafolunaire ligament (SL) tussen het os scaphoideum en het os lunatum is belangrijk voor de carpale stabiliteit.
- Het ulnaire collaterale ligament (UCL) van de duim beschermt het MCP1-gewricht tegen valgusstress (hyperabductie). Bij een ruptuur wordt de duim instabiel.
- Het flexorretinaculum vormt de bovenzijde van de carpale tunnel. Deze bevat naast de n. medianus nog de pezen van de m. flexor digitorum profundus, de m. flexor digitorum superficialis en de m. flexor pollicis longus.
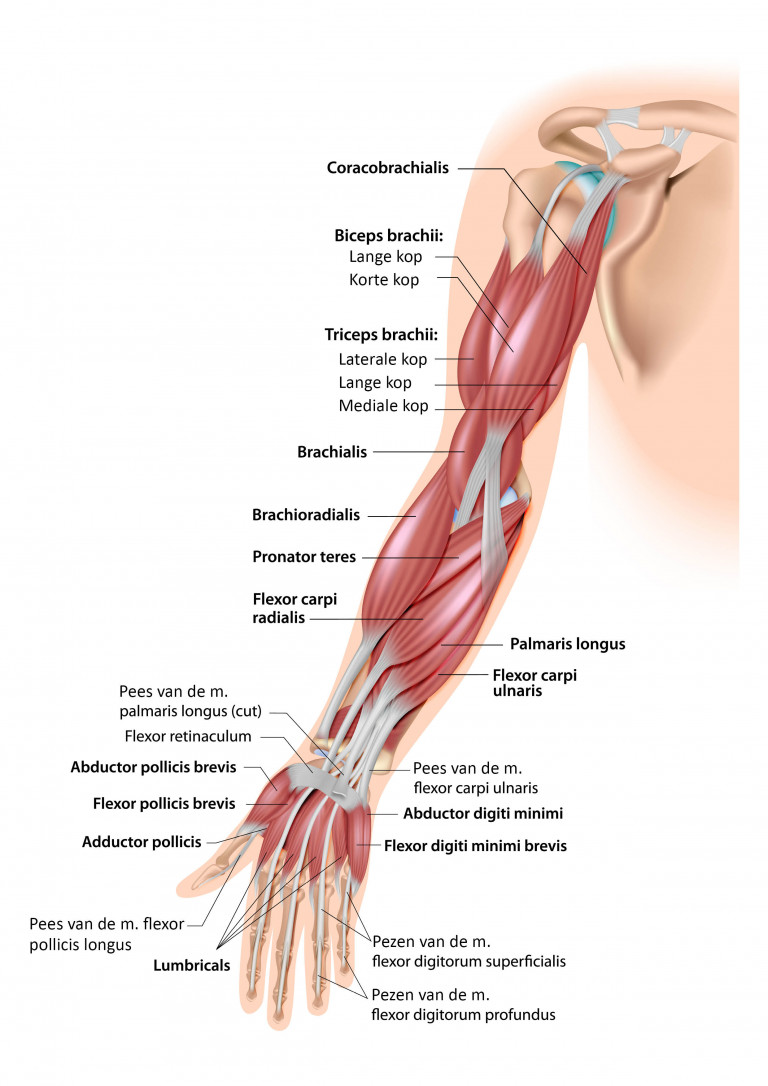
Musculatuur
Buigpezen
- Aan de volaire zijde van de pols: m. flexor carpi radialis en ulnaris, m. palmaris longus (indien aanwezig).
- Aan elke vinger: m. flexor digitorum superficialis, met aanhechting aan de middenfalanx (flexie PIP), en m. flexor digitorum profundus aan de distale falanx (flexie DIP). De peesschedes van deze pezen worden verstevigd door diverse verdikkingen, die van proximaal naar distaal genummerd zijn (A1- tot en met A4-pulley).
- Aan de duim: m. flexor pollicis longus voor de flexie van het IP-gewricht.
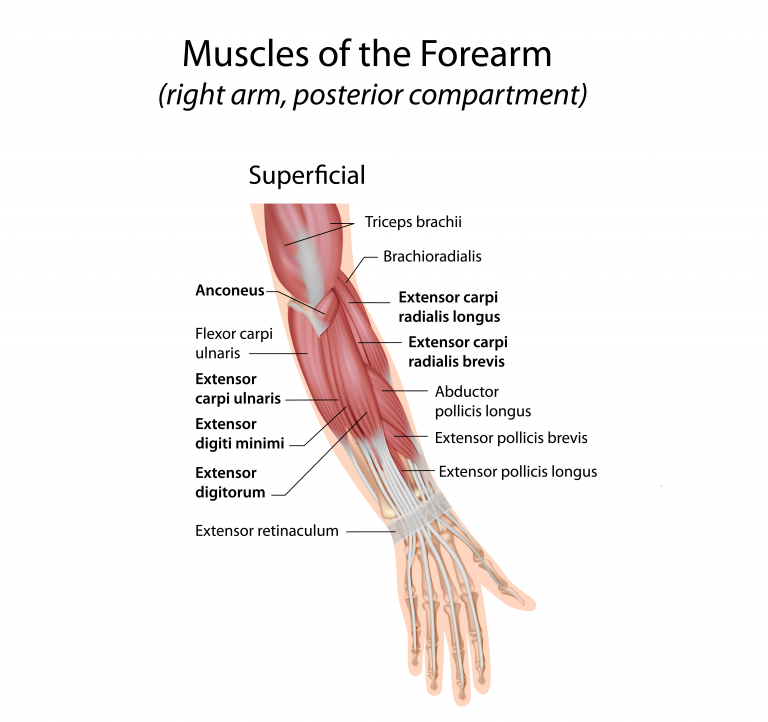
Strekpezen
- Aan de dorsale zijde van de pols lopen de strekpezen in 6 compartimenten onder het extensorretinaculum door.
- Voor de vingers: mm. extensor digitorum communis. Bij de wijsvinger en de pink is nog een additionele extensor aanwezig. De pezen splitsen zich in een centrale slip met een aanhechting aan de middenfalanx (extensie PIP) en 2 laterale slippen die aanhechten aan de basis van de distale falanx (extensie DIP).
- Voor de duim: m. extensor pollicis longus (extensie IP-gewricht) en de m. abductor pollicis longus en brevis (abductie respectievelijk extensie van het MC1-gewricht). Deze extensoren vormen samen de grenzen van de anatomische snuifdoos (tabatière anatomique).
Zenuwen
N. medianus
- Verloopt distaal van de pols door de carpale tunnel onder het transversale carpale ligament.
- Innerveert de buigpezen van de pols en de meerderheid van de oppervlakkige buigpezen van de vingers, deels als aftakking via de n. Interosseus anterior.
- De motorische tak splitst zich na de carpale tunnel af naar de duimmuis.
- De sensibele tak loopt naar de duim, wijs- en middelvinger, en naar de radiale helft van de ringvinger.
N. radialis
- Verloopt radiaal van de a. radialis.
- Innerveert de strekpezen van de pols, vingers en duim, deels als aftakking via de n. interosseus posterior.
- De sensibele tak verzorgt het dorsum en de radiale zijde van hand.
N. ulnaris
- Loopt radiaal langs de m. flexor carpi ulnaris door het kanaal van Guyon bij de pols.
- Innerveert de m. flexor carpi ulnaris, de diepe buigpezen van dig. IV en V, de spieren van de pinkmuis, de m. adductor pollicis en de helft van de m. flexor pollicis brevis.
- De sensibele takken verzorgen de pink en de ulnaire zijde van de ringvinger, en het ulnaire deel van de dorsale zijde van de hand.
Overige
Daarnaast heeft iedere vinger 2 digitale zenuwen die afhankelijk van het verzorgingsgebied afkomstig zijn van de n. medianus of de n. ulnaris.
Carpaletunnelsyndroom
Naar Samenvatting ›Epidemiologie
Naar Samenvatting ›- De prevalentie van CTS in de algemene Nederlandse bevolking is 6,8%.
- De prevalentie in de huisartsenpraktijk is voor vrouwen ongeveer 9 en voor mannen ongeveer 4 per 1000 patiënten per jaar.
- De incidentie in de huisartsenpraktijk is voor vrouwen ongeveer 5 en voor mannen ongeveer 2 nieuwe episoden per 1000 patiënten per jaar. In een normpraktijk (2095 patiënten) stelt de huisarts per jaar 7 keer de diagnose ‘CTS’.
- CTS is een aandoening die vaker voorkomt bij vrouwen dan bij mannen, en vooral in de leeftijd 45-64 jaar.
- 1/3 van de zwangere vrouwen krijgt klachten passend bij CTS, met name in het tweede en derde trimester; bij 70% van hen zijn de klachten bilateraal.
Algemene bevolking
De gerapporteerde epidemiologische cijfers voor het CTS lopen uiteen door het gebruik van verschillende definities, bijvoorbeeld op basis van klinische symptomen, elektrofysiologisch bevestigde CTS of ernst van de symptomen. In een meta-analyse van 87 onderzoeken (27 longitudinale en 60 cross-sectionele) werd een prevalentie in de algemene bevolking berekend van 6,8% (95%-BI 2,2 tot 18,7).
Huisartsenpraktijk
De incidentiecijfers voor de diagnose ‘CTS’ (ICPC-code N93) uit 2018 in de Nederlandse huisartsenpraktijk zijn beschikbaar via Nivel Zorgregistraties Eerste Lijn. De incidentie was voor mannen 2,4 en voor vrouwen 5,2 per 1000 episoden, de prevalentie was 4,2 voor mannen en 9,2 voor vrouwen. CTS komt in alle leeftijdscategorieën vaker voor bij vrouwen dan bij mannen, bij mannen valt de hoogste prevalentie in de middelbare leeftijd.
Zwangeren
De prevalentie van CTS bij zwangere vrouwen varieert afhankelijk van het onderzoeksdesign, de diagnostische criteria, de beoordeling van de criteria en de fase van de zwangerschap. In een onderzoek onder 639 zwangere vrouwen in Nederlandse verloskundepraktijken gaven 219 vrouwen (34%) klinische klachten aan passend bij CTS (pijn, tintelingen, doofheid in handen of polsen). De klachten ontstonden bij 86 zwangeren (39%) bij 21-30 weken zwangerschap en bij 97 vrouwen (40%) bij > 30 weken. De ernst nam toe in het verloop van de zwangerschap, maar waren doorgaans mild tot matig. Bij 70% van de patiënten waren de klachten bilateraal.
Etiologie en pathofysiologie
Naar Samenvatting ›De carpale tunnel is een nauwe doorgang aan de palmaire zijde van de pols. De tunnel wordt aan de dorsale zijde begrensd door de carpalia en aan de palmaire zijde door het ligamentum carpi transversum. In de tunnel lopen de n. medianus en de flexorpezen van duim en vingers. CTS wordt veroorzaakt door drukverhoging in de carpale tunnel. Deze drukverhoging kan ischemie veroorzaken in de n. medianus, wat aanleiding geeft tot verminderde zenuwgeleiding met als gevolg paresthesieën, sensibele uitval, pijn en in een vergevorderd stadium ook motorische uitval en atrofie.
De pathofysiologie van CTS wordt gekenmerkt door symptomen die voorkomen bij compressie van de n. medianus in de carpale tunnel. Aanvankelijk treden de klachten intermitterend op en zijn er bij zenuwgeleidingsonderzoek nog geen afwijkingen te vinden. Bij voortduren of verergering van de intracarpale drukverhoging treedt segmentale demyelinisatie van de n. medianus op. Op dat moment zijn er ook afwijkingen bij het zenuwgeleidingsonderzoek, aanvankelijk in de sensibele geleiding, maar later ook in de motorische geleiding. De klachten worden dan over het algemeen erger, in die zin dat intermitterende klachten min of meer permanent kunnen worden. Ook kan bij toename van de motorische uitval zwakte van de duimspieren (m. abductor pollicis brevis en m. opponens pollicis) en atrofie van de thenar (duimmuis) optreden. De zenuwbeschadiging kan uiteindelijk irreversibel worden.
Zwangeren
De oorzaak van het frequent voorkomen van CTS bij zwangeren is niet bekend. De meest gebruikelijke hypothese is dat lokale oedeemvorming als gevolg van hormonale veranderingen zorgt voor compressie van de n. medianus in de carpale tunnel. Andere factoren die mogelijk meespelen, zijn gegeneraliseerde gewichtstoename, zwangerschapshypertensie en pre-eclampsie, veranderd glucosemetabolisme en zenuwhypersensitiviteit.
Risicofactoren
Naar Samenvatting ›Factoren die mogelijk geassocieerd zijn met het ontwikkelen van CTS:
- vrouwelijk geslacht
- hogere leeftijd
- overgewicht
- zwangerschap
- diabetes mellitus (zowel type 1 als 2)
- menopauze
- posttraumatische en congenitale vormafwijkingen van de pols
- reumatoïde artritis of handartrose (CMC1-artrose)
- Hypo- en hyperthyreoïdie
Werkgerelateerde risicofactoren die mogelijk bijdragen aan het ontstaan van CTS:
- hoogrepeterende bewegingen in combinatie met knijpen en kracht zetten
- langdurig gebruik van trillend handgereedschap
- ongunstige werkhoudingen (> 30° dorsale of palmaire flexie vanuit neutrale polsstand)
Frequent beschreven risicofactoren voor het ontstaan van CTS zijn vrouwelijk geslacht, leeftijd 40-64 jaar, overgewicht, zwangerschap, diabetes mellitus (type 1 en 2), menopauze en posttraumatische en congenitale vormafwijkingen van de carpale tunnel.
In een meta-analyse van 87 onderzoeken (27 longitudinale en 60 cross-sectionele) werden risicofactoren gepoold die mogelijk geassocieerd zijn met het optreden va CTS. De meta-analyse deed geen uitspraken over de betrouwbaarheid van de onderzoeken.
- Toenemende leeftijd (tot middelbare leeftijd)
- OR 1,9 (95%-BI 1,4 tot 1,7) in 13 cross-sectionele onderzoeken
- OR 2,2 (95%-BI 1,0 tot 5,0) in 4 longitudinale onderzoeken
- Dominante hand
- OR 1,8 (95%-BI 1,4 tot 2,3) in 2 cross-sectionele onderzoeken
- Niet-kaukasische etniciteit
- OR 2,2 (95%-BI1,2 tot 4,0) in 3 cross-sectionele onderzoeken
- Overgewicht of obesitas
- OR 1,4 (95%-BI 1,3 tot 1,6) OR 1,5 (95%-BI 1,1 tot 1,9)
- Diabetes mellitus
- OR 5,3 (95%-BI 1,6 tot 16,8)
- Psychosociale en psychiatrische problematiek
- OR 2,6 (95%-BI 1,8 tot 3,6) in 4 longitudinale onderzoeken
- Structureel alcoholgebruik (> 4 eenheden per dag)
- OR 2,3 (95%-BI 0,7 tot 2,3)
De relatie met reumatoïde artritis, handartrose en hypothyreoïdie is onzeker (de kwaliteit van het bewijs is laag) in verband met significante bias en confounders in de onderzoeken.
Werkgerelateerde risicofactoren die worden gesuggereerd, zijn langdurig en repeterend werk met flexie en extensie van de polsen, met name in combinatie met knijpen en kracht zetten, en langdurig gebruik van trillend handgereedschap. De relatie met beeldschermwerk is controversieel.
Beloop en prognose
Naar Samenvatting ›- Ongeveer 25% van de patiënten met CTS ervaart spontane verbetering over een periode van 4 weken. Bij ongeveer 50% nemen de klachten op langere termijn (2 jaar) af zonder behandeling. Bij ongeveer 25% verergeren de klachten en kan uiteindelijk structurele schade aan de n. medianus ontstaan.
- Bij zwangeren is de prognose niet anders dan bij niet-zwangeren: tot 50% herstelt binnen 1-3 jaar na de bevalling. Bij ongeveer 30% van de onbehandelde patiënten nemen de klachten mettertijd echter toe.
Er zijn enkele onderzoeken waaruit het natuurlijke beloop van CTS-klachten op te maken is. Bij een onderzoek werd een afwachtend beleid gevoerd als controlegroep van een andere interventie. Hierin liet 25% van de 40 geïncludeerde patiënten spontane verbetering zien over een periode van 4 weken. Bij een ander observationeel onderzoek van 132 patiënten leken de klachten op de langere termijn (2 jaar) af te nemen bij de helft van de patiënten. Bij de andere helft van de patiënten bleven de klachten stabiel of werden deze erger.
Percentage secundaire behandelingen
Een systematisch literatuuronderzoek uit 2016 van 16 cohortonderzoeken vermeldt 4 onderzoeken met patiënten bij wie initieel afwachtend beleid werd gevoerd (n = 12 tot 344). Na 1 jaar ontving 32-58% toch een vorm van behandeling, na 3 jaar was dit 23,4% en na 10 jaar 50% van de patiënten. De pooling van de resultaten werd bemoeilijkt door aanzienlijke kans op bias en heterogeniteit van de onderzoeken.
Zwangeren
In een observationeel multicentrisch onderzoek (n = 196) met een follow-up van 15 maanden waren de verschillende uitkomstmaten (elektrofysiologische bevindingen, symptoomscore, functiescore en pijn) verbeterd in 23-34% van de deelnemers, onveranderd in 45-62% en verergerd in 16-32%. In 2 andere onderzoeken bij onbehandelde zwangeren (n = 108) was ongeveer de helft 3 jaar na de bevalling klachtenvrij. Mogelijk houdt het geven van borstvoeding de klachten langer in stand. De prognose is mogelijk gunstiger bij kortdurende klachten en klachten op jonge leeftijd. Al langer bestaande klachten bij het eerste bezoek en een positieve test van Phalen hebben mogelijk een geringere kans op spontaan herstel.
Ganglion
Naar Samenvatting ›Epidemiologie
Naar Samenvatting ›- In de algemene Nederlandse bevolking is de prevalentie 4,5 en de incidentie 3,3 episoden per 1000 personen per jaar.
In de algemene bevolking is de prevalentie van een ganglion aan hand of pols 4,5 per 1000 patiënten per jaar; de incidentie is 3,3 episoden per 1000 patiëntjaren. Vrouwen hebben 2 × zo vaak klachten als mannen.
Er zijn geen specifieke cijfers beschikbaar voor de Nederlandse huisartsenpraktijk, omdat er geen specifieke ICPC code is voor een hand- of polsganglion. Voor ganglia in het algemeen, waarvan waarschijnlijk de grote meerderheid een hand- of polsganglion betreft, is de prevalentie in de huisartsenpraktijk 4,3 per 1000 patiëntjaren (3,2 voor mannen, 5,4 voor vrouwen). De incidentie is 4,5 per 1000 patiëntjaren (3,2 voor mannen, 5,7 voor vrouwen).
Etiologie en pathofysiologie
Naar Samenvatting ›Etiologie
Naar Samenvatting ›- De oorzaak voor het ontstaan van een ganglion is meestal onbekend.
- Een ganglion ter hoogte van het DIP-gewricht (‘mucoïdcyste’) is meestal een gevolg van een degeneratieve afwijking (artrose van het DIP-gewricht). Ulceratie van de cyste komt uitsluitend voor aan het DIP-gewricht.
- Een ganglion kan een uiting zijn van artrose, al dan niet na een fractuur.
- Een ganglion kan een uiting zijn van gewrichtsinstabiliteit (met name van het scafolunaire gewricht).
- Er lijkt geen duidelijke relatie te bestaan met werk of vrijetijdsbesteding.
Meestal is de oorzaak van een ganglion onbekend. Een belangrijke oorzakelijke factor is waarschijnlijk een pre-existente aandoening aan de handgewrichten, zoals artrose, acuut trauma of instabiliteit door bijvoorbeeld een ligamentruptuur. Mogelijk leidt dit tot een beschadiging aan een gewrichtskapel met lekkage van synoviaal vocht, dat zich ontwikkelt tot een gelatineuze vloeistof met een kapselwand. Ook is het mogelijk dat het leidt tot productie van een cyste door het omliggende weefsel. Een duidelijke relatie met werk of vrijetijdsbesteding ontbreekt.
Pathofysiologie en symptomatologie
Naar Samenvatting ›- De meeste ganglia liggen aan de dorsale zijde van de pols.
- Een peesschedeganglion is vaak te vinden aan de volaire zijde van het MCP-gewricht dan wel de proximale falanx.
- Een ganglion kan ook voorkomen aan de dorsale zijde van de DIP-gewrichten (mucoïdcyste).
- Een ganglion geeft dikwijls geen klachten. Soms is er sprake van paresthesieën, pijn, cosmetische bezwaren, subjectieve zwakte en/of angst voor een kwaadaardige oorzaak.
Het vaakst komt een ganglion voor aan de dorsale zijde van de pols (70%), minder vaak aan de palmaire zijde van de pols (30%). Er bestaat vaak een relatie met het kapsel van de intercarpale gewrichten, maar de vloeistof in een ganglion verschilt biochemisch van gewrichtsvloeistof en is visceuzer. Door vulling ontstaat een vast-elastische zwelling die een paar centimeter groot kan worden.
Een ganglion geeft dikwijls geen klachten. Volaire ganglia kunnen wel paresthesieën geven door compressie van de n. medianus of de n. radialis. In een meta-analyse van 14 onderzoeken noemde 71% van de patiënten pijn als reden voor presentatie, 34% cosmetische bezwaren en 27% subjectieve zwakte. Bij een deel van de patiënten speelt mogelijk ook angst voor een kwaadaardige oorzaak een rol in het verzoek om behandeling.
Beloop en prognose
Naar Samenvatting ›Een ganglion kan geleidelijk of abrupt ontstaan en de grootte kan fluctueren. Bij ongeveer de helft van de patiënten kan het ganglion ook weer spontaan verdwijnen.
In een prospectief cohortonderzoek ontvingen 38 patiënten met in totaal 39 palmaire ganglia alleen geruststelling. Bij hen verdwenen 20 ganglia (51%) spontaan. In een vervolgpublicatie verdwenen 23 van de 55 dorsale ganglia (58%) spontaan.
Artrose van de hand
Naar Samenvatting ›Epidemiologie
Naar Samenvatting ›- Bij gebrek aan een specifieke ICPC-code zijn er geen recente cijfers over de incidentie en prevalentie in de Nederlandse huisartsenpraktijk .
- De incidentie van handartrose in de huisartsenpraktijk bij patiënten > 45 jaar lijkt voor vrouwen hoger dan voor mannen (3,6 versus 1,1 per 1000 patiënten per jaar). De incidentie neemt toe met de leeftijd.
- Het merendeel van de mensen > 55 jaar heeft radiologische kenmerken van artrose van de hand of pols, maar slechts ongeveer 20% van hen heeft ook klinische symptomen.
Het merendeel van de mensen > 55 jaar heeft radiologische kenmerken van artrose in de hand of pols, maar slechts circa 20% heeft klinische symptomen.
Niet iedereen zoekt medische hulp voor artrose van de hand.
Doordat een specifieke ICPC-code ontbreekt, zijn er geen recente incidentie- en prevalentiecijfers beschikbaar uit de Nederlandse huisartsenpraktijk. Een Engels populatieonderzoek in de huisartsenpraktijk rapporteert voor patiënten > 45 jaar een incidentie van de diagnose ‘handartrose’ van 1,1 per 1000 (95%-BI 0,7 tot 1,6) bij mannen en 3,6 (95%-BI 2,9 tot 4,5) bij vrouwen.
Deze incidentie stijgt het sterkst in de leeftijdsgroep 55-64 jaar, piekt op 75-84 jaar en daalt daarna weer licht voor zowel mannen als vrouwen.
De prevalenties voor DIP-, PIP- en CMC1-artrose worden geschat op respectievelijk 35, 18 en 21%. In dit onderzoek werd de diagnose echter röntgenologisch gesteld en niet op basis van klachten. Er bestaat een hoge associatie tussen DIP- en PIP-artrose (OR 31,7; 95%-BI 13,8 tot 72,5), terwijl CMC1-artrose vaak solitair voorkomt.
Noduli van Heberden bij de DIP-gewrichten, noduli van Bouchard bij de PIP-gewrichten en deformaties van het CMC1-gewricht konden worden aangetoond in respectievelijk 58% (mannen 53, vrouwen 62%), 30% (mannen 25, vrouwen 33%) en 18% (mannen 10, vrouwen 24%).
Etiologie en pathofysiologie
Naar Samenvatting ›- Artrose komt ook vaak voor zonder aanwijsbare oorzaak (primaire artrose) of ten gevolge van een andere aandoening (secundaire artrose), zoals reumatoïde artritis (zie NHG-Standaard Artritis).
- Het verlies van gewrichtskraakbeen en de nieuwvorming van bot kunnen het gevolg zijn van:
- langdurige mechanische belasting
- eerder trauma
- (posttraumatische) instabiliteit van het gewricht
De Britse NICE-Guidelines benadrukken dat artrose niet slechts een degeneratief proces is, maar een actief metabool proces waarin verlies van gewrichtskraakbeen leidt tot toegenomen metabole activiteit van het subchondrale bot, wat zich uit in sclerosering en de vorming van subchondrale cysten (beide zichtbaar op een röntgenfoto) en verder leidt tot uitwendig waarneembare osteofyten en een ontstekingsreactie.
Dit betekent dat er bij artrose sprake is van een proces van reparatie. In het algemeen gaat het om een langzaam, maar efficiënt reparatieproces dat vaak kan compenseren voor de initiële schade. Bij een deel van de mensen kan de weefselschade echter niet worden gecompenseerd en ontstaan symptomen als pijn en stijfheid. Deze processen verklaren tevens waarom er zoveel variatie is in klinische presentatie van artrose, tussen verschillende personen, maar ook tussen verschillende gewrichten.
Mogelijk is er sprake van een genetische factor, maar het is nog niet duidelijk welke genen verantwoordelijk zijn.
Risicofactoren
Naar Samenvatting ›Factoren die mogelijk geassocieerd zijn met het ontwikkelen van artrose:
- leeftijd
- vrouwelijk geslacht
- overgewicht
- artrose in andere gewrichten
- eerder doorgemaakte fracturen
Prospectieve populatieonderzoeken laten diverse risicofactoren zien voor het ontwikkelen van symptomatische handartrose.
De belangrijkste factoren voor handartrose zijn:
- leeftijd
- vrouwelijk geslacht
- overgewicht
- artrose in andere (hand)gewrichten
- eerder doorgemaakte fracturen
Beloop en prognose
Naar Samenvatting ›- Het merendeel van de patiënten rapporteert mettertijd een toename van pijnklachten, maar artrose van de hand heeft niet altijd een progressief beloop.
- Progressie van de artrose gaat gepaard met verminderde knijpkracht van de handspieren.
- CMC1-artrose gaat doorgaans gepaard met meer functiebeperkingen dan PIP- of DIP-artrose.
- Pijnklachten bij artrose treden vaak op in exacerbaties (flares), die gepaard kunnen gaan met toegenomen stijfheid, warmte en hydrops (zie NHG-Standaard Artritis).
- Er is nog weinig bekend over de invloed van comorbiditeit, werkgerelateerde en/of arbeidsrelevante factoren en psychosociale factoren (angst, depressie, ziekteperceptie) op het beloop van de klachten.
Artrose van de hand heeft lang niet altijd een progressief beloop. Doordat het in principe een proces van herstel en modellering betreft, kunnen episoden van pijn en functiebeperkingen gevolgd worden door een langdurige periode zonder klachten, hoewel de benige verdikkingen, met name bij de DIP- en de PIP-gewrichten, blijven bestaan. Het merendeel van de patiënten rapporteert over een periode van 2 jaar wel een toename van pijnklachten en bij 20% is er tevens sprake van radiologische progressie. Progressie gaat samen met verminderde knijpkracht van de handspieren. Artrose van het CMC-gewricht gaat gepaard met meer beperkingen in functie dan artrose van de DIP- of PIP-gewrichten. De invloed van handartrose op het dagelijks functioneren is aanzienlijk, als gevolg van pijn, stijfheid, een verminderde knijpkracht en afname van fijne motoriek.
Er zijn nog weinig gegevens over de invloed van comorbiditeit, werkgerelateerde en/of arbeidsrelevante factoren op het beloop van klachten bij handartrose. Er zijn wel aanwijzingen dat psychosociale factoren (onder andere ziekte- en pijnperceptie) een negatieve invloed hebben op de pijnbeleving, maar of dit ook een negatief effect heeft op de behandelresultaten is onbekend.
Triggervinger en triggerduim
Naar Samenvatting ›Epidemiologie
Naar Samenvatting ›- De incidentie in de algemene Nederlandse bevolking is ongeveer 2,6%.
- Er zijn geen recente incidentie- en prevalentiecijfers beschikbaar uit de Nederlandse huisartsenpraktijk.
- De aandoening komt 4-6 × vaker voor bij vrouwen en relatief vaak in de leeftijdscategorieën 1-4 en 40-70 jaar.
- Doorgaans betreft het de ringvinger, de duim of de middelvinger en vaker de dominante hand.
Er zijn geen aparte gegevens bekend voor de incidentie en prevalentie van de diagnose ‘triggervinger’ (ICPC-code L99.04) in de Nederlandse huisartsenpraktijk. Op basis van de beperkt beschikbare literatuur wordt de incidentie in de algemene bevolking geschat op circa 2,6% Bij patiënten met diabetes is de incidentie circa 10%, bij de helft van deze patiënten zijn dan vaak meerdere vingers aangedaan. De aandoening komt 4-6 keer vaker voor bij vrouwen, en meer in de leeftijdscategorieën 1-4 jaar en 40-70 jaar.
Bij mensen zonder bijkomende ziekten is de duim het vaakst aangedaan, gevolgd door dig. III en IV.
Etiologie en pathofysiologie
Naar Samenvatting ›- Irritatie van de flexorpeesschede ter hoogte van de A1-pulley (zie Relevante anatomie) leidt tot een vernauwing van de peesschede met soms ook verdikking van de flexorpees (nodus van Notta).
- De oorzaak van een triggervinger is niet bekend. Hoewel vaak gesproken wordt van ‘tenosynovitis’ worden bij pathologisch anatomisch onderzoek geen verschijnselen van inflammatie gevonden, maar wel van fibrosering.
- Bij jonge kinderen lijkt een triggerduim veroorzaakt te worden door een diameterverschil tussen de m. flexor pollicis longus en de peesschede.
Een triggervinger of triggerduim (tendovaginitis stenosans) is een tenosynovitis van de flexorpezen van de vingers of de duim. Het soepele glijden van de buigpees in de A1-pulley (eerste annulaire ligament van de buigpeeskoker) proximaal van het MCP-gewricht raakt door zwelling belemmerd en de vinger kan moeilijker gestrekt of gebogen worden. Bij jonge kinderen is de oorzaak mechanisch en heeft een diameterverschil tussen de m. flexor pollicis longus en de peesschede een extensiebeperking tot gevolg.
De oorzaak van een triggervinger is niet altijd duidelijk. De klachten treden vaak op na een zware inspanning of abnormaal gebruik van de hand, wat doet vermoeden dat microtraumata een inflammatiebeeld uitlokken. Het is onduidelijk of er een daadwerkelijke causale relatie is tussen overbelasting en dit ziektebeeld, of dat veelvuldig gebruik van hand en pols er alleen maar toe leidt dat het ziektebeeld zich eerder en duidelijker manifesteert.
Moore stelt dat de term ‘tendovaginitis’ niet correct is omdat in histologische onderzoeken geen ontstekingsreactie is aangetoond.
Er is eerder sprake van fibrosering en tendinose.
De triggervinger lijkt geassocieerd te zijn met diabetes mellitus, reumatoïde artritis, hypothyreoïdie, CTS, jicht en repetitief gebruik van de vingers.
Risicofactoren
Naar Samenvatting ›Factoren die mogelijk geassocieerd zijn met het ontwikkelen van triggervinger:
- diabetes mellitus
- reumatoïde artritis
- hypothyreoïdie
- CTS-operatie
- jicht
- repeterende bewegingen van de vingers
Beloop en prognose
Naar Samenvatting ›- Er is zeer weinig onderzoek gedaan naar het natuurlijke beloop van een triggervinger, verondersteld wordt dat 20-29% spontaan herstelt.
- Een langdurig bestaande triggervinger kan leiden tot een flexiecontractuur van het PIP-gewricht.
Het aantal onderzoeken dat rapporteert over het natuurlijke beloop en de prognose van een triggervinger is zeer beperkt en gedateerd. Een literatuuroverzicht van Moore stelt op basis van 2 artikelen dat bij 20-29% van de volwassen patiënten spontaan herstel optreedt (423 triggervingers in 369 patiënten).
Contractuur van Dupuytren
Naar Samenvatting ›Epidemiologie
Naar Samenvatting ›- De prevalentie in de Nederlandse bevolking stijgt van 5% in de leeftijd 50-55 jaar tot 53% in de leeftijd 76-80 jaar. Bij de meeste patiënten zijn noduli en strengen aanwezig zonder flexiecontractuur.
- De exacte incidentie en prevalentie in de Nederlandse huisartsenpraktijk is niet bekend.
- De aandoening komt vooral voor bij mannen rond de 50 jaar, in die leeftijdsgroep 9 × zo vaak als bij vrouwen. Op latere leeftijd is de prevalentie bij mannen en vrouwen gelijk.
- Bij patiënten met een donkere huidskleur komt een contractuur van Dupuytren minder vaak voor.
Internationaal varieert de prevalentie in de algemene bevolking sterk (2-42%) door culturele verschillen. In een Nederlands cross-sectioneel onderzoek (n = 763) bij personen van 50-89 jaar was de prevalentie 22,1%. De prevalentie steeg met de leeftijd, van 5% bij patiënten van 50-55 jaar tot 53% bij patiënten van 76-80 jaar. Bij de meeste patiënten (81%) waren er noduli en strengen zonder flexiecontractuur.
Er zijn geen aparte gegevens bekend met betrekking tot de incidentie en prevalentie van de diagnose ‘contractuur van Dupuytren’ (ICPC-code L99.03) in de Nederlandse huisartsenpraktijk. Mannen zijn vaker aangedaan dan vrouwen en de aandoening komt vooral voor bij mannen rond de 50 jaar (bij vrouwen gemiddeld 10 jaar later). De aandoening komt vooral voor bij mensen met een Noordwest-Europese achtergrond en minder bij mensen met een Afrikaanse achtergrond. De ringvinger is het vaakst aangedaan, gevolgd door de pink en de middelvinger.
Etiologie en pathofysiologie
Naar Samenvatting ›Een contractuur van Dupuytren is een fibromatose van de fascia palmaris die leidt tot noduli en strengen in de handpalm en flexiecontractuur van de vingers. De aandoening komt bij 50% van de patiënten in beide handen voor. Als slechts 1 hand is aangedaan, betreft het meestal de dominante hand.
Risicofactoren
Naar Samenvatting ›Factoren die mogelijk geassocieerd zijn met het ontwikkelen van een contractuur:
- positieve familieanamnese voor Dupuytren
- leeftijd
- mannelijk geslacht
- handtrauma in de voorgeschiedenis
- ziekte van Ledderhose (fibromatose van de fascia plantaris)
- ziekte van Peyronie (fibromatose van de zwellichamen van de penis)
De ziekte heeft een genetische predispositie, waarbij er sprake lijkt te zijn van een autosomaal dominante overerving. Er bestaat een associatie met de ziekte van Ledderhose (Dupuytren aan de voet) en met de ziekte van Peyronie (verkromming van de penis tijdens erectie). De ziekte kan ontstaan na een trauma, maar ook als complicatie na een chirurgische ingreep zoals een CTS-release.
In de literatuur worden diabetes, roken, alcoholgebruik, epilepsie, hiv-seropositiviteit, leveraandoeningen en hypercholesterolemie meermaals gesuggereerd als risicofactoren. Deze resultaten zijn vaak echter niet gecorrigeerd voor leeftijd, of tegenstrijdig.
Beloop en prognose
Naar Samenvatting ›- Het beloop kent drie fasen:
- vroege fase: huidveranderingen en intrekkingen van de huid
- intermediaire fase: vorming van noduli en strengen
- late fase: ontstaan van contracturen
- De aandoening leidt niet altijd tot symptomatische contracturen van de vingers, maar blijft bij sommige patiënten beperkt tot de handpalm.
Een contractuur van Dupuytren verloopt globaal in de 3 genoemde fasen, maar er is variatie in het beloop. Bij het merendeel van de patiënten zullen geen (ernstige) flexiecontracturen van de vingers ontstaan, omdat de contractuur beperkt blijft tot de handpalm. Er zijn echter ook patiënten bij wie juist de vingercontracturen op de voorgrond staan. De prognose is slechter indien de eerste tekenen van de ziekte op jonge leeftijd bilateraal optreden en de aandoening voorkomt bij een familielid.
Tendovaginitis van De Quervain
Naar Samenvatting ›Epidemiologie
Naar Samenvatting ›- De prevalentie in de algemene Nederlandse bevolking is voor vrouwen 13 en voor mannen 5 per 1000 personen.
- De exacte incidentie en prevalentie in de Nederlandse huisartsenpraktijk is niet bekend.
- De aandoening komt vooral voor bij vrouwen van 35-55 jaar; relatief vaak tijdens de zwangerschap en in de periode dat borstvoeding gegeven wordt.
In afwezigheid van onderzoek en van een aparte ICPC-code ontbreken cijfers met betrekking tot de diagnose ‘tendovaginitis van De Quervain’ in de Nederlandse huisartsenpraktijk. In een Engels onderzoek onder de algemene bevolking (n = 9696) was de prevalentie voor mannen 0,5% en voor vrouwen 1,3%. Bij vrouwen komt de aandoening voornamelijk voor in de leeftijd 35-55 jaar, tijdens zwangerschap en borstvoeding.
Etiologie en pathofysiologie
Naar Samenvatting ›- De pezen van de m. abductor pollicis longus en m. extensor pollicis brevis lopen doorgaans gezamenlijk in 1 compartiment aan de radiale zijde van de pols. Door verdikking van de peesschede rondom deze pezen ontstaat een relatieve vernauwing van het compartiment met irritatie van de pezen tot gevolg.
- Hoewel er wel gesproken wordt van ‘tendovaginitis’ worden er bij pathologisch anatomisch onderzoek geen verschijnselen van inflammatie gevonden.
Bij tendovaginitis van De Quervain is er sprake van verdikking en vernauwing van het kanaal aan de duimzijde van de pols waardoorheen de pezen lopen van de m. extensor pollicis brevis en de m. abductor pollicis longus. Hoewel de term ‘tendovaginitis’ een inflammatoire oorzaak doet vermoeden, is er histopathologisch sprake van verdikking en myxoïde degeneratie bij waarschijnlijk chronische overbelasting.
Kaukasische vrouwen > 60 jaar lijken een hogere kans te hebben op het ontwikkelen van de aandoening. Vaak wordt ook aangenomen dat de klachten worden veroorzaakt door overbelasting van de duim. Deze associatie is echter niet terug te vinden in de wetenschappelijke literatuur, behoudens in onderzoeken geplaagd door significante bias.
Enkele factoren zijn mogelijk geassocieerd met het ontwikkelen van De Quervain. Bij een onderzoek onder 3710 Franse werknemers bleek er op basis van gestandaardiseerd lichamelijk onderzoek sprake van De Quervain bij 45 deelnemers. Persoonlijke risicofactoren waren toenemende leeftijd en vrouwelijk geslacht (OR 4,9; 95%-BI 2,4 tot 10,1]. Werkgerelateerde factoren waren onder andere herhaalde of langdurige polsflexie in een extreme stand (OR 2,6; 95%-BI 1,3 tot 5,3) en repeterende schroefbewegingen (OR 3,4; 95%-BI 1,7 tot 7,1). Dezelfde werkgerelateerde factoren komen ook naar voren in een systematische review van 7 onderzoeken.
Risicofactoren
Naar Samenvatting ›Factoren die mogelijk geassocieerd zijn met het ontwikkelen van De Quervain:
- hogere leeftijd
- vrouwelijk geslacht
- activiteiten waarbij de pols herhaaldelijk gebogen wordt in een extreme positie
Malletvinger
Naar Samenvatting ›Epidemiologie
Naar Samenvatting ›- Bij gebrek aan een specifieke ICPC-code en onderzoek in de eerste lijn is de incidentie en prevalentie van malletvinger in de huisartsenpraktijk niet bekend.
- Vaak betreft het dig. III-V bij jongere mannen en bij oudere vrouwen.
Etiologie en pathofysiologie
Naar Samenvatting ›- De malletvinger ontstaat door ruptuur van de extensorpees bij de aanhechting aan de distale falanx wanneer deze met kracht gebogen wordt. Klassiek gebeurt dit tijdens het sporten, zoals bij basketbal, voetbal(keepers) of volleybal, maar het kan ook optreden bij tal van dagelijkse activiteiten, zoals het opmaken van bedden.
- Bij ouderen kan reeds een gering trauma leiden tot een malletvinger.
Beloop en prognose
Naar Samenvatting ›Een onbehandelde malletvinger kan leiden tot een zwanenhalsdeformiteit (swan-neck deformity) en DIP-artrose.
Er zijn geen incidentie- en prevalentiecijfers beschikbaar uit de Nederlandse praktijk.
De verdeling over leeftijd, geslacht en aangedane vinger lijkt afhankelijk van het soort populatie die onderzocht wordt. Wel lijkt een malletvinger frequenter te ontstaan bij jonge mannen, vaak op basis van een substantieel trauma. Ook oudere vrouwen zijn vaak aangedaan, maar dan na een relatief klein trauma. Doorgaans betreft het de wijs- of middelvinger of de pink.
Onbehandeld leidt een malletvinger tot een zwanenhalsdeformiteit door hyperextensie van het PIP-gewricht en flexie, en mogelijk artrose, van het DIP-gewricht.
Richtlijnen diagnostiek
Naar Samenvatting ›Bij specifieke hand- en polsaandoeningen zijn anamnese en gericht lichamelijk onderzoek (inspectie, palpatie en bewegingsonderzoek) in de regel voldoende om de diagnose te stellen en andere diagnoses onwaarschijnlijker te maken (zie Evaluatie van niet-traumatische klachten en tabel 1).
Diagnostiek algemeen
Naar Samenvatting ›Anamnese
Naar Samenvatting ›Algemene vragen
Naar Samenvatting ›Vraag naar:
- aanleiding, tijdstip (ochtend, nachtelijk) en verloop van de klachten in de tijd
- ernst van de klachten (intermitterend of continu aanwezig, werkverzuim)
- dominante of niet-dominante hand
- dagelijkse bezigheden (werk, hobby’s) en bijbehorende hand- en polsbewegingen
- zelf reeds geïnitieerde behandeling
- zwangerschap
- voorgeschiedenis:
- vergelijkbare klachten, eerder letsel, (niet-recent) trauma, eerdere voorgeschreven of chirurgische behandelingen
- diabetes of hart- en vaatziekten
- artrose, jicht, reuma of andere gewrichtsklachten, met name ipsilaterale nek-, schouder- of elleboogklachten
Specifieke vragen over de klachten
Naar Samenvatting ›Denk aan 4 soorten klachten:
- pijn:
- ernst, lokalisatie en (bi)lateraliteit
- nachtelijke pijn, klachten bij activiteit of juist in rust
- bij specifieke bewegingen (dragen van een bord, sleutel omdraaien) of bewegingen die door pijn niet meer mogelijk zijn
- veranderingen in sensibiliteit (tintelingen, prikkelingen, hypo- of hyperesthesie)
- stijfheid (continu, na rust (ochtendstijfheid) of met name na activiteit)
- zwakte (vastpakken en vasthouden)
- klikken (mogelijk teken van instabiliteit)
Een Engels onderzoek formuleerde op basis van een delphiconsensusprocedure handvatten voor structureel anamnestisch en lichamelijk onderzoek bij hand- en polsklachten in de eerste lijn. Voor deze standaard zijn die handvatten aangevuld op basis van een overzichtsartikel over klinische evaluatie van de pols.
Lichamelijk onderzoek
Naar Samenvatting ›- Verricht oriënterend lichamelijk onderzoek
- Vergelijk de klachten met de niet aangedane zijde
- Vul het lichamelijk onderzoek aan met meer specifiek onderzoek op geleide van de klachten.
Inspectie
Naar Samenvatting ›- Houding van de betrokken extremiteit en rusthouding van de hand
- Zwelling, atrofie, noduli of strengen
- Kleur en doorbloeding (aanwijzingen voor trofische stoornissen)
- Deformiteiten aan de pols of aan het MCP- (subluxatie, deviatie), DIP- of PIP-gewricht (flexiecontractuur, zwanenhals- of boutonnièredeformiteit)
Beweging en functie
Naar Samenvatting ›- Flexie, extensie, ulnaire en radiare deviatie, pro- en supinatie
- Oriënterend onderzoek van bewegingen bij ADL-activiteiten (voor de pols: dart throwing motion; voor de vingers: vuist maken)
- Onhandigheid in motoriek (vaak een uiting van licht sensibiliteitsverlies)
- Kracht (grijpkracht)
De dart throwing motion
Vraag de patiënt een (denkbeeldige) pen vast te houden en daarmee een werpbeweging te maken alsof het een dartpijltje was. Omdat het een samengestelde beweging betreft, worden zowel flexie-extensie en radio-ulnaire deviatie als rotatie getest. Deze beweging geeft een indruk van de polsmobiliteit die nodig is voor veel dagelijkse activiteiten.
Aanvullend onderzoek
Naar Samenvatting ›- Vraag alleen aanvullend onderzoek aan als dit consequenties heeft voor het beleid; doorgaans is aanvullend onderzoek niet bijdragend.
- Voor indicaties en mogelijkheden bij de meest voorkomende specifieke aandoeningen, zie de specifieke diagnostische richtlijn per aandoening in deze standaard.
Evaluatie van niet-traumatische klachten
Naar Samenvatting ›Zie tabel 1 voor de meest voorkomende niet-traumatische aandoeningen.
| Lokalisatie | Aandoening | Belangrijkste symptomen |
|---|---|---|
| Pols en/of vingers | Carpaletunnelsyndroom | (Nachtelijke) paresthesieën in voornamelijk dig. I-III en de radiale zijde van dig. IV en de aansluitende handpalmregio. Wapperen met de hand kan verlichting geven (zie ook Diagnostiek bij carpaletunnelsyndroom) |
| Ganglion | Gladde ronde, meestal pijnloze en vast-elastische zwelling, gefixeerd aan de onderlaag, vaak aan de dorsale zijde van de pols of bij de DIP-gewrichten. Er kan drukpijn zijn ter plaatse of ter hoogte van de overgang van het scafoïd en het lunatum (zie ook Diagnostiek bij ganglion) | |
| Vingers | Artrose van de PIP- en DIP- gewrichten | Pijn, zwelling, stijfheid en/of bewegingsbeperking van PIP- en DIP-gewrichten (zie ook Diagnostiek bij handartrose) |
| Triggervinger of triggerduim | ‘Hokken’ bij strekken van de vinger of duim vanuit diepe flexie, pijn bij buigen en/of drukpijn en zwelling palmair ter plaatse van het MCP-gewricht en de A1-pulley (zie ook Diagnostiek bij triggervinger) | |
| Handpalm | Contractuur van Dupuytren | Vast-elastische, soms pijnlijke verdikkingen en/of strengen in de handpalm met geleidelijk progressieve flexiecontractuur van de vingers (zie ook Diagnostiek bij contractuur van Dupuytren) |
| Radiale zijde pols | Tendovaginitis van De Quervain | Lokale (druk)pijn en/of zwelling aan radiale zijde van de pols, met name over de m. abductor pollicis longus en m. extensor pollicis brevis (zie ook Diagnostiek bij tendovaginitis van De Quervain) |
| Radiale zijde pols/duimbasis | Artrose van het CMC1-gewricht | Pijn, zwelling, stijfheid en/of bewegingsbeperking van het CMC1-gewricht (zie ook Diagnostiek bij handartrose) |
| Midcarpaal/pols | Ligamentaire hyperlaxiteit, carpale instabiliteit, scafolunaire disfunctie, posttraumatisch letsel | Pijnklachten midcarpaal en rond de pols, eventueel met giving way en klikken; mogelijk trauma in het verleden (val op de uitgestrekte hand) (zie ook Meer aspecifieke midcarpale hand- en polsklachten) |
Atypische of slecht te duiden klachten
Naar Samenvatting ›- Maak bij klachten die atypisch zijn of die niet binnen een duidelijke diagnose passen een inschatting van:
- de ernst van de klachten en beperkingen
- de verwachtingen van de patiënt ten aanzien van diagnostiek en behandeling
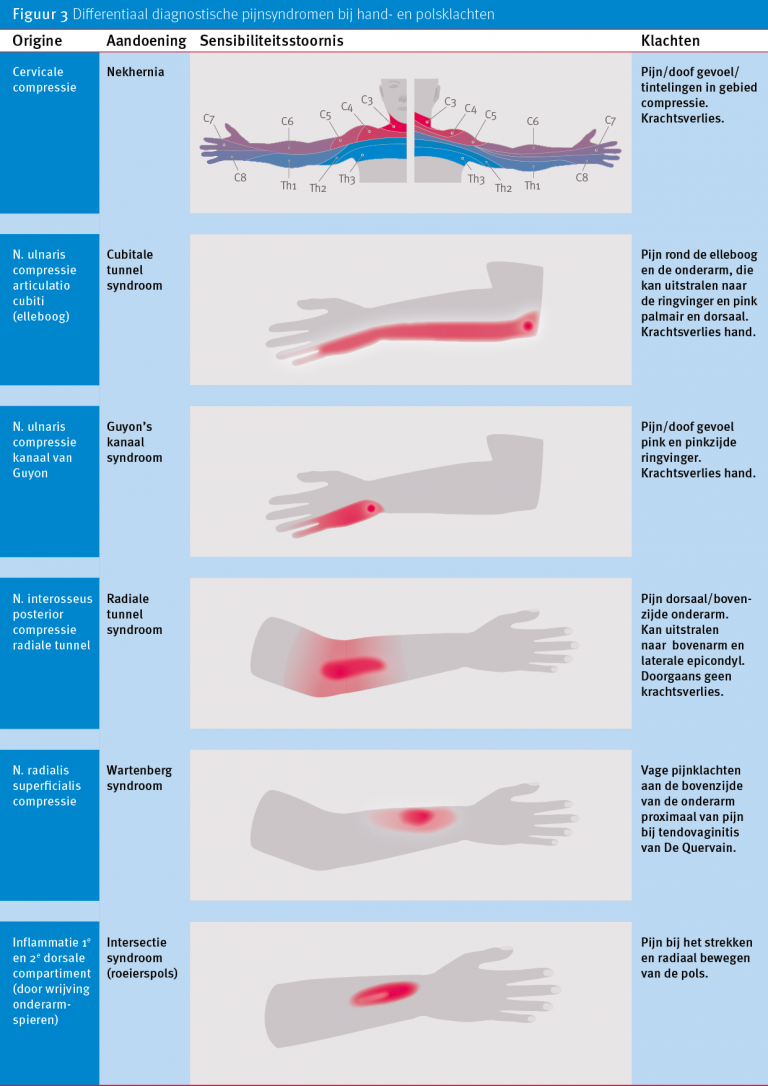
- Denk bij atypische of slecht te duiden pijnklachten die gepaard gaan met tintelingen of veranderingen in sensibiliteit ook aan:
- neurogene compressie cervicaal, rond de elleboog of rond de pols
- complex regionaal pijnsyndroom (CRPS).
Met name bij atypische of slecht te duiden pijnklachten die gepaard gaan met tintelingen of veranderingen in sensibiliteit kan er sprake zijn van neurogene compressie cervicaal, rond de elleboog of rond de pols. De belangrijkste neurogene syndromen staan beschreven in figuur 3.
Meer aspecifieke midcarpale hand- en polsklachten
Naar Samenvatting ›- Zowel de eerste als in de tweede lijn vormen aspecifieke midcarpale hand- en polsklachten een diagnostisch dilemma voor behandelaars. Er zijn substantiële lacunes in de kennis met betrekking tot diagnostiek en beleid.
- Wees bij aspecifieke midcarpale hand- en polsklachten bedacht op de gevolgen van een trauma in het verleden, zoals scafolunaire disfunctie, carpale instabiliteit of (late gevolgen van een) scafoïdfractuur. Tijdige onderkenning kan een verschil maken in het beloop.
- Overweeg bij twijfel over de diagnose laagdrempelige verwijzing of consultatie.
Er kan een scala aan (combinaties van) oorzaken ten grondslag liggen aan aspecifieke midcarpale hand- en polsklachten. Het is wenselijk om, voor zover mogelijk in de eerste lijn, onderscheid te maken tussen oorzaken met een milde prognose en oorzaken waarbij tijdige onderkenning een verschil kan maken in het beloop.
Ligamentaire hyperlaxiteit
Gegeneraliseerde polsklachten zonder voorafgaand trauma kunnen een uiting zijn van ligamentaire hyperlaxiteit.
- Bij deze klachten is er sprake van een te grote en abnormale beweeglijkheid tussen de carpale rijen onderling en het radiocarpale gewricht (en niet tussen 2 carpalia, zoals bij scafolunaire instabiliteit).
- De pijnklachten kunnen optreden bij abrupte bewegingen in de pols en kunnen gepaard gaan met een gevoel van blokkade en/of controleverlies. De abrupte bewegingen zijn aanvankelijk niet pijnlijk en kunnen gepaard gaan met een hoorbare of voelbare laagfrequente klik (clunck).
- De klachten treffen vooral jonge vrouwen. Vaak zijn beide polsen aangedaan.
- Een ‘occult ganglion’ kan een uiting zijn van deze instabiliteit.
- De klachten leiden in de regel niet tot vervroegde artrose.
Posttraumatische letsels bij hand- en polsklachten
Letsel van het ligamentum scapholunatum(SL-letsel)
Gegeneraliseerde polsklachten kunnen ook het gevolg zijn van disfunctie van de carpalia. Het meest voorkomend hierbij is SL-letsel.
- SL-letsel kan ontstaan na een acuut trauma of als gevolg van chronische degeneratie.
- Drukpijn aan de dorsale zijde van de pols juist distaal van de rand van de radius kan duiden op letsel van het SL-ligament.
- De aandoening kan leiden tot klachten van scafolunaire instabiliteit of dissociatie, zoals progressieve pijn, bewegingsbeperking en zwelling.
- Onbehandeld zullen deze instabiliteitsklachten leiden tot vroegtijdige artrose in het radiocarpale en het midcarpale gewricht. Deze scapholunate advanced collapse (SLAC-wrist) kan invaliditeit tot gevolg hebben.
(Occulte) fractuur of pseudoartrose van het scafoïd
- De voorgeschiedenis vermeldt vaak een val op de uitgestrekte hand.
- Er is persisterende (druk)pijn over de anatomische snuifdoos, het proximale deel van de duimmuis (proximale scafoïdpool) en bij pronatie van de hand tegen weerstand.
- Een onbehandelde scafoïdfractuur kan leiden tot necrose van de proximale pool, gevolgd door artrose van het radiuskopje, het capitatum en uiteindelijk alle carpalia: scaphoid nonunion advanced collapse (SNAC-wrist).
- De behandelopties zijn beperkter naarmate de bijkomende artrose vordert.
Diagnostiek bij carpaletunnelsyndroom
Naar Samenvatting ›- Er bestaat geen gouden standaard voor de diagnose ‘CTS’.
- Maak op basis van anamnese en lichamelijk onderzoek onderscheid tussen:
- ‘klassiek CTS’
- ‘mogelijk CTS’
- diagnose CTS onwaarschijnlijk (zie Evaluatie CTS).
Over de diagnostiek van CTS in de eerste lijn zijn geen onderzoeken bekend, maar ook in de tweede lijn is er geen eenduidige definitie van CTS, bij gebrek aan een algemeen geaccepteerde gouden standaard voor de diagnose ‘CTS’. Afwijkende resultaten van aanvullend onderzoek staan niet altijd in relatie tot de aanwezigheid en ernst van klachten, deels omdat de hoofdklacht (paresthesieën en pijn) niet objectief meetbaar is. Daarnaast laat aanvullend onderzoek met een EMG of echo pas afwijkingen zien bij functieverlies en/of anatomische veranderingen aan de n. medianus als gevolg van langer bestaande compressie. Ook kan het klinische beeld variëren. Een atypische presentatie komt herhaaldelijk voor, met sensibele stoornissen die niet corresponderen met het verzorgingsgebied van de n. medianus.
In deze standaard wordt een onderverdeling gemaakt in ‘klassiek CTS’ en ‘mogelijk CTS’. Dit is in overeenstemming met de multidisciplinaire Richtlijn Carpaletunnelsyndroom, geïnitieerd door de Nederlandse Vereniging van Neurologie, die de definitie van de American Academy of Neurology (AAN) en de American Academy of Orthopedic Surgeons (AAOS) gebruikt. In de Britse eerste lijn is een (uitgebreider) diagnostisch algoritme beschikbaar, maar ter wille van de landelijke overeenstemming sluit deze standaard aan bij de Nederlandse multidisciplinaire richtlijn.
Anamnese
Naar Samenvatting ›- De anamnese is gericht op het vaststellen van de aan- of afwezigheid van typische klachten voor CTS en het bepalen van de ernst en hinder van de klachten.
- Vraag naar:
- paresthesieën of tintelingen (met name in dig. I-III)
- nachtelijke klachten en wakker worden van deze klachten
- krachtsverlies (voorwerpen uit de handen laten vallen)
- invloed van specifieke bewegingen (verbetering bij wapperen of warm water; toename bij flexie van de pols of compressie volair zoals bij autorijden, telefoneren, typen of gebruik van vibrerend handgereedschap)
- eerdere behandeling en effect hiervan (spalken, injecties, handtherapie, operaties)
Lichamelijk onderzoek
Naar Samenvatting ›- Het lichamelijk onderzoek kan de diagnose aannemelijker maken, maar dient vooral om een indruk te krijgen van de ernst van de aandoening.
- Lichamelijk onderzoek is ook van belang wanneer de anamnese aanleiding geeft om aan andere aandoeningen dan CTS te denken.
- Onderzoek klachten en afwijkingen die passen bij ernstig CTS; deze hebben een negatieve prognostische waarde omdat ze in een laat stadium optreden (krachtsverlies is echter weinig specifiek voor CTS):
- atrofie van de thenar
- krachtsverlies van de m. abductor pollicis brevis (verminderde kracht bij abductie van de duim tegen weerstand)
- krachtsverlies van de m. opponens pollicis (verminderde kracht bij het drukken van de duim tegen de top van de pink)
- We bevelen provocatietests niet aan omdat hun diagnostische waarde beperkt is.
Atrofie en krachtsverlies
Atrofie van de duimmuis en krachtsverlies van de m. abductor pollicis brevis zijn weinig specifieke, maar wel klinisch relevante aanwijzingen voor het bestaan van een CTS. Deze aanwijzingen zijn te testen door de kracht bij abductie en adductie van de duim tegen weerstand te testen.
Provocatietests
Provocatietests zijn wijdverbreid in zowel de eerste als de tweede lijn.
Er is echter kritiek op het gebruik ervan wegens de geringe negatief voorspellende waarde en het gebrekkige onderscheidend vermogen tussen CTS en andere oorzaken voor paresthesieën in de hand, zoals cervicale radiculopathie, een neurogeen thoracic outlet syndrome, ulnaropathie of polyneuropathie. Onderzoeken naar de testeigenschappen zijn van lage kwaliteit.
Een meta-analyse uit 2013 berekende de likelihood ratio’s (LR) voor de meest voorkomende hand- en elleboogtests.
Een LR > 2,0 voor een positieve testuitslag wordt gezien als bijdragend, voor een negatieve testuitslag is dat een LR < 0,5.
In dit onderzoek voldeden 2 provocatietests aan de genoemde criteria.
- Test van Phalen
- uitvoering: volledige palmair flexie van de pols met de elleboog in volledige flexie en de onderarm in pronatie
- positief indien < 1 minuut representatieve symptomen ontstaan
- de gemiddelde LR in 5 geïncludeerde onderzoeken was voor een positieve testuitslag 2,68 en voor een negatieve testuitslag 0,54
- Teken van Tinel:
- uitvoering: percussie van de n. medianus ter hoogte en net proximaal van de carpale tunnel bij een ontspannen pols in circa 20° extensie
- de gemiddelde LR in 5 geïncludeerde onderzoeken was voor een positieve testuitslag 2,95 en voor een negatieve testuitslag 0,57
- Voor de overige tests waren slechts gegevens uit 1 onderzoek beschikbaar (symptom relief manoeuvre, flick sign), of liepen de gegevens erg uiteen (Durkan’s compression test).
Conclusie
Het bewijs voor de diagnostische waarde van provocatietests bij CTS is laag. De negatief voorspellende waarde is gering en met de tests kan geen onderscheid worden gemaakt tussen CTS en andere neurologische hand- en armpathologie.
Aanvullend onderzoek
Naar Samenvatting ›- Bij twijfel over de diagnose: overweeg aanvullende diagnostiek alvorens te starten met behandeling.
- De keuze voor EMG, zenuwechografie of verwijzing voor aanvullend onderzoek is afhankelijk van de lokale afspraken en beschikbaarheid (zie ook Consultatie en verwijzing).
Het stellen van de diagnose ‘klassiek CTS’ op basis van alleen anamnese en lichamelijk onderzoek is in overeenstemming met de multidisciplinaire richtlijn, op basis van de volgende overwegingen.
- Bij een klassieke presentatie is de toegevoegde waarde van aanvullend onderzoek in de vorm van een EMG of zenuwecho beperkt, gezien de hoge pretestwaarschijnlijkheid van de aanwezigheid van CTS.
- De meest voorkomende symptomen van CTS (tintelingen en pijn) zijn niet objectiveerbaar met aanvullend onderzoek. Bovendien laat aanvullend onderzoek pas in een laat stadium afwijkingen zien, namelijk als er reeds anatomische afwijkingen zijn (zenuwecho) of bij functieverlies van de n. medianus (zenuwgeleidingsonderzoek). Deze afwijkingen correleren niet altijd met de ernst van de ervaren klachten.
- Ruim 80% van de diagnoses ‘CTS’ door een niet-tweedelijns specialist, zoals een huisarts, wordt bevestigd in de tweede lijn.
Evaluatie CTS
Naar Samenvatting ›Klassiek CTS
Naar Samenvatting ›Stel de diagnose ‘klassiek CTS’ indien alle onderstaande 5 kenmerken aanwezig zijn:
- volwassen patiënt
- tintelingen, al dan niet met pijn en een doof gevoel, in het verdelingsgebied van de n. medianus
- patiënt wordt ’s nachts wakker van de klachten
- de klachten worden erger of juist minder door bepaalde houdingen of bewegingen van de hand en pols (bijvoorbeeld vermindering door wapperen)
- anamnese en lichamelijk onderzoek geven geen aanwijzingen voor een andere oorzaak
Mogelijk CTS
Naar Samenvatting ›Bij < 5 van de bovengenoemde kenmerken is er geen sprake van een klassiek, maar van een mogelijk CTS. Symptomen die ook bij CTS kunnen passen, zijn:
- functievermindering van de hand in de ochtenduren
- klachten die bij het voortschrijden van de aandoening ook overdag bestaan
- krachtsverlies
- klachten in de gehele hand met soms ook uitstraling naar de arm
- De diagnose ‘mogelijk CTS’ is een indicatie voor aanvullend onderzoek (zie Aanvullend onderzoek).
Differentiaaldiagnose
Naar Samenvatting ›Diagnostiek bij ganglion
Naar Samenvatting ›De diagnose ‘ganglion’ kan op basis van anamnese en lichamelijk onderzoek goed gesteld worden.
Anamnese
Naar Samenvatting ›Vraag naar:
- aard en ernst van de klachten (pijnklachten, cosmetische bezwaren, subjectieve zwakte)
- verwachtingen ten aanzien van het consult en de behandeling (geruststelling, verwijdering)
- eerdere klachten, eventuele behandeling hiervan
- eventuele (onterechte) angst voor een maligne aandoening
Lichamelijk onderzoek
Naar Samenvatting ›- Noteer de plaats in relatie tot de gewrichten of pezen van de hand en pols.
- Palpeer de zwelling en let op fixatie van de zwelling aan de onderlaag.
- Let bij volaire ganglia op paresthesieën door compressie op de n. medianus of n. ulnaris.
- Bij twijfel: doorlicht de zwelling in een donkere ruimte met een fel lampje (diafanoscopie).
- Wees alert op aspecten die kunnen duiden op een alternatieve diagnose (slecht afgrensbare, diepliggende of ossale zwelling; progressief groeiend of pijnlijk; niet lichtdoorlatend bij diafanoscopie).
De diagnose is goed te stellen door klinisch onderzoek.
- Bij het lichamelijk onderzoek voelt men een gladde en vast-elastische zwelling, gefixeerd aan de onderlaag.
- Bij diafanoscopie doorlicht een ganglion helder.
- Dorsaal bevinden ganglia zich vaak ter hoogte van de pols (ter hoogte van het scafolunaire ligament).
- Volaire ganglia komen minder vaak voor. Deze zijn doorgaans aanwezig ter hoogte van de polsplooi en gaan vaak uit van het radiocarpale gewricht of van het gewricht tussen scafoïd en trapezium. Hierbij kan compressie ontstaan van de n. medianus of n. ulnaris, met paresthesie of zwakte als gevolg.
Aanvullend onderzoek
Naar Samenvatting ›- Overweeg echografie bij twijfel over de diagnose (atypische lokalisatie of aspect van de laesie) om alternatieve diagnosen uit te sluiten (zie Evaluatie ganglion).
- Wees terughoudend met aspiratie pro diagnosi. Aspiratie heeft slechts beperkte diagnostische waarde en als (gelijktijdige) behandeling van een ganglion is het niet effectiever dan afwachtend beleid (zie Aspiratie).
Evaluatie ganglion
Naar Samenvatting ›- Stel de diagnose ‘ganglion’ bij een gladde en vast-elastische tot zeer vaste zwelling, gefixeerd aan de onderlaag ter hoogte van het DIP-gewricht, de pols (doorgaans dorsale zijde) of de overgang tussen het os scaphoideum en het os lunatum.
- Bij twijfel bevestigt diafanie bij doorlichten of echografie de diagnose.
- Bestaat er hinder bij een polsganglion, denk dan ook aan carpale instabiliteit als onderliggende oorzaak (zie Meer aspecifieke midcarpale hand- en polsklachten).
Differentiaaldiagnose
Naar Samenvatting ›- Noduli bij handartrose of jicht
- Tumoren:
- rond de pols: bijvoorbeeld lipoom of sarcoom (negatieve diafanoscopie)
- aan de vingers en metacarpalia: met name enchondromen
- Synovitis (van een extensorloge) van de pols
- Een ganglion kan een uiting zijn van onderliggend lijden aan de pols, denk aan:
- carpale instabiliteit of artrose
- chronisch scafolunair letsel
- niet-genezen hand- of polsfractuur
Diagnostiek bij handartrose
Naar Samenvatting ›Anamnese
Naar Samenvatting ›- Vraag specifiek naar:
- leeftijd van de patiënt (> 45 jaar)
- aanwezigheid en duur van startstijfheid (< 30 minuten)
- lokalisatie van de klachten (doorgaans DIP- en PIP-gewrichten of CMC1). Bij CMC1-artrose worden pijnklachten in de duimmuis ter hoogte van de handpalm aangegeven
- Vraag naar andere aspecten die passen bij artrose:
- krachtsverlies in de hand
- in het verleden doorgemaakt trauma van de hand (met name fracturen)
- pijn bij wringende bewegingen (veelvoorkomende klacht bij artrose van het CMC1-gewricht), bijvoorbeeld pincet- of sleutelgreep
- beperkingen in activiteiten door verminderde handkracht en souplesse
- klachten aan andere gewrichten die duiden op artrose (vooral knie of heup)
Diagnostische criteria voor handartrose zijn vastgesteld in de NICE-richtlijn:
- leeftijd > 45 jaar, en
- pijn tijdens bewegen in ≥ 1 gewricht, en
- geen of kortdurende (< 30 minuten) stijfheid in de ochtend of bij bewegen na een periode van rust.
Dezelfde NICE-richtlijn benadrukt het belang van een ‘holistische aanpak’ in de analyse en behandeling van patiënten met handartrose.
- Invloed op sociale activiteiten en gewenste levensstijl
- Beroepsmatige beperkingen, aanpassingen en voorzieningen
- Psychologische effecten van pijn en andere bestaande stressoren
- Aan- of afwezigheid van een (adequaat) steunnetwerk
- Andere pijnklachten, al dan niet in het kader van een chronisch pijnsyndroom
- Houding ten opzichte van beweging
- Comorbiditeit
- Zelfbehandeling en copingstrategieën
Lichamelijk onderzoek
Naar Samenvatting ›- Stel vast welke gewrichten zijn aangedaan en onderzoek de aanwezigheid van anatomische afwijkingen als gevolg van langer bestaande artrose.
- PIP- en DIP-gewrichten: benige verdikkingen bij de PIP-gewrichten (noduli van Bouchard) of bij de DIP-gewrichten (noduli van Heberden); noduli hoeven echter niet aanwezig te zijn
- CMC1-gewricht:
- pijn en zwelling rond de basis van de duim
- palpeer het CMC1-gewricht net distaal van tabatière anatomique en polsgroeve volair.
- beoordeel de aanwezigheid van pijn en crepiteren in het CMC1-gewrichtbij flexie-extensie, rotatie en/of axiale tractie en compressie.
- zwanenhals- of Z-deformiteit bij collaps van de duim; de adductiecontractuur van het CMC1-gewricht met hyperextensie van het MCP1-gewricht geeft een vierkant aspect aan de hand (square hand).
- Test het scafotrapeziotrapezoïdale gewricht (STT) proximaal van het CMC1-gewricht.
CMC1-artrose
- Zwelling dorsoradiaal rond de basis van duim kan ontstaan door een gewrichtsontsteking en osteofytvorming in het CMC1-gewricht.
- Er zijn verschillende specifieke tests voor het CMC1-gewricht:
- grinding test: pijn en crepiteren bij axiale compressie gecombineerd met rotatie van MC1.
- crank test: pijn en crepiteren bij axiale compressie gecombineerd met passieve flexie-extensie van MC-1.
- distraction-torque test: pijn bij roteren van basis MC-1 met tegelijkertijd axiale tractie. Deze test is suggestief voor synovitis bij mildere ziekte.
STT-artrose
- Nieuw, zowel in deze standaard als in de multidisciplinaire richtlijn Primaire artrose van de duimbasis, is het advies om het scafotrapeziotrapezoïde gewricht (STT-gewricht) apart te testen ter differentiatie.
- Het STT-gewricht is palpabel proximaal van het CMC1-gewricht, volair ter plaatse van het tuberkel van het scafoïd en radiaal net distaal van de anatomische snuifdoos.
Aanvullend onderzoek
Naar Samenvatting ›- Laboratoriumonderzoek (onder andere CRP) is niet geïndiceerd bij artrose (zie NHG-Standaard Artritis).
- We bevelen röntgenonderzoek voor de stadiëring van artrose niet aan vanwege de discrepantie tussen radiologische kenmerken en de klinische symptomen van artrose van de hand of pols.
Evaluatie handartrose
Naar Samenvatting ›- Stel de diagnose ‘handartrose’ op basis van anamnese en lichamelijk onderzoek bij:
- leeftijd > 45 jaar
- geen of kortdurende stijfheid (< 30 minuten) bij bewegen in de ochtend of na een periode van rust
- pijn (en crepitaties) tijdens bewegen in een of meer hand- en polsgewrichten (onderscheid in ieder geval PIP-, DIP-, CMC1- en/of STT-artrose).
- Let op het bestaan van een andere aandoening (CTS, tendinitis rond de pols), die mogelijk gelijktijdige behandeling behoeft.
Differentiaaldiagnose
Naar Samenvatting ›- Reumatoïde artritis (leeftijd bij diagnose vaak < 40 jaar, minder vaak symmetrische klachten, met name pols-, MCP- en PIP-gewrichten aangedaan zonder DIP-gewrichten, noduli, ochtendstijfheid > 60 min)
- Andere vormen van artritis (zie NHG-Standaard Artritis)
- Denk bij de jongere patiënt met langer bestaande klachten met een (mild) trauma in de voorgeschiedenis aan (uitgebreid) posttraumatisch letsel (zie Meer aspecifieke midcarpale hand- en polsklachten).
- Aanvullende differentiaaldiagnose bij CMC1-artrose:
- (begeleidende) STT-artrose
- tendovaginitis van De Quervain (proximale radiale pijnklachten)
Diagnostiek bij triggervinger
Naar Samenvatting ›Anamnese
Naar Samenvatting ›- Vraag specifiek naar belemmeringen bij het buigen of strekken van de vinger of duim en begeleidende pijnklachten
- Schat de ernst van de functiebeperking van de triggervinger in:
- verstoorde beweging van de vinger
- blokkade die zelf kan worden verholpen
- blokkade die ‘doorbewogen’ moet worden
- gefixeerde contractuur
- Onderzoek de andere vingers en de contralaterale hand op tekenen van bijkomende triggervingers
- Vraag naar risicofactoren die mogelijk geassocieerd zijn:
- diabetes
- reumatoïde artritis
- hypothyreoïdie
- jicht
- CTS-operatie
- repeterende vingerbewegingen bij (werkgerelateerde) activiteiten en hobby’s
De diagnose ‘triggervinger’ of ‘triggerduim’ is klinisch goed te stellen. De ernst van de klachten kan worden vastgelegd met behulp van de indeling volgens Quinell:
- graad I: verstoorde beweging van de vinger
- graad II: blokkade die zelf kan worden verholpen
- graad III: blokkade die ‘doorbewogen’ moet worden
- graad IV: gefixeerde contractuur
Deze indeling geeft een beschrijving van de functionele klachten, maar heeft geen behandelconsequenties.
Lichamelijk onderzoek
Naar Samenvatting ›- Laat de patiënt de aangedane vinger volledig flecteren en daarna extenderen om het blokkeren van de triggervinger uit te lokken.
- Laat eventueel een krachtige vuist maken; soms is een krachtige aanspanning nodig.
- Bepaal de ernst van de functionele beperking (verstoorde beweging, blokkade of gefixeerd).
- Palpeer de flexorpees (in de handpalm bij de duim of net proximaal van het MCP-gewricht) en let op een zwelling die eventueel drukpijnlijk is en met de beweging van de flexorpezen meebeweegt.
- Stel vast of er voelbare of pijnlijke zwelling is ter plaatse van de flexorpees.
Evaluatie
Naar Samenvatting ›Stel de diagnose ‘triggervinger’ of ‘triggerduim’ op basis van een vervelend of pijnlijk gevoel aan de palmaire zijde van de basis van vinger of duim, en het moeilijker of schokkend buigen of strekken van de vinger of duim, al dan niet met een (op te heffen) blokkade in de beweging.
Diagnostiek bij contractuur van Dupuytren
Naar Samenvatting ›Stel de diagnose ‘contractuur van Dupuytren’ aan de hand van klinisch onderzoek.
Anamnese
Naar Samenvatting ›- Vraag naar:
- langzaam progressieve streng- en nodusvorming in de handpalm met een flexiecontractuur van de vingers
- vóórkomen van de aandoening in de familie
- handtrauma of handoperatie, ziekte van Ledderhose of ziekte van Peyronie in de voorgeschiedenis
- Let op:
- snelle progressie van een flexiecontractuur
- pijnklachten in de hand of vingers
- de ernst van de beperkingen
De diagnose ‘contractuur van Dupuytren’ is goed te stellen aan de hand van klinisch onderzoek. Het betreft een doorgaans langzaam progressieve contractuur van de palmaire aponeurosis. Meestal begint de aandoening in de pink en ringvinger waarbij de vingers in een permanente flexiestand terechtkomen. De anamnese richt zich op het vaststellen van de functionele beperkingen in de hand en van eventuele verwijsindicaties (pijnklachten, snelle progressie, ernstige functionele beperkingen) (zie Evaluatie).
Lichamelijk onderzoek
Naar Samenvatting ›- Maak een inschatting van de ernst van de klachten.
- Inspecteer en palpeer de palmaire zijde van de vingers (vooral de vierde en vijfde straal) en de handpalm (soms begint de aandoening alleen in de vingers). Let daarbij op:
- kenmerkende noduli en pijnklachten
- huidintrekkingen in de handpalm
- Bepaal de mate van flexiecontractuurvorming ter hoogte van het MCP- en het PIP-gewricht. Gebruik hiervoor bijvoorbeeld de table top test van Hueston, waarbij de mate van beperking in het plat op de tafel kunnen leggen van de hand overeen komt met de ernst van de flexiecontractuur in de MCP-gewrichten.
Stadiëring
Er zijn meerdere graderingssystemen. De toepasbaarheid in de huisartsenpraktijk is echter beperkt bij gebrek aan klinische consequenties.
Table top test
Als alternatief kan de table top test van Hueston een praktische indicatie geven van de ernst van de flexiecontractuur.
De mate waarin uitvoering van de test niet mogelijk is, geeft een indicatie van de ernst van de contractuur. Voor de behandeling zijn de functionele beperkingen echter leidend.
Bij de table top test wordt de patiënt gevraagd om de hand plat op de tafel te leggen. Een contractuur in een MCP-gewricht leidt ertoe dat de metacarpalia het tafelblad niet meer kunnen raken. In deze houding is de mate van de flexiecontractuur ook gemakkelijker in te schatten dan wanneer de patiënt de handpalm laat zien aan de onderzoeker.
Evaluatie
Naar Samenvatting ›- Stel de diagnose ‘contractuur van Dupuytren’ bij vast-elastische, soms pijnlijke knobbels in de handpalm en vingers (vooral pink en ringvinger), die zich kunnen ontwikkelen tot strengen van fibrotisch weefsel.
- Differentiaaldiagnose:
- posttraumatische contractuur (niet redresseerbare flexiestand van de vinger)
- triggervinger (doorgaans redresseerbaar).
Diagnostiek bij tendovaginitis van De Quervain
Naar Samenvatting ›Anamnese
Naar Samenvatting ›Vraag naar:
- lokalisatie van de pijn: de patiënt wijst met 1 vinger de pijn aan, doorgaans ter hoogte van de processus styloideus radii, soms met uitstraling naar de duim of naar de onderarm.
- ernst van de pijn
- uitlokkende factoren, zoals bepaalde bewegingen.
- (beroeps)activiteiten waarbij de pols veelvuldig in geforceerde flexie wordt gebracht (veel schrijven, kapsters)
Lichamelijk onderzoek
Naar Samenvatting ›- Onderzoek:
- zwelling of crepitaties over het eerste dorsale compartiment radiaal
- drukpijn op de radiale zijde van de pols en de betreffende pezen
- Doorgaans zijn er geen beperkingen in de beweging te verwachten, wel kan pijn het bewegen bemoeilijken.
Weerstandstests
Naar Samenvatting ›- Overweeg, als toevoeging aan het lichamelijk onderzoek (een combinatie van) weerstandstests zoals de test van Eichhoff, de test van Finkelstein en/of wrist hyperflexion and abduction of the thumb (WHAT-test).
- Laat de tests eerst door de patiënt zelf uitvoeren in verband met pijnklachten bij een geforceerde beweging door de onderzoeker.
- Een negatieve test sluit een tendovaginitis van De Quervain goed uit.
Een systematische zoekopdracht naar de accuraatheid van weerstandstests voor De Quervain leverde 2 bruikbare resultaten op met betrekking tot 3 verschillende tests: de test van Eichhoff, de test van Finkelstein en wrist hyperflexion and abduction of the thumb (WHAT-test).
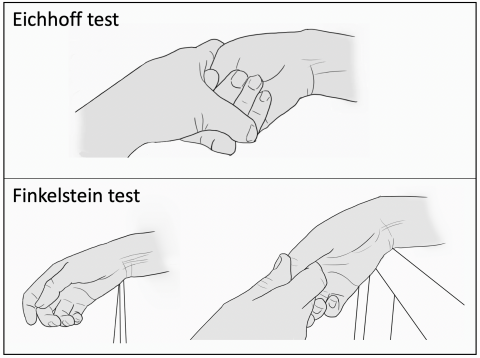
- In de literatuur en in de praktijk bestaat een wijdverbreid misverstand rond de nomenclatuur van de meest voorkomende test voor De Quervain.
Doorgaans wordt namelijk met de test van Finkelstein in werkelijkheid de test van Eichhoff bedoeld.
- Bij de test van Eichhoff sluit de patiënt de duim in een vuist en buigt de onderzoeker vervolgens de vuist in ulnairdeviatie.
- Bij de test van Finkelstein legt de patiënt de onderarm op de tafel met de hand over de rand in ulnairdeviatie met lengtetractie. De onderzoeker flecteert vervolgens de duim in de handpalm.
- Een positieve test geeft een toename van herkenbare pijnklachten door passieve rek van de betrokken pezen in het eerste extensorcompartiment (m. abductor pollicis longus en m. extensor pollicis brevis). Dit is tegelijkertijd het kritiekpunt van deze tests, omdat er een substantiële kans zou zijn op fout-positieve resultaten.
- Wu et al. onderzocht het aantal foutpositieven bij 36 asymptomatische patiënten zonder afwijkingen op echografie (72 polsen). De test van Finkelstein lijkt een betere sensitiviteit te hebben dan die van Eichhoff (100 versus 89%).
WHAT-provocatietest
Bij de WHAT-test wordt de pols in diepe palmaire flexie gebracht met een volledig gestrekte duim. Indien vervolgens de klachten toenemen bij abductie van de duim tegen weerstand is de test positief.
Hierbij worden de pezen van het eerste extensorcompartiment actief gebruikt en tegen hun pulley gedrukt. Dit geeft verergering van herkenbare pijnklachten.
De WHAT-test is vergeleken met de test van Eichhoff bij 100 patiënten met een klinische vermoeden van De Quervain (pijnklachten aan de radiale zijde van de pols). De patiënten die positief testten aan 1 of beide polsen werden onderzocht met echografie. De sensitiviteit van de WHAT-test lijkt beter dan die van de test van Eichhoff (99 versus 89%), maar er werden geen uitspraken gedaan over de significantie van deze resultaten. Een negatieve Eichhoff of WHAT-test sluit een tendovaginitis van De Quervain goed uit. De lage specificiteit van beide tests (14% voor de Eichhoff, 29% voor de WHAT-test) maakt echter het aantonen van een tendovaginitis van De Quervain niet goed mogelijk door de vele foutpositieve uitslagen.
Conclusie
Er is te weinig bewijs om een aanbeveling te doen over de waarde van weerstandstests bij het aantonen van De Quervain. De tests hebben een lage specificiteit en geven daardoor een hoog aantal foutpositieven. Een negatieve test lijkt echter een tendovaginitis van De Quervain wel goed uit te sluiten.
Evaluatie
Naar Samenvatting ›- Overweeg de diagnose ‘tendovaginitis van De Quervain’ indien er sprake is van pijn aan de radiale zijde van de pols, eventueel met als begeleidende symptomen zwelling van het eerste dorsale compartiment of ≥ 1 positieve weerstandstest.
- Differentiaaldiagnose:
- radiocarpale, CMC1- of STT-artrose (zie Handartrose)
- compressiesyndromen (zie figuur 3)
- denk bij de jongere patiënten met langer bestaande klachten en een (mild) trauma in de voorgeschiedenis aan andere posttraumatische oorzaken (zie Evaluatie traumatische klachten en Meer aspecifieke midcarpale hand- en polsklachten).
Diagnostiek bij traumatische klachten
Naar Samenvatting ›- Ga bij acuut ontstane klachten na een recent trauma gestructureerd na of er sprake kan zijn van pathologie die directe behandeling en/of verwijzing behoeft.
- Gebruik hierbij zo nodig de Handletselkaart.
Anamnese
Naar Samenvatting ›Vraag naar:
- traumamechanisme
- tijdstip van het trauma
- lokalisatie van de klachten
- dominante of niet-dominante hand
- beroep en hobby’s
Lichamelijk onderzoek
Naar Samenvatting ›- Zwelling, hematoom of wonden
- Standafwijking (deviatie, zwanenhals- of boutonnièredeformiteit) of rotatieafwijking (afwijkende arcade en rotatie van de vingers, zie Handletselkaart)
- Motoriek van vingers en pols (actieve en passieve functie, zie Handletselkaart)
- Sensibiliteit in de vingers
- Vascularisatie (pulsaties a. radialis en a. ulnaris, capillary refill)
- Vergelijk met de niet-aangedane zijde
Aanvullend onderzoek
Naar Samenvatting ›- Laat röntgenfoto’s maken bij vermoeden van ossaal letsel
- Vraag geen aanvullend onderzoek aan bij vermoeden van pees- of zenuwletsel, maar verwijs naar de trauma-, plastisch of orthopedisch chirurg (zie Beleid bij traumatische klachten).
Evaluatie traumatische klachten
Naar Samenvatting ›- Bij bepaalde acuut traumatische letsels is het van belang de behandeling direct te starten of hiervoor te verwijzen (zie tabel 2).
- Overweeg consultatie of verwijzing als een vermoeden van pees- of zenuwletsel in de acute situatie niet goed te beoordelen is.
- Wees bij persisterende posttraumatische klachten bedacht op oorzaken waarbij tijdige onderkenning een verschil kan maken in het beloop. Voorbeelden zijn letsel van het ligamentum scapholunatum, carpale instabiliteit of een (oude) scafoïdfractuur (zie Meer aspecifieke midcarpale hand- en polsklachten). Deze aandoeningen kunnen uiteindelijk leiden tot uitgebreide posttraumatische schade
| Lokalisatie | Aandoening | Belangrijkste symptomen |
|---|---|---|
| Acute klachten | ||
| Tabatière anatomique (anatomische snuifdoos) | Scafoïdfractuur |
|
| MCP-1 | Skiduim (letsel aan de ulnaire collaterale band) |
|
| Vingers | Malletvinger (letsel aan de extensorpees van de distale falanx) |
|
| Vingers | Jersey finger (letsel aan de flexorpees van de distale falanx) |
|
| Persisterende posttraumatische klachten (zie Meer aspecifieke midcarpale hand- en polsklachten) | ||
| Pols | Carpale instabiliteit (letsel van het SL-ligament) |
|
| Tabatière anatomique (anatomische snuifdoos) | (Oude) scafoïdfractuur |
|
Jersey finger
- Avulsiefractuur van de diepe flexorpees aan de basis van de distale falanx, doorgaans van de ringvinger, met onvermogen tot actieve flexie van het DIP-gewricht.
- Het letsel ontstaat vaak na geforceerde extensie van een geflecteerde vinger (grijpen van shirt bij wegrennende tegenspeler).
- Het missen van een jersey finger kan behandeling onmogelijk maken omdat niet alleen de pees terugtrekt, maar ook de peeskoker collabeert en verlittekent.
Skiduim (UCL-letsel)
- Ruptuur van het ulnaire collaterale ligament (UCL) na een (sub)luxatie in het MCP1-gewricht.
- Er wordt onderscheid gemaakt tussen ligamentair UCL-letsel en UCL-letsel met een avulsiefractuur van de proximale falanx (stenerlaesie) dan wel de volaire plaat.
- De behandeling wordt bepaald door de mate van instabiliteit en de aan- of afwezigheid van een stenerlaesie.
Diagnostiek bij malletvinger
Naar Samenvatting ›Anamnese
Naar Samenvatting ›Vraag specifiek naar:
- aanleiding en aard van het trauma (sport, blijven haken met de vinger, bed opmaken); het initiële trauma is in de regel niet pijnlijk; de pijnklachten ontstaan meestal daarna.
- tijdstip van ontstaan
- handdominantie en dagelijkse activiteiten met de handen
Lichamelijk onderzoek
Naar Samenvatting ›- Let op de combinatie van:
- permanente flexiestand van het DIP-gewricht en
- onvermogen tot actieve extensie van de distale falanx
- Soms ontstaat een zwanenhalsdeformatie (met hyperextensie van het PIP-gewricht) of is er sprake van lokale zwelling.
Aanvullend onderzoek
Naar Samenvatting ›Vraag (uitgesteld) röntgenonderzoek aan om onderscheid te maken tussen:
- tendinogene malletvinger of ossale malletvinger met kleine avulsiefractuur
- ossale malletvinger met avulsiefractuur > 30% van het gewrichtsoppervlak van het DIP-gewricht
Evaluatie
Naar Samenvatting ›- Stel de diagnose ‘malletvinger’ bij een acuut ontstane flexiestand van het DIP-gewricht met onvermogen tot actieve extensie van de distale falanx.
- Maak met röntgenonderzoek onderscheid tussen een conservatief behandelbare malletvinger (tendinogeen of ossaal met avulsiefragment <30%) en een malletvinger met een mogelijke operatie-indicatie (ossaal met avulsiefragment >30%).
Richtlijnen beleid
Naar Samenvatting ›Beleid bij carpaletunnelsyndroom
Naar Samenvatting ›Voorlichting en adviezen
Naar Samenvatting ›- Leg uit:
- verhoogde druk in de carpale tunnel zorgt voor compressie van de zenuw, die hierdoor tintelingen en pijn geeft in de hand. Langdurige druk kan schade veroorzaken aan de zenuw met toename van klachten en krachtsvermindering tot gevolg.
- tot 50% van de patiënten met CTS ervaart spontane verbetering binnen 1 jaar; bij 25% nemen de klachten toe.
- de klachten kunnen langere tijd aanhouden ondanks behandeling.
- Bespreek de mogelijkheden tot aanpassing van de dagelijkse werkzaamheden
- Benadruk dat het belangrijk is de hand en pols binnen de pijngrenzen te blijven gebruiken om onnodige stijfheid te voorkomen
- Geef (slaap)houdingsadviezen ter voorkoming van langdurige polsflexie en volaire druk op de pols
Thuisarts
Naar Samenvatting ›Verwijs naar de informatie op thuisarts.nl. De informatie op Thuisarts is gebaseerd op deze NHG-Standaard.
Gezamenlijke besluitvorming
Naar Samenvatting ›- Er zijn diverse acceptabele niet-operatieve en operatieve opties voor de behandeling van ‘klassiek’ of met aanvullend onderzoek bewezen CTS. Dit zijn:
- een afwachtend beleid met voorlichting en adviezen
- een (nacht)spalk
- een corticosteroïdinjectie
- een operatie (CTS-release)
- Er zijn echter duidelijke verschillen in invasiviteit en voor- en nadelen. Hierdoor spelen bij de behandelkeuze de waarden en voorkeuren van de patiënt een belangrijke rol.
- Bespreek de voor- en nadelen van de behandelopties en kom tot gezamenlijke besluitvorming.
- Gebruik eventueel de Keuzekaart Carpaletunnelsyndroom, deze geeft een samenvatting van de interventies en de voor- en nadelen. Let op: deze keuzekaart (2017) wordt binnenkort gereviseerd; de genoemde effectiviteitspercentages kunnen iets verschillen van de Standaard.
- Maak een keuze op basis van gezamenlijke besluitvorming met aandacht voor:
- persoonlijke voorkeuren van de patiënt
- voor- en nadelen behandelingen
- ervaring van de huisarts met infiltraties van de carpale tunnel
CTS in de zwangerschap
Naar Samenvatting ›- Bij zwangerschap zijn prognose en beleid niet anders dan buiten de zwangerschap. Wel valt na de bevalling (en borstvoeding) een oorzakelijke factor weg; dit kan meespelen in het afwegen van de verschillende behandelopties.
- Indien gekozen wordt voor een corticosteroïdbehandeling tijdens de zwangerschap of borstvoeding, doe dit eenmalig en in lage dosering.
Afwachtend beleid
Naar Samenvatting ›- Kies eerst voor een periode van afwachten als de pijnklachten en/of beperkingen mild tot matig zijn en niet langer dan enkele weken bestaan; bij ongeveer 25% van de patiënten treedt spontane verbetering op binnen 4 weken.
- Bespreek de kans op spontane verbetering
- Bespreek de onzekere effectiviteit van niet-operatieve behandelopties
Pijnstilling
Naar Samenvatting ›- Adviseer zo nodig pijnmedicatie conform het beleid bij acute nociceptieve pijn in de NHG-Standaard Pijn (paracetamol en/of een (dermaal) NSAID).
Spalkbehandeling of corticosteroïdinjectie
Naar Samenvatting ›Een (nacht-)spalkbehandeling of een corticosteroïdinjectie lijken gelijkwaardige opties voor matige tot ernstige CTS-klachten.
- De effectiviteit van beide behandelingen lijkt na 6 weken gelijk.
- Bespreek de voor- en nadelen van de behandelopties en kom tot gezamenlijke besluitvorming.
De effectiviteit van een spalkbehandeling en een corticosteroïdinjectie lijkt na 6 weken gelijk. De werkgroep adviseert daarom een keuze te maken op basis van gezamenlijke besluitvorming (shared decision making), met aandacht voor:
- persoonlijke voorkeuren van de patiënt
- voor- en nadelen van beide behandelingen
- ervaring van de huisarts met injecties in de carpale tunnel
Voor- en nadelen
Er is geen belangrijk verschil tussen beide behandelingen in effect op de subjectieve verbetering, ernst van de CTS-klachten, pijn, handfunctie of kans op recidief. De kans op bijwerkingen is klein bij beide behandelingen.
Kwaliteit van bewijs
De kwaliteit van het bewijs is redelijk tot laag. Er is afgewaardeerd in verband met risico op onnauwkeurigheid (bewijs gebaseerd op 1 onderzoek) en afwezigheid van blindering van patiënten.
Waarden en voorkeuren
De werkgroep verwacht substantiële variatie in hoe patiënten de voor- en nadelen van beide behandelingen afwegen. Mogelijk is er een lichte voorkeur bij patiënten voor een injectie in vergelijking met een spalk (25% vs. 13% van 234 patiënten; de overgebleven patienten hadden geen duidelijke voorkeur).
Middelen
De kosten van een corticosteroïdinjectie zijn circa € 2-8 per injectie, afhankelijk van het gebruikte corticosteroïd (medicijnkosten.nl, geraadpleegd 10 januari 2021). De kosten van een spalk (enkele tientallen euro's) zijn hoger, zeker in het geval van een handgemaakte brace. Daarbij komen de kosten van een spalk doorgaans voor rekening van de patiënt.
Gelijkheid
Beide alternatieven zijn beschikbaar voor alle patiënten in de eerste lijn. Er is een kleine kans dat de eigen kosten van een spalk patiënten ervan zouden kunnen weerhouden deze behandeloptie te kiezen.
Aanvaardbaarheid
- Patiënten kunnen een spalk als oncomfortabel ervaren. In dat geval kan eventueel nog overgegaan worden op een handgemaakte spalk. Voor sommige patiënten (die bijvoorbeeld werken met vloeistoffen) kan een spalk geen goede optie zijn, omdat deze niet gedragen zou kunnen worden tijdens de belastende activiteiten.
- Voor corticosteroïdinjecties geldt dat er ook patiënten zijn die een duidelijke voorkeur hebben voor (of weerstand tegen) een injectie.
- De werkgroep schat daarom in dat de voorkeur voor een behandeloptie voor patiënten afhankelijk is van de persoonlijke voorkeuren en omstandigheden van een patiënt.
Haalbaarheid
Beide interventies zijn reeds beschikbaar in de huidige praktijk. Eventueel zal verwezen moeten worden voor het aanmeten van een spalk, of het verrichten van de injectie indien de huisarts zich hiertoe niet bekwaam acht.
Uitgangsvraag
Is een spalkbehandeling (vergeleken met een corticosteroïdinjectie) aan te bevelen bij de behandeling van patiënten met mild of matig CTS?
| Patiënten | Patiënten met milde/matige klachten van carpaletunnelsyndroom |
|---|---|
| Interventie | Spalkbehandeling |
| Vergelijking | Corticosteroïdinjectie |
| Uitkomstmaten |
Ernst klachten |
Achtergrond
De effectiviteit van veelgebruikte niet-medicamenteuze behandelingen voor het CTS is onduidelijk.
Methode
Er is een systematische literatuurzoekactie naar SR’s en RCT’s uitgevoerd in PubMed en Embase in januari 2020.
Resultaten
Resultaat zoekactie
De zoekactie leverde 2 systematische literatuuronderzoeken naar de effectiviteit van spalkbehandeling vergeleken met corticosteroïdinjecties op. De cochranereview van Page voldeed aan de AMSTAR-criteria en werd als uitgangspunt genomen. Een aanvullende search na de zoekdatum van dit literatuuronderzoek leverde 2 aanvullende RCT’s op.
Onderzoekskarakteristieken
Page includeerde 19 RCT’s met in totaal 1190 deelnemers met CTS, waarvan 12 onderzoeken spalkbehandeling vergeleken met een andere niet-chirurgische interventie.
In slechts 1 RCT (n = 23) werd de effectiviteit van spalkbehandeling plus NSAID’s vergeleken met corticosteroïdinjecties. De gemiddelde leeftijd van de deelnemers was 48 jaar en de meerderheid was vrouw (96%). De follow-upduur was 8 weken.
De 2 aanvullende RCT’s vergeleken spalkbehandeling ten opzichte van corticosteroïdinjecties.
So keek bij 50 patiënten in de tweede lijn naar verbetering van de score op de Boston Carpal Tunnel Questionnaire (BCTQ) na 4 weken. De gemiddelde leeftijd van de deelnemers was 57 jaar en 86% was vrouw.
Chesterton onderzocht de verbetering van de score op de BCTQ bij 234 patiënten met een mild of matig CTS in de eerste lijn in Engeland. De gemiddelde leeftijd van de deelnemers was 52 jaar en 66% was vrouw. De deelnemers werden 24 maanden gevolgd; alleen de kortetermijnresultaten (6 maanden) zijn gepubliceerd.
Effectiviteit en bijwerkingen
Bekijk de tabel voor de samenvatting van de resultaten. De Boston Carpal Tunnel Questionnaire (BCTQ) geeft inzicht in de klachten en de ernst van de klachten bij het uitvoeren van specifieke handelingen. De BCTQ bestaat uit 2 delen:
- de Symptom Severity Scale (SSS), 11 items betreffende de ernst van de klachten;
- de Functional Status Scale (FSS), 8 items over de belemmering in uitvoering van specifieke activiteiten.
Beide onderdelen van de BCTQ hebben een bereik van 0-5. Een afname van de baseline BCTQ-SSS met minimaal 46% en een afname van de baseline BCTQ-FSS met minimaal 28% worden klinisch relevant beschouwd.
Bij pijn wordt gebruik gemaakt van een Numerical Rating Scale (NRS) op een schaal van 0 tot 10, waarbij 0 geen pijn impliceert en 10 de ergst denkbare pijn. Een afname van 2 punten wordt klinisch relevant beschouwd. Verwijzing voor chirurgie gebruiken we als proxy voor recidief klachten.
We presenteren alleen de resultaten van Chesterton, de RCT in de eerste lijn. Echter, de resultaten zijn in lijn met de resultaten van de 2 klein onderzoeken in de tweede lijn (totaal 73 patiënten) met korte follow-up (4-8 weken); zij laten ook geen klinisch relevante verschillen laten zien in BCTQ-SSS, BCTQ-FSS, pijn (VAS).
Conclusie
- Er is waarschijnlijk niet of nauwelijks verschil in pijn tussen patiënten met spalkbehandeling of corticosteroïdinjecties op korte termijn (6 weken) (kwaliteit van bewijs redelijk) en middellange termijn (6 maanden) (kwaliteit van bewijs laag).
- Er is waarschijnlijk niet of nauwelijks verschil in BCTQ-score (handfunctie en ernst symptomen) tussen patiënten met spalkbehandeling of corticosteroïdinjecties op korte termijn (6 weken) (kwaliteit van bewijs redelijk) en middellange termijn (6 maanden) (kwaliteit van bewijs laag).
- Er is mogelijk niet of nauwelijks verschil in aantal verwijzingen voor chirurgie tussen spalkbehandeling en corticosteroïdinjecties (kwaliteit van bewijs laag).
- Er traden geen ernstige onverwachte bijwerkingen op. Er is waarschijnlijk niet of nauwelijks verschil in bijwerkingen bij spalkbehandeling of corticosteroïdinjecties (kwaliteit van bewijs redelijk).
- Er is niet gerapporteerd over de uitkomst van werkhervatting.
Spalkbehandeling
Naar Samenvatting ›Overweeg een spalkbehandeling voor patiënten met matige tot ernstige pijnklachten en/of beperkingen van CTS die hiervoor gemotiveerd zijn, vooral in de volgende situaties:
- zwangerschap
- ter overbrugging in afwachting van een geplande operatie
- bij een patiënt met een duidelijke voorkeur voor niet-invasief beleid
Bespreek de voor- en nadelen:
- het bewijs voor de effectiviteit is zeer onzeker; op de korte termijn (4 weken) geeft een spalk mogelijk klachtenvermindering, maar op langere termijn (> 6 maanden) is de werkzaamheid onduidelijk
- een spalk moet aangeschaft of aangemeten worden, of de kosten vergoed worden is afhankelijk van de zorgverzekering die de patiënt heeft
- het dragen van de spalk kan zorgen voor ongemak (moeite met in slaap vallen, tintelingen bij het afdoen in de ochtend), maar slechts bij een zeer klein percentage maakt dit het dragen onmogelijk
- de recidiefkans is ongeveer 5% binnen 7-36 maanden na het stoppen met de spalk.
Adviseer de spalk in ieder geval ’s nachts te dragen en zo mogelijk ook overdag bij activiteiten die de klachten verergeren (zie Praktische aanwijzingen orthesen bij hand- en polsklachten)
De kwaliteit van het bewijs voor de vergelijking tussen spalkbehandeling en afwachtend beleid is zeer laag. Daarnaast kunnen de klachten ook spontaan (zonder behandeling) verbeteren. Indirect is er echter wel bewijs van betere kwaliteit dat spalkbehandeling en een corticosteroïdinjectie vergelijkbare effectiviteit hebben (zie Spalkbehandeling of corticosteroïdinjectie). Hiermee lijkt het waarschijnlijker dat de voordelen van een spalk opwegen tegen de nadelen. Daarom geven we een zwakke aanbeveling voor het gebruik van een spalk, waarbij het advies is de onzekerheid in bewijs met de patiënt te bespreken.
Voor- en nadelen
Er is te veel onzekerheid in het bewijs over de voor- en nadelen om te bepalen of de voordelen opwegen tegen de nadelen van een spalk. Mogelijk is er een verbetering van het door de patiënt ervaren herstel en de ernst van de CTS-klachten na 4 en 12 weken. Dit voordeel lijkt na 6 maanden niet meer te bestaan. Er is ook veel onzekerheid in het bewijs voor aanvullende ergotherapie en zelfmanagementadviezen bij spalkbehandeling.
Kwaliteit van bewijs
Er was zeer veel onzekerheid (de kwaliteit van het bewijs was zeer laag). Er werd onder andere afgewaardeerd voor risico op vertekening en onnauwkeurigheid van de effecten.
Waarden en voorkeuren
De werkgroep schat in dat er variatie bestaat in hoe patiënten de mogelijke voor- en nadelen van een spalk afwegen. Hierbij speelt naast door individuele voorkeuren ook mee dat de oorzaak van de klachten verschilt tussen patiënten (bijvoorbeeld zwangerschap).
Middelen
De kosten van een spalk zijn enkele tientallen euro's, een handgemaakte brace is duurder. De kosten van een spalk komen doorgaans voor rekening van de patiënt.
Aanvaardbaarheid
Voor een minderheid van de patiënten zal een spalk minder aanvaardbaar zijn. Sommige patiënten zullen een spalk oncomfortabel vinden maar het percentage waarbij het dragen hierdoor onmogelijk wordt is klein. Een handgemaakte spalk kan een comfortabeler alternatief zijn. Sommige patiënten vinden de kosten van een spalk niet aanvaardbaar.
Haalbaarheid
Beide behandelingen worden ingezet in de huidige praktijk en zijn haalbaar. Voor het eventueel aanmeten van een spalk is een verwijzing nodig.
Uitgangsvraag
Is een spalkbehandeling (vergeleken met een afwachtend beleid) aan te bevelen bij de behandeling van patiënten met mild of matig CTS?
| Patiënten | Patiënten met milde/matige klachten van carpaletunnelsyndroom |
|---|---|
| Interventie | Spalkbehandeling |
| Vergelijking | Afwachtend beleid |
| Uitkomstmaten |
Ervaren verbetering |
Achtergrond
De effectiviteit van veelgebruikte niet-medicamenteuze behandelingen voor CTS is onduidelijk.
Methode
Er is een systematische literatuurzoekactie naar SR’s en RCT’s uitgevoerd in PubMed en Embase in maart 2020.
Resultaten
Resultaat zoekactie
De zoekactie leverde 3 systematische literatuuronderzoeken op waarin de effectiviteit van spalkbehandeling vergeleken werd met corticosteroïdinjecties. De cochranereview van Page (2012) voldeed aan de AMSTAR-criteria en werd als uitgangspunt genomen. Jiménez Del Barrio vermeldde geen zoekstrategie en geen duidelijke in- of exclusiecriteria. Een aanvullende search na de zoekdatum van dit literatuuronderzoek leverde geen aanvullende RCT’s op.
Onderzoekskarakteristieken
Page includeerde 2 RCT’s waarin spalkbehandeling werd vergeleken met geen behandeling bij patiënten met milde tot matig ernstige CTS-klachten. In deze RCT’s werden de klachten gedefinieerd als passend bij CTS (tintelingen, doofheid, hyp-of paresthesie in het verzorgingsgebied van de n. medianus, positieve test van Phalen, hypesthesie, thenaratrofie) met ≥ 1 afwijkend EMG. De intensiteit van de klachten werd niet beschreven. Er zijn geen onderzoeken gevonden bij patiënten met ernstige CTS-klachten. Manente (n = 83) vergeleek een spalk die 4 weken 's nachts werd gedragen met geen behandeling. Premoselli (n = 50) deed een quasi-gerandomiseerd onderzoek waarin een nachtspalk gedurende 6 maanden werd vergeleken met geen behandeling. Manente rapporteerde resultaten na 4 weken, Premoselli na 3 en na 6 maanden. De gemiddelde leeftijd van de deelnemers was 48-50 jaar en 86-90% was vrouw. In de cochranereview is ervoor gekozen om gegevens niet te combineren vanwege het hoge risico op bias in beide onderzoeken.
Effectiviteit en bijwerkingen
Bekijk de tabel voor de samenvatting van de resultaten. De door patiënten ervaren verbetering is gemeten met de Patient’s Global Impression of Change Questionnaire (4 categorieën, gedichotomiseerd in ‘weinig tot veel verbetering’ versus ‘geen verbetering tot verslechtering’). Een toename van > 25% van het aantal patiënten dat verbetering ervaart, wordt als klinisch relevant beschouwd.
De BCTQ bestaat uit 2 delen:
- de Symptom Severity Scale (SSS), 11 items betreffende de ernst van de klachten;
- de Functional Status Scale (FSS), 8 items over de belemmering in uitvoering van specifieke activiteiten.
Beide onderdelen van de BCTQ hebben een bereik van 0-5. Een afname van de baseline BCTQ-SSS met minimaal 46% en een afname van de baseline BCTQ-FSS met minimaal 28% worden klinisch relevant beschouwd.
Recidiefkans
In de geïncludeerde onderzoeken werden geen uitspraken gedaan over de kans op recidief na het stoppen van de spalkbehandeling. Er zijn wel aanwijzingen dat in een klein percentage van de patiënten de klachten recidiveren (5% na 7-36 maanden).
Conclusie
- We zijn onzeker of een spalkbehandeling een subjectieve verbetering van CTS-symptomen geeft (kwaliteit van bewijs zeer laag).
- We zijn onzeker of een spalkbehandeling de ernst van de klachten (pijn, doof gevoel, tintelingen) vermindert (kwaliteit van bewijs zeer laag).
- We zijn onzeker of een spalkbehandeling de handfunctie verbetert (kwaliteit van bewijs zeer laag).
- We zijn onzeker of het dragen van een spalk meer ongemak geeft (kwaliteit van bewijs zeer laag).
- Er is niet gerapporteerd over de uitkomsten recidief en werkhervatting.
- De onderzoeken naar verschillende typen spalken zijn zeer heterogeen. Hierdoor is het op basis van deze literatuur niet mogelijk om een duidelijke uitspraak te doen met betrekking tot het soort spalk.
- Er is ook onvoldoende bewijs met betrekking tot het effect van continu dragen dan wel alleen in de nacht dragen. Aangezien er geen duidelijk voordeel lijkt te zijn voor continu dragen lijkt het advies om de spalk ’s nachts te dragen afdoende. Eventueel kan de patiënt ervoor kiezen de spalk ook te dragen bij activiteiten die de klachten uitlokken (autorijden, werkzaamheden).
Corticosteroïdinjectie
Naar Samenvatting ›Overweeg een corticosteroïdinjectie voor patiënten met matige tot ernstige pijn en/of beperkingen bij CTS die hiervoor gemotiveerd zijn. Bespreek de voor- en nadelen:
- directe behandeling mogelijk tijdens het consult
- ten opzichte van placebo mogelijk meer patiëntgerapporteerde verbetering tot 6 weken na de injectie, zonder verschil in ernst van klachten en handfunctie.
- mogelijke bijwerkingen: veranderingen van de huid rondom de injectieplaats (3%), blozen (flushing, 15%), enkele dagen na de injectie toename van de pijnklachten (46%)
- mogelijke complicaties: injectie in de zenuw en lokale infectie zijn in theorie mogelijk, maar worden in de literatuur niet gemeld
- de recidiefkans na 1 injectie is ongeveer 40%, ongeveer 60% van deze patiënten heeft vervolgens baat bij een tweede injectie en uiteindelijk heeft ongeveer 23% van de patiënten toch een indicatie voor een CTS-operatie.
- de kans op recidief is groter bij vrouwen, diabetici en patiënten met EMG-afwijkingen.
Mogelijk geeft een corticosteroïdinjectie een ervaren verbetering van de klachten. Er zijn geen zwaarwegende nadelen van de behandeling. Het lijkt daarom redelijk om een injectie aan te bieden aan patiënten die gemotiveerd zijn voor deze optie, met name omdat het lijkt te gaan om patiëntgerapporteerde verbetering. De verschillen tussen een corticosteroïdinjectie en placebo op langere termijn zijn echter onzeker.
Voor- en nadelen
Patiënten lijken na een corticosteroïdinjectie kortdurend (1-8 weken) meer patiëntgerapporteerde verbetering van de CTS-klachten te ervaren dan na een injectie met placebo. Er is geen verschil in ernst van de klachten tussen de 2 groepen. De kans op bijwerkingen is klein.
Kwaliteit van bewijs
De kwaliteit van bewijs is redelijk tot zeer laag. Er is afgewaardeerd voor serieuze risico's op bias, onnauwkeurigheid en inconsistentie.
Waarden en voorkeuren
Het is de mening van de werkgroep dat er substantiele variatie bestaat tussen patiënten in hoe zij de voor- en nadelen afwegen.
Middelen
De kosten van een corticosteroïdinjectie zijn circa € 2-8 per injectie, afhankelijk van het gebruikte corticosteroïd (medicijnkosten.nl, geraadpleegd 10 januari 2021).
Haalbaarheid
De behandeling wordt ingezet in de huidige praktijk en is haalbaar.
Uitgangsvraag
Is een corticosteroïdinjectie (vergeleken met placebo) aan te bevelen bij de behandeling van patiënten met mild of matig CTS?
| Patiënten | Patiënten met milde/matige klachten van carpaletunnelsyndroom (CTS) |
|---|---|
| Interventie | Corticosteroïdinjectie |
| Vergelijking | Placebo |
| Uitkomstmaten | Ernst CTS-klachten (pijn, doofheid, tintelingen) Handfunctie Recidief Bijwerkingen Werkhervattingen |
Achtergrond
De effectiviteit van veelgebruikte behandelingen voor het CTS is onduidelijk.
Methode
Er is een systematische literatuurzoekactie naar SR’s en RCT’s uitgevoerd in PubMed en Embase in april 2020.
Resultaten
Resultaat zoekactie
De zoekactie leverde 1 systematisch literatuuronderzoek op naar de effectiviteit van corticosteroïdinjecties vergeleken met placebo. Een aanvullende search na de zoekdatum van dit literatuuronderzoek leverde geen aanvullende RCT’s op.
Onderzoekskarakteristieken
Chen includeerde 6 RCT’s met in totaal 373 patiënten met CTS waarin de effectiviteit van corticosteroïdinjecties werd vergeleken met placebo (of geen injectie bij 1 onderzoek). De follow-upduur varieerde van 1 week tot 12 maanden. Gegevens van follow-upmomenten > 8 weken waren niet meegenomen in de meta-analyse. De gemiddelde leeftijd van de deelnemers was 47-57 jaar en 74-87% was vrouw.
Effectiviteit en bijwerkingen
Bekijk de tabel voor de samenvatting van de resultaten.
Voor behandelrespons wordt een toename van 25% van het aantal patiënten dat aangeeft tevreden te zijn met de behandeling als klinisch relevant beschouwd. De Boston Carpal Tunnel Questionnaire (BCTQ) geeft inzicht in de klachten en de ernst van de klachten bij het uitvoeren van specifieke handelingen.
De BCTQ bestaat uit 2 delen:
- de Symptom Severity Scale (SSS), 11 items betreffende de ernst van de klachten;
- de Functional Status Scale (FSS), 8 items over de belemmering in uitvoering van specifieke activiteiten.
Beide onderdelen van de BCTQ hebben een bereik van 0-5. Een afname van de baseline BCTQ-SSS met minimaal 46% en een afname van de baseline BCTQ-FSS met minimaal 28% worden klinisch relevant beschouwd.
Recidiefkans
In de geïncludeerde onderzoeken werden geen uitspraken gedaan over de kans op recidief na een corticosteroïdinjectie. Er was wel een prospectief observationeel onderzoek met 500 patiënten waarin dit werd beschreven. Bij circa 60% was 1 injectie afdoende. Wederom circa 60% had goed effect na 2 injecties; 23% van alle patiënten was pas symptoomvrij na een CTS-release. De kans op recidief lijkt groter bij vrouwen, diabetici en patiënten met EMG-afwijkingen.
Conclusie
- Corticosteroïdinjecties verhogen waarschijnlijk het percentage patiënten dat tevreden is met de behandeling op korte termijn (1-6 weken) (kwaliteit van bewijs redelijk).
- Er is mogelijk niet of nauwelijks verschil in ernst van de klachten (kwaliteit van bewijs laag).
- We zijn onzeker of een corticosteroïdinjectie de handfunctie verbetert (kwaliteit van bewijs zeer laag).
- Er treden mogelijk bijwerkingen van voorbijgaande aard op na corticosteroïdinjectie (kwaliteit van bewijs laag).
- Er is niet gerapporteerd over de uitkomsten ‘recidief’ en ‘werkhervatting’.
Praktische adviezen
Naar Samenvatting ›- Informeer de patiënt over de bijwerkingen, waaronder voorbijgaande lokale pijnklachten, flushing, pigmentatieveranderingen rond de injectieplaats, infectie en/of zenuwschade.
- Injecteer alleen bij voldoende bekwaamheid en kennis van de anatomie, techniek en potentiële risico’s van de betreffende injectie.
- Voorkom irreversibele subcutane atrofie en vermijd te sterke subcutane opzwelling en afzetting van het steroïd langs de naald:
- spuit niet te veel vloeistof in
- trek de naald niet al spuitend terug
- Let op dat de naald niet in de zenuw of de pezen wordt geplaatst.
Keuze van corticosteroïd voor injecties bij hand- en polsklachten
Naar Samenvatting ›- Gebruik als eerste keuze op basis van praktische overwegingen 10 mg triamcinolonacetonide 10 mg/ml (zie tabel 3).
- Gelijkwaardige alternatieven zijn:
- 2 mg dexamethason 4 mg/ml
- 20 mg methylprednisolon 40 mg/ml.
| Aandoening | Middelen en dosering (Beschikbare toediening) |
|---|---|
CTS De Quervain | Voorkeursmiddel:
Alternatieven:
|
| Triggervinger | Voorkeursmiddel:
Alternatieven:
|
- Informeer de patiënt over de bijwerkingen, waaronder voorbijgaande lokale pijnklachten, flushing, pigmentatieveranderingen rond de injectieplaats, infectie en/of zenuwschade.
- Injecteer alleen bij voldoende bekwaamheid en kennis van de anatomie, techniek en potentiële risico’s van de betreffende injectie.
- Voorkom irreversibele subcutane atrofie en vermijd te sterke subcutane opzwelling en afzetting van het steroïd langs de naald:
- spuit niet te veel vloeistof in
- trek de naald niet al spuitend terug
- Bij een injectie voor tendovaginitis is het van belang de injectie te plaatsen in de peesschede en niet in de pees, gezien het risico op peesrupturen bij herhaalde injecties in ontstoken pezen.
Inleiding
In deze standaard is een corticosteroïdinjectie een van de behandelopties voor CTS, triggervinger en tendovaginitis van De Quervain (zwakke aanbevelingen). Er is veel variatie met betrekking tot de gebruikte corticosteroïden in de praktijk en met name in de literatuur. In dit detail wordt de onderbouwing gegeven voor het advies over corticosteroïdkeuze bij deze aandoeningen.
CMC- I-artrose
Bij CMC- I-artrose wordt de voorkeur gegeven aan niet-invasieve conservatieve behandelingen boven een injectie. Deze indicatie wordt daarom buiten beschouwing gelaten voor dit detail. De conclusies worden wel overgenomen voor CMC- I-artrose, omdat er geen redenen bekend zijn waarom bij CMC- I-artrose een ander corticosteroïd zou moeten worden gekozen.
Inventarisatie van beschikbare middelen
De volgende systemische corticosteroïden zijn in Nederland beschikbaar voor intra-articulaire injectie of injectie in pezen: bètamethason, dexamethason, hydrocortison, methylprednisolon, prednisolon, triamcinolonacetonide en triamcinolonhexacetonide.
Gelijkwaardigheid
Om een uitspraak te doen over de gelijkwaardigheid van de overgebleven middelen (betamethason, dexamethason, hydrocortison, methylprednisolon, prednisolon, triamcinolonacetonide en triamcinolonhexacetonide) wordt gekeken naar effectiviteit, veiligheid, tolerantie en toepasbaarheid.
Effectiviteit
Er is gezocht naar vergelijkende onderzoeken bij de verschillende aandoeningen in deze standaard.
CTS
Een recente RCT (n = 80) vergelijkt triamcinolonacetonide 20 en 40 mg met methylprednisolon 20 en 40 mg bij patiënten met CTS. Alle groepen toonden mogelijk een klein voordeel op functionele uitkomsten na 3 maanden, met mogelijk een klein voordeel in de groep met triamcinolon 40 mg.
Om de dosering van verschillende middelen te vergelijken, kunnen deze worden afgezet tegen dosisequivalente eenheden op basis van de defined daily dose (DDD) voor parenteraal gebruikte corticosteroïden (tabel 4). We gaan ervan uit dat de parenterale dosisequivalentie ook geldt voor lokale injecties. In dit onderzoek ontving de triamcinolongroep dus een potentere (in dosisequivalentie circa 2,5 keer sterkere) dosering corticosteroïden. In de studie werden geen bijwerkingen gerapporteerd.
| Dexamethason | Methylprednisolon | Triamcinolon | Prednisolon | Hydrocortison |
|---|---|---|---|---|
| 1,5 mg | 20 mg | 7,5 mg | 10 mg | 30 mg |
| Bron: WHO ATC/DDD Index | ||||
Triggervinger
Een RCT (n = 84) vergeleek 1-1,5 ml injecties van 1 : 1 lidocaïne 1% met ófwel triamcinolonacetonide 10 mg/ml, ófwel dexamethason 4 mg/ml.
Op 3 maanden waren er geen verschillen in functie en tevredenheid.
Teruggerekend naar dosisequivalente eenheden op basis van de DDD voor parenteraal gebruikte corticosteroïden (tabel 4) was de dosering corticosteroïd in de dexamethasongroep 2 keer zo hoog als in de triamcinolongroep. Deze relatief hogere dosering had geen invloed op de effectiviteit of het optreden van bijwerkingen.
Tendovaginitis van De Quervain
Er zijn geen vergelijkende onderzoeken gevonden met betrekking tot de effectiviteit van verschillende corticosteroïden, doseringen of frequenties.
Veiligheid
De corticosteroïden verschillen onderling niet in de aard en frequentie van (ernstige) bijwerkingen. Er zijn geen ernstige bijwerkingen of interacties (met levensgevaar, invaliditeit, arbeidsongeschiktheid of opname in het ziekenhuis) gemeld voor de beschikbare middelen.
In de SmPC-tekst van dexamethason wordt vermeld dat bij een patiënt gedurende het gehele leven niet meer dan 5 injecties per gewricht moeten worden gegeven, dit in verband met het gevaar van aseptische botnecrose bij herhaalde injecties. Onduidelijk is waarom de registratieteksten van de verschillende injectiecorticosteroïden hierin onderling verschillen. Het voorbehoud is echter voor de meeste indicaties bij hand- en polsklachten niet relevant, omdat het daarbij niet gaat om intra-articulaire injecties.
Tolerantie
De corticosteroïden verschillen onderling niet ten aanzien van tolerantie. In de literatuur en de praktijk wordt ook voorbijgaand blozen in het gezicht (facial flushing) genoemd, maar dit komt niet terug in de Nederlandse geneesmiddelenregistratie. Toename van pijnklachten in de eerste dagen na de injectie is niet ongewoon.
Toepasbaarheid
De contra-indicaties van de verschillende corticosteroïden verschillen niet van elkaar:
- ulcus ventriculi of duodeni
- actieve infecties
- overgevoeligheid
- tropische worminfecties
- na vaccinatie met levend verzakt virus
- niet-stabiele gewrichten (in verband met mogelijke intra-articulaire beschadiging bij herhaalde injecties)
Conclusies inzake de gelijkwaardigheid van beschikbare corticosteroïden
Verschillen op basis van effectiviteit
Op basis van de gevonden onderzoeken waarin corticosteroïden onderling worden vergeleken zijn er tussen dexamethason, methylprednisolon en triamcinolonacetonide geen klinisch relevante verschillen in effectiviteit bij de aandoeningen in deze standaard.
Er werden geen vergelijkende onderzoeken gevonden over betamethason, hydrocortison, prednisolon en triamcinolonhexacetonide. Bij voldoende geregistreerde alternatieven vallen daarom deze middelen af in het advies.
Verschillen op basis van veiligheid en toepasbaarheid
Alle resterende beschikbare corticosteroïden zijn vergelijkbaar op het gebied van veiligheid en toepasbaarheid.
Verschillen op basis van werkingsduur
Het is onduidelijk of een langere halfwaardetijd ook een voordeel biedt voor de effectiviteit. In de praktijk wordt echter vaak wel geopteerd voor een middel met een langere werkingsduur. Mogelijk zorgt een lagere oplosbaarheid (triamcinolonacetonide) voor een langere werkingsduur ten opzichte van beter oplosbare middelen (dexamethason en methylprednisolon). De relatie tussen halfwaardetijd of oplosbaarheid met de duur van het klinische effect van een injectie is echter onvoldoende onderzocht. Er zijn daarom weinig gegronde argumenten voor een voorkeur op basis van werkingsduur. Dexamethason, methylprednisolon en triamcinolonacetonide worden gelijkwaardig geacht voor injectie in de hand en pols.
Dosering
Er zijn 3 RCT’s beschikbaar die verschillende doseringen vergelijken bij in totaal 285 patiënten met CTS-klachten. Alle 3 onderzoeken betreffen methylprednisolon, in doseringen van 12-80 mg. In geen van de onderzoeken lijkt er een duidelijk voordeel te zijn van een hoge dosering boven een lage dosering. Er zijn geen vergelijkende onderzoeken gevonden voor verschillende doseringen triamcinolonacetonide of dexamethason.
Wat verder opvalt is dat de meeste gerapporteerde doseringen hoger zijn dan de geregistreerde doseringen. Dit is ook het geval in de RCT’s die geïncludeerd zijn in de PICO’s van deze standaard; het lijkt bovendien te stroken met de klinische praktijk in de eerste en tweede lijn.
In tabel 5 is het bereik van de gerapporteerde doseringen uit bovengenoemde onderzoeken samengevat.
Geregistreerde dosering1 | Gerapporteerde doseringen in beschikbare onderzoeken | Aanbevolen dosering in de NHG-Standaard |
| Dexamethason 4 mg/ml (1 ml ampul) | ||
Pols- of ellebooggewricht: 0,8-4 mg
| Geen onderzoeken | CTS, tendovaginitis van De Quervain en epicondylitis: 2 mg |
Peesschede: 0,4-1 mg
| Triggervinger 4-6 mg | Triggervinger: 1 mg |
| Methylprednisolon 40 mg/ml (1 ml ampul) | ||
Pols- of ellebooggewricht: 10-40 mg
| CTS: 12-80 mg | CTS, tendovaginitis van De Quervain en epicondylitis: 20 mg |
| Peesschede, inclusief epicondylitis: 4-30 mg | Geen onderzoeken | Triggervinger: 10 mg |
| Triamcinolonacetonide 10 mg/ml (5 ml ampul); 40 mg/ml (1 ml ampul) | ||
Pols- of ellebooggewricht: 2,5-5 mg
| CTS: 20-40 mg
| CTS, tendovaginitis van De Quervain en epicondylitis: 10 mg
|
| Peesschede klein gewricht: 2,5-5 mg | Triggervinger: 10-15 mg | Triggervinger: 5 mg |
| 1 Bron: KNMP kennisbank/ SmPC (CBG) | ||
Voor het gebruiksgemak en de veiligheid bij de bereiding is besloten om 1 dosering per aandoening te adviseren in deze standaard. Hierbij is rekening gehouden met verschillende zaken:
- Er is gekozen voor een makkelijk af te lezen dosering voor de beschikbare concentraties.
- Aangezien in de beschreven onderzoeken geen voordeel van de hoge boven de lage dosering werd gerapporteerd, is in deze standaard waar mogelijk gekozen voor de lage dosering. Deze is vergeleken met de maximale geregistreerde dosering en overschrijdt deze niet.
Ampullen
De kleinste ampullen die op dit moment beschikbaar zijn in Nederland voor de benodigde doseringen zijn:
- Triamcinolonacetonide
- 10 mg/ml (5 ml ampul)
- 40 mg/ml (1 ml ampul)
- Methylprednisolon:
- 40 mg/ml (1 ml ampul)
- Dexamethason:
- 4 mg/ml (1 ml ampul)
Triamcinolonacetonide 40 mg/ml geeft in vergelijking met de 10 mg/ml een grotere kans op dosisafwijkingen vanwege de sterkere concentratie bij de lage doseringen. Daarmee is er ook een groter risico op overdosering en daarmee dosisgerelateerde bijwerkingen zoals lokale huidafwijkingen, of op onderdosering en daarmee op onvoldoende effectiviteit. De ampullen met een hogere concentratie hebben daarom niet de voorkeur.
Triamcinolonacetonide 10 mg/ml is alleen verkrijgbaar in een 5 ml ampul. De spillage is daardoor groter dan bij andere ampullen.
Kosten
Voor de kostenvergelijking van de gelijkwaardig geachte corticosteroïden wordt doorgaans gekeken naar het effect van dosisequivalente hoeveelheden (tabel 4). Voor alle indicaties wordt 1 ampul aangebroken, dus beoordelen we hier de kosten van 1 ampul. Deze zijn het laagst voor methylprednison 40 mg/ml 1 ml ampul (circa € 2,25) en het hoogst voor triamcinolonacetonide 10 mg/ml 5ml ampul (circa € 5 per stuk). Deze prijzen zijn exclusief afleverkosten (www.medicijnkosten.nl)
Overwegingen
Het lijkt in de praktijk een voordeel (vanwege voorraadbeheer en ervaring) om bij alle 3 de indicaties hetzelfde injectiecorticosteroïd te adviseren.
Om verwisselingen te voorkomen lijkt het ook een voordeel om aan te sluiten bij het geadviseerde injectiecorticosteroïd in NHG-Standaard Schouderklachten en NHG-Standaard Traumatische knieklachten. Daarom zou de voorkeur uitgaan naar triamcinolonacetonide. Dit is ook het middel dat in de meeste onderzoeken gebruikt wordt. Het gebruiksgemak en de uniformiteit voor in de praktijk wegen in dit geval op tegen het verschil in kosten.
Op dit moment is er, op basis van het beschikbare beperkte bewijs, geen aanwijzing voor superieure effectiviteit van een type of dosering corticosteroïd boven de beschikbare alternatieven. Er is om praktische overwegingen een lichte voorkeur voor triamcinolonacetonide 10 mg/ml, met als verder gelijkwaardige alternatieven dexamethason 4 mg/ml en methylprednisolon 40 mg/ml. Zie Tabel 3 voor de geadviseerde doseringen per aandoening.
CTS-operatie
Naar Samenvatting ›Overweeg verwijzing bij een mogelijke indicatie voor operatie. De indicaties hiervoor zijn:
- matige tot ernstige pijnklachten en/of beperkingen van CTS
- atrofie van de duimmuis en/of spierzwakte van de thenar
Toelichting
Bij een chirurgische CTS-release wordt het ligamentum carpi transversum over de carpale tunnel gekliefd. Dit is meestal een (minimaal invasieve) open procedure.
Voor- en nadelen
Voordelen:
- een open operatie lijkt op middellange termijn (6-26 weken) effectiever dan een corticosteroïdinjectie of spalk.
- op een langere termijn (> 1 jaar) is geen verschil aantoonbaar.
Nadelen:
- complicaties (onder andere infectie, bloeding, wondinfectie, CRPS, zenuwschade)
- bij ongeveer 5% van de geopereerde patiënten persisteren (een deel van) de klachten.
- (beperkt) behandeldelay door verwijzing en eventuele wachtlijst voor operatie (overweeg eventueel een spalk ter overbrugging).
Een (open) CTS-operatie lijkt effectiever dan een corticosteroïdinjectie op middellange termijn of een spalkbehandeling op de korte tot middellange termijn. Voor patiënten is er tussen de drie behandelingen echter een groot verschil in (ervaren) impact en ernst van de potentiële bijwerkingen. Tevens is een operatie een invasieve en duurdere behandeling. De werkgroep geeft daarom slechts een zwakke aanbeveling voor een operatie. Een getrapte behandeling heeft de voorkeur.
Voor- en nadelen
Open chirurgie heeft na 6 weken tot 6 maanden mogelijk een hoger succespercentage dan een spalkbehandeling (kwaliteit van bewijs laag). Er lijkt geen verschil te zijn in klachtenvermindering, de handfunctie of de kans op bijwerkingen.
Open chirurgie leidt mogelijk na 12-20 weken tot grotere reductie van symptomen dan corticosteroïdinjecties (kwaliteit van bewijs laag). Op kortere termijn lijkt er geen verschil te zijn in klachtenvermindering, handfunctie of kans op bijwerkingen.
De aard van de potentiële bijwerkingen is bij een operatie wel ernstiger.
Kwaliteit van bewijs
De kwaliteit van het bewijs is laag. Er is afgewaardeerd voor serieuze kans op bias door imprecisie en gebrek aan blindering.
Waarden en voorkeuren
De werkgroep verwacht substantiële variatie in de afwegingen van patiënten met betrekking tot de voor- en nadelen van de interventies.
Resources
De kosten van een brace zijn enkele tientallen euro's, een handgemaakte spalk is duurder. Deze komen doorgaans voor rekening van de patiënt.
De kosten van een corticosteroïdinjectie zijn circa € 2-8 per injectie, afhankelijk van het gebruikte corticosteroïd (medicijnkosten.nl, geraadpleegd 10 januari 2021).
De kosten van een operatie zijn hoger dan een spalkbehandeling of (herhaalde) corticosteroïd injectie.
Aanvaardbaarheid
Beide interventies zijn reeds beschikbaar in de huidige praktijk. Eventueel zal verwezen moeten worden voor een operatie, of het verrichten van de injectie indien de huisarts zich hiertoe niet bekwaam acht.
Uitgangsvraag
Is een chirurgische behandeling (vergeleken met een corticosteroïdinjectie) aan te bevelen bij de behandeling van patiënten met CTS?
| Patiënten | Patiënten met carpaletunnelsyndroom |
|---|---|
| Interventie | Open chirurgie |
| Vergelijking | Corticosteroïdinjectie |
| Uitkomstmaten | Ernst klachten Handfunctie Recidief Bijwerkingen/complicaties Werkhervatting |
Achtergrond
De effectiviteit van open chirurgie ten opzichte van veelgebruikte niet-operatieve behandelingen voor het CTS is onduidelijk.
Methode
Er is een systematische literatuurzoekactie naar SR’s en RCT’s uitgevoerd in PubMed en Embase in januari 2020.
Resultaten
Resultaat zoekactie
De zoekactie leverde 3 systematische literatuuronderzoeken op waarin de effectiviteit van chirurgie werd vergeleken met niet-chirurgische behandelingen bij CTS. De review van Shi voldeed aan de AMSTAR-criteria en werd als uitgangspunt genomen. Een aanvullende search na de zoekdatum van dit literatuuronderzoek leverde geen aanvullende RCT’s op.
Onderzoekskarakteristieken
Shi includeerde RCT’s waarin chirurgie met diverse conservatieve behandelingen voor CTS werden vergeleken. Er werden 3 RCT’s geïncludeerd waarin open chirurgie werd vergeleken met corticosteroïdinjecties. De behandeling vond plaats in ziekenhuis setting. De follow-upduur varieerde van 12 weken tot 2 jaar. De gemiddelde leeftijd van de deelnemers was 45-52 jaar en 73-96% was vrouw.
Effectiviteit en bijwerkingen
Bekijk de tabel voor de samenvatting van de resultaten. De ernst van de symptomen werd gemeten met de Global Symptom Score (GSS). Deze beoordeelt de symptomen op een schaal van 0 (geen symptomen) tot 10 (ernstig) in 5 categorieën: pijn, gevoelloosheid, paresthesie, zwakte/onhandigheid en nachtelijk ontwaken. De totaalscore heeft een bereik van 0-50. De resultaten van de RCT’s voor deze uitkomst hebben we gepoold met een random effects model. Bij handknijpkracht wordt een toename van 5,0-6,5 kg klinisch relevant beschouwd.
Recidiefkans
In de geïncludeerde onderzoeken werden geen uitspraken gedaan over de kans op recidief na corticosteroïdinjectie(s).
Conclusie
- Er is na 4-6 weken mogelijk niet of nauwelijks verschil in reductie van symptomen tussen open chirurgie en corticosteroïdinjecties (kwaliteit van bewijs laag).
- Open chirurgie leidt na 12-20 weken mogelijk tot een grotere reductie van symptomen in vergelijking met corticosteroïdinjecties (kwaliteit van bewijs laag).
- Er is na 3 maanden mogelijk niet of nauwelijks verschil in reductie van nachtelijke paresthesieën, pijn overdag en functionele beperkingen (kwaliteit van bewijs laag).
- Er is mogelijk niet of nauwelijks verschil in handfunctie (kwaliteit van bewijs laag).
- Er traden geen ernstige bijwerkingen op. Bijwerkingen van voorbijgaande aard komen wel veelvuldig voor, maar er is mogelijk niet of nauwelijks verschil in de kans op bijwerkingen tussen open chirurgie en corticosteroïdinjecties (kwaliteit van bewijs laag).
- Er is niet gerapporteerd over de uitkomsten ‘recidief’ en ‘werkhervatting’.
Uitgangsvraag
Is een chirurgische behandeling (vergeleken met een spalkbehandeling) aan te bevelen bij de behandeling van patiënten met CTS?
| Patiënten | Patiënten met carpaletunnelsyndroom |
|---|---|
| Interventie | Openchirurgie |
| Vergelijking | Spalkbehandeling |
| Uitkomstmaten | Ernst klachten Handfunctie Recidief Bijwerkingen/complicaties Werkhervatting |
Achtergrond
De effectiviteit van open chirurgie in vergelijking tot veelgebruikte niet-operatieve behandelingen voor het CTS is onduidelijk.
Methode
Er is een systematische literatuurzoekactie naar SR’s en RCT’s uitgevoerd in PubMed en Embase in september 2020.
Resultaten
Resultaat zoekactie
De zoekactie leverde 2 systematische literatuuronderzoeken op naar de effectiviteit van chirurgie vergeleken met niet-chirurgische behandelingen bij CTS. De review van Shi voldeed aan de AMSTAR-criteria en werd als uitgangspunt genomen. Een aanvullende search na de zoekdatum van dit literatuuronderzoek leverde geen aanvullende RCT’s op.
Onderzoekskarakteristieken
Shi includeerde RCT’s waarin chirurgie werd vergeleken met diverse conservatieve behandelingen voor CTS. In 3 RCT’s werd open chirurgie vergeleken met spalkbehandeling. De behandeling vond plaats in ziekenhuizen. De follow-upduur varieerde van 12 weken tot 1 jaar. De gemiddelde leeftijd van de deelnemers was 45-51 jaar en 53-95% was vrouw.
Effectiviteit en bijwerkingen
Bekijk de tabel voor de samenvatting van de resultaten. Voor de success rate wordt een toename van 25% van het aantal responders op de behandeling als klinisch relevant beschouwd. De Boston Carpal Tunnel Questionnaire (BCTQ) geeft inzicht in de klachten en de ernst van de klachten bij het uitvoeren van specifieke handelingen. De BCTQ bestaat uit 2 delen:
- de Symptom Severity Scale (SSS), 11 items betreffende de ernst van de klachten;
- de Functional Status Scale (FSS), 8 items over de belemmering in uitvoering van specifieke activiteiten.
Beide onderdelen van de BCTQ hebben een bereik van 0-5. Een afname van de baseline BCTQ-SSS met minimaal 46% en een afname van de baseline BCTQ-FSS met minimaal 28% worden klinisch relevant beschouwd.
Recidiefkans
In de geïncludeerde onderzoeken werden geen uitspraken gedaan over de kans op recidief na het stoppen van de spalkbehandeling. Er zijn wel aanwijzingen dat bij circa 5% van de patiënten de klachten persisteren.
Conclusie
- Open chirurgie heeft na 6 weken tot 6 maanden mogelijk een grotere succeskans dan spalkbehandeling (kwaliteit van bewijs laag). Na 12 maanden is er mogelijk geen verschil meer (kwaliteit van bewijs laag).
- Er is na 6 weken tot 12 maanden mogelijk niet of nauwelijks verschil in reductie van symptomen en handfunctie tussen open chirurgie en spalkbehandeling (kwaliteit van bewijs laag).
- Er traden geen ernstige bijwerkingen op. Bijwerkingen van voorbijgaande aard komen wel veelvuldig voor, maar er is mogelijk niet of nauwelijks verschil in de kans op bijwerkingen tussen open chirurgie en spalkbehandeling (kwaliteit van bewijs laag).
- Er is niet gerapporteerd over de uitkomsten ‘recidief’ en ‘werkhervatting’.
Controles
Naar Samenvatting ›- Controleer het effect van de behandeling na ongeveer 4-6 weken, of eerder bij toename van klachten of aanwijzingen voor complicaties.
- Heroverweeg de diagnose bij geen effect op de ingezette behandeling. Verwijs zo nodig voor verdere diagnostiek of behandeling (zie Consultatie en verwijzing bij CTS).
- Adviseer zwangeren contact op te nemen indien > 6 weken na de bevalling nog hinderlijke klachten bestaan.
Controle na spalkbehandeling
Naar Samenvatting ›- Stop een spalkbehandeling indien de spalk correct gedragen is maar na 4-6 weken niet leidt tot vermindering van de klachten.
- Probeer de spalk bij goed effect op geleide van klachten af te bouwen:
- bouw de spalk bij belastende momenten als laatste af
- heroverweeg de behandeling (of de diagnose) indien het afbouwen niet succesvol is
Controle na corticosteroïdinjectie
Naar Samenvatting ›- Indien de injectie geen effect heeft, overweeg dan een alternatieve diagnose, incorrecte techniek of non-respons van de patiënt.
- Geef eventueel eenmalig nogmaals een corticosteroïdinjectie.
- Indien de klachten recidiveren, herhaal de injectie dan alleen als het effect duidelijk aanwezig en langdurig was, en niet eerder dan 3-6 maanden na de laatste injectie.
Consultatie en verwijzing bij CTS
Naar Samenvatting ›Nadere diagnostiek
Naar Samenvatting ›- Verwijs patiënten met een mogelijk CTS en matige tot ernstige klachten naar de algemeen, plastisch, orthopedisch of neurochirurg dan wel neuroloog (afhankelijk van de lokale afspraken).
- De keuze voor EMG of zenuwecho is ziekenhuisafhankelijk.
Handtherapie
Naar Samenvatting ›Overweeg verwijzing naar de handtherapeut:
- bij twijfel over het gebruik en de keuze van de spalk
- als een bestaande spalk goed effect heeft, maar niet comfortabel is of niet duurzaam genoeg voor langdurig gebruik
- Er is veel onduidelijk over de inhoud van de termen ‘handentherapie’ en ‘handentherapeut’. Handtherapie omvat (een combinatie van) advies over belasting en ADL, ondersteunende immobilisatiemiddelen en oefentherapie. Een handtherapeut is een fysio- of ergotherapeut die zich gespecialiseerd heeft in hand- en polsklachten.
- Vanwege de vaak complexe aard van hand- en polsklachten en hun specifieke behandeling kan het voordelig zijn om specifiek naar een handtherapeut te verwijzen bij hand- en polsklachten. De keuze voor de verwijzer hangt af van het netwerk van de individuele huisartsenpraktijk en de regionale beschikbaarheid van handtherapeuten en gespecialiseerde behandelcentra (zie ook https://handtherapie.com/patiënten/zoek-uw-handtherapeut)
Bedrijfsarts
Naar Samenvatting ›Adviseer patiënten contact op te nemen met de bedrijfsarts bij een vermoeden van werkgerelateerde klachten of klachten bij werkzaamheden:
- voor het bespreken van de aard van de behandeling in relatie tot de werkomstandigheden
- voor het bespreken van (tijdelijke) werkaanpassingen
- bij twijfel over behoud van het werk van de patiënt
- voor afstemming van het behandelbeleid en de inzetbaarheid van de patiënt.
Verwijzing voor mogelijke operatieve behandeling
Naar Samenvatting ›- Overweeg verwijzing naar een algemeen, plastisch, orthopedisch of neurochirurg (afhankelijk van de lokale afspraken):
- bij CTS-klachten met ernstige invloed op het dagelijks functioneren of op het werk
- bij symptomatische krachtvermindering van de m. opponens pollicis of m. abductor pollicis brevis
- bij duimmuisatrofie
- bij aanhoudende klinische klachten ondanks conservatieve behandeling of corticosteroïdinjectie
- Overweeg verwijzing naar een ‘CTS-straat’ indien deze in de regio beschikbaar is.
Beleid bij ganglion
Naar Samenvatting ›Voorlichting en advies
Naar Samenvatting ›Leg uit dat het een onschuldige aandoening betreft die bij de helft van de patiënten spontaan verdwijnt.
Thuisarts
Naar Samenvatting ›Verwijs naar de informatie op thuisarts.nl. De informatie op Thuisarts is gebaseerd op deze NHG-Standaard.
Aspiratie
Naar Samenvatting ›We bevelen aspiratie niet aan, want dit is mogelijk niet effectiever dan afwachtend beleid. Het achterlaten van corticosteroïden heeft geen toegevoegde waarde.
Overweeg aspiratie bij patiënten met zwaarwegende contra-indicaties voor operatie, bespreek dat de voordelen van aspiratie onzeker zijn en leg uit dat:
- het risico op bijwerkingen, waaronder aanhoudende lokale gevoeligheid, ongeveer 3-5% is
- de recidiefkans na aspiratie ongeveer 50% is
- laat geen corticosteroïden achter
De werkgroep ontraadt het verrichten van een aspiratie als behandeling voor een symptomatisch ganglion, omdat er in effectiviteit mogelijk geen verschil is met afwachtend beleid, maar de patiënt wel wordt blootgesteld aan eventuele bijwerkingen. Er is geen bewijs dat het toevoegen van corticosteroïden invloed heeft op de recidiefkans. Het achterlaten van corticosteroïden wordt daarom in ieder geval afgeraden.
Voor- en nadelen
Aspiratie met of zonder achterlaten van corticosteroïden heeft geen effect op de gerapporteerde pijn en handfunctie, of op de kans op recidief. Er is een kleine kans op bijwerkingen bij aspiratie met achterlating van corticosteroïden.
Kwaliteit van bewijs
De kwaliteit van het bewijs is laag. Er werd afgewaardeerd voor risico op bias.
Waarden en voorkeuren
De werkgroep schat in dat weinig patiënten zullen opteren voor aspiratie (met of zonder corticosteroïd) op basis van de bekende voor- en nadelen.
Middelen
De kosten van een corticosteroïdinjectie zijn circa € 2-8 per injectie, afhankelijk van het gebruikte corticosteroïd (medicijnkosten.nl, geraadpleegd 10 januari 2021).
Aanvaardbaarheid
Voor een aspiratie met of zonder corticosteroïd geldt dat er ook patiënten zijn die een duidelijke voorkeur hebben voor (of weerstand tegen) een injectie.
Uitgangsvraag
Is aspiratie met of zonder corticosteroïden (vergeleken met afwachtend beleid) aan te bevelen bij patiënten met een ganglion?
| Patiënten | Patiënten met ganglion |
|---|---|
| Interventie | Aspiratie met of zonder corticosteroïden |
| Vergelijking | Afwachtend beleid |
| Uitkomstmaten | Klachten Recidief Bijwerkingen Werkhervatting |
Achtergrond
De effectiviteit van aspiratie, eventueel gecombineerd met een corticosteroïdinjectie, in vergelijking met afwachtend beleid bij ganglion is onduidelijk.
Methode
Er is een systematische literatuurzoekactie naar SR’s en RCT’s uitgevoerd in PubMed en Embase in januari 2020 en een systematische literatuurzoekactie naar cohortonderzoeken uitgevoerd in PubMed in april 2020.
Resultaten
Resultaat zoekactie
De zoekactie leverde 1 systematisch literatuuronderzoek op waarin de effectiviteit van aspiratie werd vergeleken met afwachtend beleid bij ganglion. Een aanvullende search na de zoekdatum van dit literatuuronderzoek leverde geen aanvullende RCT’s of cohortonderzoeken op.
Onderzoekskarakteristieken
Head includeerde 2 cohortonderzoeken met in totaal 209 deelnemers met een ganglion (76 deelnemers met ganglion in handpalm en 133 deelnemers met ganglion op bovenzijde pols). In deze cohortonderzoeken werd de effectiviteit van aspiratie met of zonder corticosteroïden vergeleken met afwachtend beleid. De behandelingen vonden plaats in een poliklinische setting. De follow-upduur was 5 en 6 jaar. De gemiddelde leeftijd van de deelnemers was 47 versus 37 jaar en de meerderheid was vrouw (63 versus 73%).
Effectiviteit en bijwerkingen
Bekijk de tabel voor de samenvatting van de resultaten. De Patient Evaluation Measure (PEM) geeft inzicht in de klachten en beperkingen op basis van 14 vragen over de handfunctie, zoals pijn en uiterlijk, impact op het werk en tevredenheid. De vragenlijst wordt gescoord op een 7-punts visuele analoge schaal en uitgedrukt als percentage van het maximum (100% is volledig beperkt).
Conclusie
- Er zijn geen gerandomiseerde onderzoeken bekend waarin de effectiviteit van aspiratie met corticosteroïden vergeleken met afwachtend beleid bij ganglion is onderzocht.
- Er is op langere termijn mogelijk niet of nauwelijks verschil in het ervaren van pijn, handfunctie of optreden van een recidief tussen aspiratie en afwachtend beleid (kwaliteit van bewijs laag).
- Bij aspiratie treden mogelijk bijwerkingen op bij 3-5% van de patiënten (kwaliteit van bewijs laag).
- Er is mogelijk niet of nauwelijks verschil in werkhervatting tussen aspiratie en afwachtend beleid (kwaliteit van bewijs laag).
Operatieve behandeling
Naar Samenvatting ›Overweeg bij patiënten met ernstige klachten van een symptomatisch ganglion en een (duidelijke) wens hebben tot behandeling een verwijzing voor excisie gezien de kleinere kans op recidief. Een excisie kan open (meestal) of endoscopisch worden uitgevoerd.
Bespreek de voor- en nadelen:
- de recidiefkans na excisie is 21%, dat is lager dan bij afwachtend beleid of aspiratie
- het risico op complicaties, waaronder vasculaire schade, (tijdelijke) neurogene schade en littekenvorming, is ongeveer 14%
Een operatie lijkt effectiever in het voorkomen van een recidief bij een symptomatisch ganglion. Daarnaast is de kans op bijwerkingen beperkt. De werkgroep ontraadt het verrichten van een aspiratie als behandeling voor een symptomatisch ganglion, omdat er geen verschil is in effectiviteit met een afwachtend beleid, maar de patiënt wel blootstelt aan bijwerkingen.
Voor- en nadelen
Er is geen bewijs ten aanzien van het effect op de ernst van de klachten. De kans op recidief is lager bij een excisie dan bij een aspiratie met achterlaten van corticosteroïden. Echter is het onduidelijk of dit een symptomatisch recidief betrof. De frequentie en aard van de potentiële bijwerkingen is bij een operatie meer en ernstiger dan van een aspiratie met of zonder corticosteroïden.
Kwaliteit van bewijs
De kwaliteit van het bewijs was laag. Er werd afgewaardeerd in verband met risico op bias en onnauwkeurigheid (bewijs soms gebaseerd op 2 onderzoeken met kleine aantallen patiënten).
Waarden en voorkeuren
De werkgroep verwacht substantiële variatie in de afweging van patiënten met betrekking tot de voor- en nadelen van de interventies.
Middelen
De kosten van een corticosteroïdinjectie zijn circa € 2-8 per injectie, afhankelijk van het gebruikte corticosteroïd (medicijnkosten.nl, geraadpleegd 10 januari 2021). De kosten van een operatie zijn hoger dan die van (herhaalde) aspiratie met of zonder corticosteroïd.
Aanvaardbaarheid
- Een operatie zal om meerdere redenen (onder andere perceptie van de impact, pijn, nabehandeling, gevolgen voor werk, cosmetische bewaren tegen een litteken) voor sommige patiënten niet wenselijk zijn.
- Voor aspiratie met of zonder corticosteroïd geldt dat er ook patiënten zijn, die een duidelijke voorkeur hebben voor (of weerstand tegen) een injectie.
Haalbaarheid
Beide interventies zijn reeds beschikbaar in de huidige praktijk. Eventueel zal verwezen moeten worden voor een operatie.
Uitgangsvraag
Is een aspiratie met of zonder corticosteroïden (vergeleken met open chirurgie) aan te bevelen bij patiënten met ganglion?
| Patiënten | Patiënten met ganglion |
|---|---|
| Interventie | Aspiratie met of zonder corticosteroïden |
| Vergelijking | Open chirurgie |
| Uitkomstmaten | Klachten Recidief Bijwerkingen Werkhervatting |
Achtergrond
De effectiviteit van aspiratie, eventueel gecombineerd met een corticosteroïdinjectie, in vergelijking met chirurgische excisie bij een ganglion is onduidelijk.
Methode
Er is een systematische literatuurzoekactie naar SR’s en RCT’s uitgevoerd in PubMed en Embase in januari 2020.
Resultaten
Resultaat zoekactie
De zoekactie leverde een systematisch literatuuronderzoek naar de effectiviteit van open chirurgie vergeleken met aspiratie bij ganglion op. Een aanvullende search na de zoekdatum van dit literatuuronderzoek leverde één aanvullende RCT op.
Onderzoekskarakteristieken
Head includeerde 2 RCT’s met in totaal 60 deelnemers met een ganglion op de bovenzijde van de pols (24 versus 36 deelnemers) waarin de effectiviteit van open chirurgie werd vergeleken met aspiratie met corticosteroïden.
De behandelingen vonden plaats in een poliklinische setting. De follow-upduur was 6-12 maanden. De gemiddelde leeftijd van de deelnemers was 31 jaar en de meerderheid was vrouw (81 versus 83%).
Hassan vergeleek chirurgie met aspiratie met corticosteroïden bij 100 deelnemers met ganglion aan de pols (zijde niet nader gespecificeerd).
De gemiddelde leeftijd van de deelnemers was 47 jaar en 58% was vrouw. De follow-upduur was 3 maanden. We hebben geen RCT’s gevonden die open chirurgie vergeleken met aspiratie zonder corticosteroïden.
Effectiviteit en bijwerkingen
Bekijk de tabel voor de samenvatting van de resultaten. Er traden geen complicaties op in de beide behandelgroepen. De RCT’s zijn te klein om complicatiegegevens rigoureus te evalueren. In Head 2015 werden daarom de complicaties over verschillende onderzoeksontwerpen gepoold (RCT, cohort en casusreeksen).
Conclusie
- Bij aspiratie met corticosteroïden is de kans op een recidief mogelijk groter dan bij open chirurgie (kwaliteit van bewijs laag).
- Bij aspiratie met corticosteroïden treden mogelijk minder complicaties en minder ernstige complicaties op in vergelijking met open chirurgie (kwaliteit van bewijs laag).
- Er is niet gerapporteerd over de uitkomsten ‘verminderen/verdwijnen van klachten’ en ‘werkhervatting’.
- Aspiratie zonder corticosteroïden in vergelijking met open chirurgie is niet onderzocht.
Controles
Naar Samenvatting ›Nodig patiënten die kiezen voor afwachtend beleid uit om terug te komen indien zij alsnog excisie wensen.
Consultatie en verwijzing
Naar Samenvatting ›Verwijs patiënten met een duidelijke behandelwens voor excisie van het ganglion naar een algemeen, plastisch of orthopedisch chirurg (afhankelijk van de lokale afspraken):
- indien het ganglion pijn of ADL-beperkingen geeft
- bij een recidief ganglion na aspiratie
- bij ulceratie van de cyste aan het DIP-gewricht (‘mucoïdcyste’). Bij ernstige artrose kan een artrodese van het DIP-gewricht noodzakelijk zijn; bereid de patiënt hierop voor.
Beleid bij handartrose
Naar Samenvatting ›- Behandel zo lang mogelijk conservatief, kies bij voorkeur voor een combinatie van behandelingen (zoals een spalk met handtherapie en pijnstilling; eventueel een corticosteroïdinjectie op indicatie).
- Besteed aandacht aan alle domeinen van artrose (zie Artrose van de hand en Diagnostiek bij handartrose)
Samenvatting van bewijs
Achtergrond
Bij het conservatieve beleid bij (CMC-I-)artrose wordt een individuele balans gezocht tussen belasting en belastbaarheid door het toepassen van een combinatie van behandelingen die patiënten zo lang mogelijk een acceptabel niveau van functioneren en pijn geven. Een van de mogelijkheden is het gebruik van een spalk. Deze wordt ingezet om de belastbaarheid van de hand te vergroten en de kans op overbelasting te verminderen. De huisarts kan zelf een advies geven over de spalkbehandeling of hiervoor verwijzen naar een gespecialiseerde handtherapeut.
Resultaten
Buhler et al. bespreken in een meta-analyse 4 tweedelijns RCT’s (n = 236) waarin de effectiviteit van een spalkbehandeling wordt vergeleken met gebruikelijke zorg zonder spalk bij patiënten met CMC-I-artrose.[Buhler 2019] In 3 onderzoeken werd een rigide CMC-spalk gebruikt, in 1 onderzoek een zachte spalk. De follow-up varieerde van 1 tot 12 maanden. De uitkomstmaten waren pijn (gemeten op een VAS-schaal) en functie (met diverse vragenlijsten).
Effectiviteit en bijwerkingen
Op de korte termijn (0 tot 3 maanden) werd niet of nauwelijks verschil gezien tussen een spalk of de gebruikelijke zorg zonder spalk. Op de middellange termijn (3 tot 12 maanden) werd meer reductie van pijn gezien met een spalk (SMD -0,7;95%-BI -1,04 tot -0,35) en een kleine verbetering in functie (SMD -0,42; 95%-BI: -0,77 tot -0,08).
Er werden geen belangrijke bijwerkingen gerapporteerd. Geen van de studies rapporteerden over kwaliteit van leven.
Kwaliteit van bewijs
De kwaliteit van bewijs was laag tot zeer laag. Er werd afgewaardeerd voor risico op bias (door het gebrek aan blindering) en onnauwkeurigheid.
Conclusie
Op basis van de bestaande studies lijkt een spalk niet of nauwelijks effect te hebben op de pijn en de functie op de korte termijn (0 tot 3 maanden; kwaliteit van bewijs: zeer laag). Mogelijk geeft een spalk wel iets meer verbetering van pijn en functie op de middellange termijn (3-6 maanden; kwaliteit van bewijs: laag). Het effect op kwaliteit van leven is onzeker wegens gebrek aan bewijs. Bijwerkingen door het gebruik werden niet gerapporteerd.
Waarom deze aanbeveling
Er is onzekerheid over het effect van een spalkbehandeling. Mogelijk is er een beperkt postief effect op de pijn en de functie bij CMC-I-artrose op de middellangetermijn. Er is variatie te verwachten in hoe acceptabel patiënten een spalk vinden; of ze het ongemak vinden opwegen tegen de mogelijke voordelen. De aard van de klachten, bij welke activiteiten men klachten ervaart, praktische aspecten, het draagcomfort en de kosten zullen tegen elkaar moeten worden afgewogen om tot een individuele keuze te komen.
Voorlichting en advies
Naar Samenvatting ›- Leg uit dat:
- de oorzaak niet altijd bekend is, maar dat langdurige belasting, een oud trauma, instabiliteit en (bekende) reumatoïde artritis een oorzaak kunnen zijn.
- het beloop variabel is en tijdelijke opvlammingen kent.
- progressie gepaard gaat met krachtsverlies en uiteindelijk deformatie.
- Bespreek:
- de relatie tussen belasting en belastbaarheid.
- de mogelijkheden tot aanpassing van de dagelijkse werkzaamheden.
- Benadruk dat het belangrijk is de hand en pols binnen de pijngrenzen te blijven gebruiken om onnodige stijfheid te voorkomen
Thuisarts
Naar Samenvatting ›Verwijs naar de informatie op thuisarts.nl. De informatie op Thuisarts is gebaseerd op deze NHG-Standaard.
Niet-medicamenteuze behandeling
Naar Samenvatting ›Spalkbehandeling
Naar Samenvatting ›- Overweeg een spalkbehandeling bij patiënten met belastingafhankelijke klachten en een voorkeur voor deze behandeling.
- Adviseer de brace te gebruiken als ondersteuning op basis van het optreden en de intensiteit van de dagelijkse klachten.
- Gebruik tijdens de nacht is in principe niet nodig.
- Zie Praktische aanwijzingen orthesen bij hand- en polsklachten.
- In diverse systematische literatuuronderzoeken werden geen onderzoeken gevonden van hoge kwaliteit naar spalkbehandeling bij triggervinger.
- De wel beschikbare onderzoeken zijn vaak observationeel of vergelijken 2 verschillende typen spalken. Onderling verschillen de onderzoeken substantieel in het soort spalk, de behandelduur en de gebruikte uitkomstmaten. Het succespercentage is 47-77%.
- DIP-spalken en nachtspalken lijken minder effectief dan MCP- en continue spalken. Immobilisatie van een enkel gewicht lijkt afdoende. Mogelijke bijwerkingen zijn klachten van de spalk en stijfheid.
Conclusie
Er is te weinig bewijs van voldoende kwaliteit om een gefundeerde aanbeveling te doen over het gebruik van spalken bij triggervinger. Bij de beschikbare lage succespercentages en het risico op stijfheid van de vinger met gevolgen voor de handfunctie adviseert de werkgroep terughoudendheid met het gebruik.
Handtherapie
Naar Samenvatting ›- Bij progressieve handartrose kan handtherapie mogelijk bijdragen aan het behoud van spierkracht en functie; overweeg op indicatie verwijzing naar een handtherapeut (zie Consultatie en verwijzing)
- Handtherapie kan gegeven worden in combinatie met voorlichting en eventueel spalktherapie indien dit aansluit bij de behoeften van de patiënt.
Medicamenteuze behandeling
Naar Samenvatting ›Pijnstilling
Naar Samenvatting ›Adviseer zo nodig pijnmedicatie conform het beleid bij acute nociceptieve pijn in de NHG-Standaard Pijn (paracetamol en/of een (dermaal) NSAID).
Corticosteroïdinjectie
Naar Samenvatting ›Wees terughoudend met het aanbieden van een corticosteroïdinjectie aan patiënten met CMC1-artrose. Incidenteel kan een corticosteroïdinjectie een optie zijn bij acute exacerbatie (flare) van lokale klachten die onvoldoende reageren op pijnstilling (zie NHG-Standaard Artritis).
Praktische toepassing
- Gebruik als eerste keuze op basis van praktische overwegingen 10 mg triamcinolonacetonide 10 mg/ml (zie tabel 3).
- Gelijkwaardige alternatieven zijn:
- 2 mg dexamethason 4 mg/ml
- 20 mg methylprednisolon 40 mg/ml.
- Informeer de patiënt over de bijwerkingen, waaronder voorbijgaande lokale pijnklachten, flushing, pigmentatieveranderingen rond de injectieplaats, infectie en/of zenuwschade.
- Injecteer alleen bij voldoende bekwaamheid en kennis van de anatomie, techniek en potentiële risico’s van de betreffende injectie.
- Voorkom irreversibele subcutane atrofie en vermijd te sterke subcutane opzwelling en afzetting van het steroïd langs de naald:
- spuit niet te veel vloeistof in
- trek de naald niet al spuitend terug
De kwaliteit van bewijs is zeer laag en laat geen voordeel zien van een corticosteroïdinjectie. Daarnaast geldt dat een corticosteroïdinjectie in principe al geen blijvend effect heeft op een chronische aandoening. De voorkeur gaat daarom uit naar andere behandelingen.
Voor- en nadelen
Er is te veel onzekerheid in het bewijs over de voor- en nadelen om te bepalen of de voordelen opwegen tegen de nadelen van een corticosteroïdinjectie.
Kwaliteit van bewijs
De kwaliteit van bewijs is zeer laag. Er is afgewaardeerd voor de serieuze kans op bias, inconsistenties en indirect bewijs.
Waarden en voorkeuren
De werkgroep verwacht substantiële variatie in de afweging van patiënten met betrekking tot de voor- en nadelen van beide behandelopties.
Middelen
De kosten van een corticosteroïdinjectie zijn circa € 2-8 per injectie, afhankelijk van het gebruikte corticosteroïd (medicijnkosten.nl, geraadpleegd 10 januari 2021).
Aanvaardbaarheid
Het is de mening van de werkgroep dat de meerderheid van patiënten met klachten openstaat voor een injectie.
Haalbaarheid
De behandeling wordt ingezet in de huidige praktijk en is haalbaar.
Uitgangsvraag
Is een corticosteroïdinjectie (vergeleken met conservatieve behandeling) aan te bevelen bij de behandeling van patiënten met handartrose?
| Patiënten | Patiënten met handartrose |
|---|---|
| Interventie | Corticosteroïdinjectie |
| Vergelijking | Conservatieve behandeling |
| Uitkomstmaten | Pijn Handfunctie (knijpkracht) Bijwerkingen/complicaties Werkhervatting |
Achtergrond
De effectiviteit van een corticosteroïdinjectie ten opzichte van een conservatieve behandeling voor handartrose is onduidelijk.
Methode
Er is een systematische literatuurzoekactie naar SR’s en RCT’s uitgevoerd in PubMed en Embase in januari 2020.
Resultaten
Resultaat zoekactie
De zoekactie leverde één systematisch literatuuronderzoek naar de effectiviteit en veiligheid van niet-farmacologische, farmacologische en chirurgische behandelingen bij handartrose op. Een aanvullende search na de zoekdatum van dit literatuuronderzoek leverde geen aanvullende RCT’s op.
Onderzoekskarakteristieken
In de review van Kroon werden geen RCT’s geïncludeerd die corticosteroïdinjecties vergeleken met niet-injectiegebaseerde interventies (bijvoorbeeld handtherapie, ortheses).
Wel werden 4 RCT’s geïncludeerd waarin corticosteroïdinjecties werden vergeleken met placebo, 3 trials bij patiënten met duimbasisartrose (CMC1; bereik 40-126 patiënten)
en 1 trial bij patiënten met artrose in een vingergewricht (PIP en DIP; n = 60).
Omdat de werkgroep van mening is dat de Nederlandse huisarts geen corticosteroïdinjectie overweegt bij patiënten met vingergewrichtartrose, worden de resultaten van Spolidoro niet meegenomen.
De behandeling vond plaats in ziekenhuizen. De follow-upduur was 24-26 weken. De gemiddelde leeftijd was 60-67 jaar en 68-90% was vrouw. De score op de schaal van Kellgren-Lawrence (KL-score) werd gerapporteerd in 2 onderzoeken. Een deel van de patiënten had een radiologisch ernstige artrose: 47% had een KL-score > 3,
de gemiddelde KL-score was 3.
Mandl gebruikte een anestheticum (bupivacaïne) als controle-injectie,
de overige onderzoeken gebruikten een zoutoplossing. Omdat Mandl alleen is meegenomen in de langetermijnuitkomsten (26 weken) was het gebruik van een anestheticum geen reden om dit onderzoek te excluderen.
Effectiviteit en bijwerkingen
Zie tabel 13 voor een samenvatting van de effecten op duimbasisartrose (CMC1).
De pijnscore is gemeten met een visuele analoge schaal (VAS) van 0 (geen pijn) tot 100 (ergst denkbare pijn). Een afname van 20 punten wordt klinisch relevant beschouwd.
Bij de handfunctie is gebruik gemaakt van Disabilities of the Arm, Shoulder and Hand (DASH). Hoe hoger de DASH-score, des te groter zijn de klachten of beperkingen. De DASH-score heeft een bereik van 0 tot 100, een afname van 10 punten wordt als klinisch relevant beschouwd.
Conclusie
- We vonden gerandomiseerde trials waarin corticosteroïdinjecties zijn vergeleken met placebo of hyaluronzuurinjecties. Alleen de onderzoeken die corticosteroïden vergeleken met placebo zijn meegenomen in dit overzicht.
- Bij duimbasisartrose (CMC1) zijn we onzeker of een corticosteroïdinjectie reductie van pijn of verbetering van handfunctie geeft (kwaliteit van bewijs zeer laag).
- Er zijn geen bijwerkingen opgetreden in de trials.
- Er is niet gerapporteerd over de uitkomst ‘werkhervatting’.
Controles
Naar Samenvatting ›- Controleer het effect van de behandeling na ongeveer 4-6 weken, of eerder bij toename van klachten of aanwijzingen voor complicaties.
- Pas pijnmedicatie eventueel aan bij onvoldoende effect.
- Stop een spalkbehandeling indien het dragen van de spalk na 4-6 weken niet leidt tot een vermindering van de klachten.
- Continueer de spalk bij voldoende effectiviteit op indicatie.
Consultatie en verwijzing
Naar Samenvatting ›Handtherapie
Naar Samenvatting ›Overweeg een (eenmalig) consult of verwijzing naar een handtherapeut (zie Handtherapie) bij:
- klachten tijdens dagelijkse activiteiten door beginnende deformatie of verlies van mobiliteit
- twijfel over het gebruik en de keuze van de spalk, of bij goed effect van een bestaande brace, maar als deze oncomfortabel is of niet duurzaam genoeg voor chronisch gebruik.
- advies over het aanpassen van de dagelijkse activiteiten, oefentherapie en ondersteunende hulpmiddelen.
Revalidatiearts
Naar Samenvatting ›Overweeg verwijzing naar een revalidatiearts indien:
- de behandeling gecompliceerd wordt door comorbiditeit of polyartrose, én
- het behandeldoel niet primair diagnostisch of chirurgisch is, én
- de patiënt baat kan hebben bij een multidisciplinair begeleidingstraject
Kaderarts
Naar Samenvatting ›Overweeg overleg met een kaderhuisarts bewegingsapparaat voor advies over diagnostisch onderzoek of beleid (indien regionaal beschikbaar).
Bedrijfsarts
Naar Samenvatting ›Adviseer patiënten contact op te nemen met de bedrijfsarts bij een vermoeden van werkgerelateerde klachten of klachten bij werkzaamheden:
- voor het bespreken van de aard van de behandeling in relatie tot de werkomstandigheden
- voor het bespreken van (tijdelijke) werkaanpassingen
- bij twijfel over behoud van het werk van de patiënt
- voor afstemming van het behandelbeleid en de inzetbaarheid van de patiënt.
Verwijzing voor mogelijke operatieve behandeling
Naar Samenvatting ›- Overweeg verwijzing naar een algemeen, plastisch of orthopedisch chirurg (afhankelijk van de lokale afspraken) bij langdurige pijn of bewegingsbeperking met consequenties voor ADL-activiteiten en onvoldoende effect van conservatieve therapie, vooral van het CMC1- of STT-gewricht omdat hier de meeste chirurgische opties zijn.
- Er zijn veel verschillende (combinaties van) operatieve behandelopties, zonder dat een daarvan bewezen superieur is:
- ligamentreconstructie bij instabiliteit
- osteotomie
- ostectomie
- artrodese
- gewrichtsvervanging
- De behandelkeuze ligt bij de behandelend specialist.
Er is grote diversiteit in (combinaties van) operatieve behandelopties zonder bewezen superioriteit van een bepaalde techniek.
Beleid bij triggervinger
Naar Samenvatting ›Voorlichting en advies
Naar Samenvatting ›- Leg uit dat een vernauwing van de peesschede en soms de pees zelf zorgt voor het ‘hokken’ van de vinger.
- Bespreek dat de indicatie voor behandeling afhangt van de mate van klachten.
- Leg uit dat de klachten spontaan verbeteren bij tot ongeveer 30% van de patiënten.
Thuisarts
Naar Samenvatting ›Verwijs naar de informatie op thuisarts.nl. De informatie op Thuisarts is gebaseerd op deze NHG-Standaard.
Spalkbehandeling
Naar Samenvatting ›We bevelen het dragen van een (nacht)spalk niet aan, vanwege het ontbreken van voldoende bewijs voor effectiviteit.
Corticosteroïdinjectie
Naar Samenvatting ›Overweeg een corticosteroïdinjectie in eerste instantie bij patiënten met een symptomatische triggervinger en wens tot behandeling. Bespreek de voor- en nadelen, leg uit dat de kans dat de symptomen verdwijnen na een injectie ongeveer 60% is.
Praktische toepassing
- Gebruik als eerste keuze op basis van praktische overwegingen 5 mg triamcinolonacetonide 10 mg/ml (zie tabel 3).
- Gelijkwaardige alternatieven zijn:
- 1 mg dexamethason 4 mg/ml
- 10 mg methylprednisolon 40 mg/ml.
- Informeer de patiënt over de bijwerkingen, waaronder voorbijgaande lokale pijnklachten, flushing, pigmentatieveranderingen rond de injectieplaats, infectie en peesschade.
- Injecteer alleen bij voldoende bekwaamheid en kennis van de anatomie, techniek en potentiële risico’s van de betreffende injectie.
- Voorkom irreversibele subcutane atrofie en vermijd te sterke subcutane opzwelling en afzetting van het steroïd langs de naald:
- spuit niet te veel vloeistof in
- trek de naald niet al spuitend terug
- Bij een injectie voor een tenosynovitis is het van belang de injectie te plaatsen in de peesschede en niet in de pees, vanwege het risico op peesrupturen bij herhaalde injecties in ontstoken pezen.
De voorkeur van de werkgroep gaat in eerste instantie uit naar de minst invasieve behandeling, aangezien het onzeker is of er een verschil is in effectiviteit tussen corticosteroïdinjecties en open chirurgie. Daarnaast is het niet mogelijk een uitspraak te doen over de daadwerkelijke handfunctie en resolutie. Weliswaar lijkt het risico op complicaties even groot en is er bij een operatie een kleinere kans op een recidief, maar de impact van een operatie (en de eventuele complicaties) is groter dan voor een injectie. Een getrapte behandeling heeft daarom de voorkeur.
Voor- en nadelen
Er is te veel onzekerheid door de zeer lage kwaliteit van de onderzoeken met betrekking tot het effect van beide interventies op het verdwijnen van de klachten om hierover een uitspraak te doen. Er zijn minder recidieven na een operatie (< 1 jaar), maar meer pijnklachten in de eerste week ten opzichte van een corticosteroïdinjectie.
Kwaliteit van bewijs
De kwaliteit van het bewijs was laag tot zeer laag. Er werd afgewaardeerd i.v.m. serieuze kans op bias, inconsistentie en onnauwkeurigheid door onder andere de lage aantallen in de onderzoeken en afwezigheid van blindering.
Waarden en voorkeuren
De werkgroep verwacht substantiële variatie in de afweging van patiënten met betrekking tot de voor- en nadelen van de interventies.
Middelen
De kosten van een corticosteroïdinjectie zijn circa € 2-8 per injectie, afhankelijk van het gebruikte corticosteroïd (medicijnkosten.nl, geraadpleegd 4 mei 2020). De kosten van een operatie zijn hoger dan die van een (herhaalde) corticosteroïdinjectie.
Aanvaardbaarheid
De hogere recidiefkans bij een injectie kan patiënten ervan weerhouden om voor deze optie te kiezen. Een operatie kan om meerdere redenen (perceptie van de impact, pijn, nabehandeling, gevolgen voor werk, cosmetische bezwaren tegen een litteken) voor sommige patiënten niet aanvaardbaar zijn, in ieder geval in eerste instantie.
Haalbaarheid
Beide interventies zijn reeds beschikbaar in de huidige praktijk. Eventueel zal verwezen moeten worden voor een operatie, of het verrichten van de injectie indien de huisarts zich hiertoe niet bekwaam acht.
Uitgangsvraag
Is een corticosteroïdinjectie (vergeleken met open chirurgie) aan te bevelen bij patiënten met triggervinger?
| Patiënten | Patiënten met triggervinger (duim of andere vingers) |
|---|---|
| Interventie | Corticosteroïdinjectie |
| Vergelijking | Open chirurgie |
| Uitkomstmaten | Ervaren verbetering Pijn Ernst klachten (pijn) Handfunctie Recidief Bijwerkingen/complicaties Werkverzuim |
Achtergrond
Bij een triggervinger zijn er verschillende behandelopties. Naast een afwachtend beleid, kan een corticosteroïdinjectie (ontstekingsremmers) of operatie overwogen worden. Huisartsen kunnen een corticosteroïdinjectie zelf toedienen, maar wat zijn de effecten en bijwerkingen van corticosteroïdinjectie? We vergelijken met open chirurgie, omdat percutane chirurgie zelden in Nederland wordt gedaan (5% van de operaties).
Methode
Er is een systematische literatuurzoekactie naar SR’s en RCT’s uitgevoerd in PubMed en Embase in januari 2020.
Resultaten
Resultaat zoekactie
De zoekactie leverde een systematisch literatuuronderzoek (cochranereview) op naar de effectiviteit van chirurgie bij triggervinger. Een aanvullende search na de zoekdatum van dit literatuuronderzoek leverde geen aanvullende RCT’s op.
Onderzoekskarakteristieken
De cochranereview includeerde 2 RCT’s met in totaal 269 deelnemers (270 triggervingers). Hierin werd de effectiviteit van open chirurgie vergeleken met corticosteroïdinjecties bij de behandeling van triggervinger (zowel duim als andere vingers). De behandelingen vonden plaats in een poliklinische setting. De follow-upduur was 6-12 maanden. De gemiddelde leeftijd van de deelnemers was 54-60 jaar en 67-88% was vrouw. De interventies in de geïncludeerde RCT’s verschilden iets: Hansen gebruikte echogeleide injecties, terwijl Sato injecties deed zonder het gebruik van echo. In beide trials werd de injectie herhaald bij uitblijven van effect.
Effectiviteit en bijwerkingen
Bekijk de tabel voor de samenvatting van de resultaten. Verdwijnen van klachten is gedefinieerd als het uitblijven van terugval of terugkeer van de triggervinger (triggervinger score I of IIa). In 1 RCT werd pijn gescoord op een numerical rating scale (NRS) van 1 (geen pijn) tot 10 (ergst denkbare pijn). Een afname van 2 punten werd als klinisch relevant beschouwd. De andere RCT rapporteerde het percentage patiënten dat plaatselijk pijn ervoer. Voor de subgroep met een triggerduim werden effectiviteit en veiligheid niet apart gerapporteerd
Conclusie
- We zijn onzeker of een injectie met corticosteroïden minder klachtenreductie geeft dan open chirurgie (kwaliteit van bewijs zeer laag).
- Corticosteroïdinjecties geven mogelijk minder pijn op korte termijn (1 week) in vergelijking met open chirurgie, op middellange termijn (3-6 maanden) is er mogelijk niet of nauwelijks verschil en op langere termijn (12 maanden) ervaren patiënten mogelijk meer pijn (kwaliteit van bewijs laag).
- Corticosteroïdinjecties hebben in vergelijking met chirurgie een grotere kans op een recidief (kwaliteit van bewijs redelijk).
- Er is mogelijk niet of nauwelijks verschil in het optreden en de ernst van de bijwerkingen (kwaliteit van bewijs laag). Bijwerkingen die optraden zijn infecties, opvliegers, huidongemakken en vetnecrose. Deze traden op in beide groepen.
- Er is niet gerapporteerd over de uitkomst ‘handfunctie’.
Corticosteroïdinjectie bij diabetes mellitus
Naar Samenvatting ›Wees bij patiënten met (insulineafhankelijke) diabetes terughoudend met het herhalen van de injectie vanwege persisterende klachten (< 3-6 maanden); de succeskans is waarschijnlijk lager dan bij niet-diabetici.
Er is een meta-analyse van 5 onderzoeken naar de effectiviteit van corticosteroïdinjecties bij diabetici met een triggervinger. De kwaliteit van zowel de meta-analyse en de geïncludeerde onderzoeken (1 RCT, 1 prospectief cohortonderzoek, 3 retrospectieve onderzoeken) is echter laag tot zeer laag.
Onderzoekskarakteristieken
De meta-analyse van Chang omvatte in totaal 381 patiënten met diabetes en 449 patiënten zonder diabetes. Van de 5 geïncludeerde artikelen vergeleken er 4 injecties bij diabetici en niet-diabetici, en daarvan vergeleken er 3 ook niet-insulineafhankelijke met insulineafhankelijke diabetici. Bij 1 onderzoek ontbrak een controlegroep met patiënten zonder diabetes. Primaire uitkomstmaat was therapiefalen, gedefinieerd als persisterende pijnklachten of noodzaak tot operatie. Bij 3 onderzoeken volgde rapportage na 1 en 3 injecties, bij 1 onderzoek na 1 injectie en bij 1 onderzoek na 3 injecties. De follow-upduur varieerde van 3 weken tot 3 maanden.
Resultaten
Na 1 injectie was er geen verschil in therapiefalen tussen diabetici en niet-diabetici (faalpercentage 64 versus 49%; RR 1,49; 95%-BI 0,80 tot 2,79; p = 0,21). Er was wel een significant hoger risico op therapiefalen na 3 injecties binnen 3 maanden (faalpercentage 52 versus 30%; RR 2,03; 95%-BI 1,51 tot 2,74; p < 001), met name voor de insulineafhankelijke groep in vergelijking met de niet-diabetici (RR 2,37; 95%-BI 1,61 tot 3,47; p < 0,001).
Conclusie
Er lijkt geen verschil in therapiefalen tussen diabetici en niet-diabetici bij een eerste corticosteroïdinjectie bij een triggervinger. Bij herhaling van de injectie binnen 3 maanden is de kans op succes significant lager, met name bij insulineafhankelijke diabetici.
Controles
Naar Samenvatting ›- Controleer het effect van de behandeling na ongeveer 4-6 weken, of eerder bij toename van klachten of aanwijzingen voor complicaties.
- Indien de injectie geen effect heeft, overweeg dan een alternatieve diagnose, incorrecte techniek of non-respons van de patiënt.
- Geef eventueel eenmalig nogmaals een corticosteroïdinjectie.
- Indien de klachten recidiveren, herhaal de injectie dan alleen als het effect duidelijk aanwezig en langdurig was, en niet eerder dan 3-6 maanden na de laatste injectie.
Consultatie en verwijzing
Naar Samenvatting ›- Wees terughoudend met verwijzing voor chirurgie (zie Corticosteroïdinjectie).
- Overweeg verwijzing naar een algemeen, plastisch of orthopedisch chirurg (afhankelijk van de lokale afspraken) alleen bij:
- triggervinger met duidelijke functionele beperkingen, indien corticosteroïdinjectie niet het gewenste resultaat oplevert of niet gewenst is
- gefixeerde triggervinger (graad IV) met wens tot correctie
- De operatie bestaat uit release van de A1-pulley (het bandje van de flexorpees ter hoogte van de metacarpus) in een (mini-)open of percutane procedure. Er is geen consensus ten aanzien van de techniek.
- Bespreek de voor- en nadelen:
- recidiefkans ongeveer 5% binnen 6-12 maanden
- risico op complicaties (bloeding, infectie, zenuwschade) ongeveer 13%
Beleid bij contractuur van Dupuytren
Naar Samenvatting ›Voorlichting en advies
Naar Samenvatting ›- Leg uit dat:
- strengvorming in het peesblad van de handpalm zorgt voor het samentrekken hiervan
- de snelheid en ernst van het beloop varieert
- Bespreek dat:
- er geen permanente oplossing is voor deze aandoening
- er geen bewijs is voor de effectiviteit van spalken of injecties in de eerste lijn
Thuisarts
Naar Samenvatting ›Verwijs naar de informatie op thuisarts.nl. De informatie op Thuisarts is gebaseerd op deze NHG-Standaard.
Niet-medicamenteuze en medicamenteuze behandeling
Naar Samenvatting ›Orale medicatie, spalken, fysiotherapie of (corticosteroïd)injecties worden niet aanbevolen vanwege gebrek aan bewijs.
- In 1 systematisch literatuuronderzoek zijn geen onderzoeken van hoge kwaliteit gevonden naar conservatieve behandelmethoden van Dupuytren die ook beschikbaar zijn in de eerste lijn.
- Een ander systematisch literatuuronderzoek naar conservatieve therapie bij vroege Dupuytren (contracturen < 30°) includeerde onderzoeken van lagere kwaliteit en vond 11 vooral (zeer) oude onderzoeken naar medicamenteuze therapie en 5 onderzoeken naar fysiotherapie. De zeer lage kwaliteit van bewijs, kleine patiëntenaantallen en heterogeniteit van de onderzoeken met betrekking tot patiënten, interventies en uitkomstmaten maken uitspraken over de effectiviteit onmogelijk.
Conclusie
Er is geen bewijs van voldoende kwaliteit voor orale medicatie, injectietherapie of fysiotherapie om een aanbeveling te doen voor toepassing ervan in de eerste lijn.
Controles
Naar Samenvatting ›Nodig patiënten die kiezen voor afwachtend beleid uit om terug te komen indien zij alsnog behandeling wensen.
Consultatie en verwijzing
Naar Samenvatting ›Kaderhuisarts
Naar Samenvatting ›Overweeg overleg met een kaderhuisarts bewegingsapparaat voor advies over diagnostisch onderzoek of beleid (indien regionaal beschikbaar).
Bedrijfsarts
Naar Samenvatting ›Adviseer patiënten contact op te nemen met de bedrijfsarts bij een vermoeden van werkgerelateerde klachten of klachten bij werkzaamheden:
- voor het bespreken van de aard van de behandeling in relatie tot de werkomstandigheden
- voor het bespreken van (tijdelijke) werkaanpassingen
- bij twijfel over behoud van het werk van de patiënt
- voor afstemming van het behandelbeleid en de inzetbaarheid van de patiënt.
Verwijzing voor mogelijke operatieve behandeling
Naar Samenvatting ›- De functionele beperkingen van de patiënt zijn leidend.
- Overweeg verwijzing naar een algemeen, plastisch of orthopedisch chirurg bij een patiënt met een behandelwens en:
- functionele belemmering van de hand door de contractuur (de mate van de MCP-flexiecontractuur is hierbij geen criterium meer)
- snelle progressie van de flexiecontractuur van een vinger (verwijs PIP-contracturen tijdig, omdat deze sneller irreversibel worden door contractuur van het kapsel).
- pijn in hand of vinger
De meest gebruikelijke vormen van operatieve behandeling zijn:
- selectieve fasciëctomie is de gouden standaard vanwege de relatief geringe kans op complicaties en op recidief, maar kent een relatief lange hersteltijd
- percutane naaldfasciotomie is minimaal invasief, maar heeft een hoge recidiefkans
- de plaats en de vergoeding van andere therapeutische opties in de tweede lijn zijn nog onduidelijk.
Beleid bij tendovaginitis van De Quervain
Naar Samenvatting ›Voorlichting en advies
Naar Samenvatting ›- Leg uit dat:
- de pijnklachten ontstaan door irritatie van de pezen van de duim in de smalle peeskoker zodra deze gebruikt of opgerekt worden.
- er weinig gegevens zijn over de prognose; chronische tendinitisklachten (> 3 maanden) reageren doorgaans slechter op behandeling.
- Bespreek:
- de relatie tussen belasting en belastbaarheid
- de mogelijkheden tot aanpassing van de dagelijkse werkzaamheden
- Benadruk dat het belangrijk is de hand en pols binnen de pijngrenzen te blijven gebruiken om onnodige stijfheid te voorkomen
- Geef (slaap)houdingsadviezen en adviseer bewegingen te vermijden die de klachten uitlokken (met name flexie-extensie van de pols met kracht zetten)
Thuisarts
Naar Samenvatting ›Verwijs naar de informatie op thuisarts.nl. De informatie op Thuisarts is gebaseerd op deze NHG-Standaard.
Pijnstilling
Naar Samenvatting ›Adviseer zo nodig pijnmedicatie conform het beleid bij acute nociceptieve pijn in de NHG-Standaard Pijn (paracetamol en/of een (dermaal) NSAID).
Spalkbehandeling of corticosteroïdinjectie
Naar Samenvatting ›Wees terughoudend met het adviseren van een spalkbehandeling of een corticosteroïdinjectie vanwege gebrek aan bewijs. Indien deze behandelingen toch overwogen worden, heeft een combinatiebehandeling de vookeur (advies op basis van consensus in de werkgroep wegens gebrek aan bewijs van voldoende kwaliteit).
Overweeg een spalkbehandeling of een corticosteroïdinjectie bij patiënten bij wie klachten > circa 6 weken bestaan en afwachtend beleid geen effect heeft.
Er zijn 2 recente systematische literatuuronderzoeken verschenen over de effectiviteit van conservatieve behandelingen en corticosteroïdinjecties bij De Quervain.
- Een recent literatuuronderzoek includeerde een cochranereview (van 1 klein onderzoek) en 15 andere individuele RCT’s betreffende de effectiviteit van corticosteroïdinjecties, acupunctuur en spalkbehandeling. Er werden geen onderzoeken gevonden over andere conservatieve interventies. De kwaliteit van de individuele onderzoeken was doorgaans laag door de verschillen in interventies, controlegroepen en uitkomstmaten en follow-upduur. Hierdoor waren de resultaten van de onderzoeken niet samen te voegen. Ook rapporteerden veel onderzoeken niet de duur van de klachten. Chroniciteit van de klachten, complicaties en recidiefpercentages werden doorgaans niet gerapporteerd.
- Het ander recent literatuuronderzoek includeerde 6 onderzoeken (334 patiënten) en vergeleek corticosteroïdinjecties met een (nacht)spalkbehandeling en een gecombineerde injectie/spalkbehandeling. Ook hier was de kwaliteit van bewijs zeer laag.
- Er lijkt geen verschil te zijn in effectiviteit tussen een corticosteroïdinjectie en een spalkbehandeling (3 onderzoeken).
- Een gecombineerde behandeling lijkt een hoger succespercentage te hebben dan een spalkbehandeling alleen (RR 0,53; 95%-BI 0,35 tot 0,80, p < 0,001; 2 onderzoeken) of corticosteroïdinjecties alleen (RR 0,76; 95%-BI 0,64 tot 0,89; p < 0,001; 2 onderzoeken). Het verschil in pijn was wel statistisch, niet klinisch relevant verschillend.
Conclusie
Door gebrek aan bewijs is het onzeker of spalkbehandeling dan wel corticosteroïdinjecties effectief zijn bij tendovaginitis van De Quervain. Mogelijk geeft een gecombineerde behandeling een grotere kans op succes.
Spalkbehandeling
Naar Samenvatting ›- Overweeg een spalkbehandeling bij patiënten met belastingafhankelijke klachten en een voorkeur voor deze behandeling.
- Gebruik tijdens de nacht is in principe niet nodig.
- Zie Praktische aanwijzingen orthesen bij hand- en polsklachten.
Bij keuze voor corticosteroïdinjectie
Naar Samenvatting ›- Gebruik als eerste keuze op basis van praktische overwegingen 10 mg triamcinolonacetonide 10 mg/ml (zie tabel 3).
- Gelijkwaardige alternatieven zijn:
- 2 mg dexamethason 4 mg/ml
- 20 mg methylprednisolon 40 mg/ml.
Controles
Naar Samenvatting ›Controleer het effect van de behandeling na ongeveer 4-6 weken, of eerder bij toename van klachten of aanwijzingen voor complicaties.
Controle na spalkbehandeling
Naar Samenvatting ›- Stop een spalkbehandeling indien het dragen van de spalk na 4-6 weken niet leidt tot een vermindering van de klachten.
- Probeer de spalk bij goed effect op geleide van klachten af te bouwen.
- bouw de spalk bij belastende momenten als laatste af.
- heroverweeg de gekozen behandeling (of de diagnose) indien het afbouwen niet succesvol is.
Controle na corticosteroïdinjectie
Naar Samenvatting ›- Indien de injectie geen effect heeft, overweeg dan een alternatieve diagnose, incorrecte techniek of non-respons van de patiënt.
- Geef eventueel eenmalig nogmaals een corticosteroïdinjectie.
- Indien de klachten recidiveren, herhaal de injectie dan alleen als het effect duidelijk aanwezig en langdurig was, en niet eerder dan 3-6 maanden na de laatste injectie.
Consultatie en verwijzing
Naar Samenvatting ›- Overweeg verwijzing naar een handtherapeut (zie Handtherapie):
- bij twijfel over het gebruik en de keuze van de spalk
- als een bestaande spalk goed effect heeft, maar oncomfortabel is
- Overweeg verwijzing naar een algemeen, orthopedisch of plastisch chirurg (afhankelijk van de lokale afspraken) bij onvoldoende resultaat van conservatieve behandeling; de operatie bestaat uit endoscopische of open release van het peescompartiment
- Overweeg consultatie van een kaderhuisarts bewegingsapparaat voor advies over diagnostisch onderzoek of beleid (indien regionaal beschikbaar).
Bedrijfsarts
Naar Samenvatting ›Adviseer patiënten contact op te nemen met de bedrijfsarts bij een vermoeden van werkgerelateerde klachten of klachten bij werkzaamheden:
- voor het bespreken van de aard van de behandeling in relatie tot de werkomstandigheden
- voor het bespreken van (tijdelijke) werkaanpassingen
- bij twijfel over behoud van het werk van de patiënt
- voor afstemming van het behandelbeleid en de inzetbaarheid van de patiënt.
Beleid bij traumatische klachten
Naar Samenvatting ›Voorlichting en advies
Naar Samenvatting ›- Adviseer in afwachting van verdere diagnostiek de hand hoog te houden en te ontzien, maar hand en pols binnen de pijngrenzen wel te blijven gebruiken om onnodige stijfheid te voorkomen
- Geef zo nodig een mitella.
Pijnstilling
Naar Samenvatting ›Adviseer zo nodig pijnmedicatie conform het beleid bij acute nociceptieve pijn in de NHG-Standaard Pijn (paracetamol en/of een (dermaal) NSAID).
Consultatie en verwijzing
Naar Samenvatting ›Tweede lijn
Naar Samenvatting ›Verwijs, gezien het risico op blijvende schade, altijd bij acuut letsel met een vermoeden van:
- pees- of zenuwletsel
- intra-articulaire fracturen
- (sub)luxaties
- skiduim
- jersey finger
Kies bij vermoeden van een fractuur, afhankelijk van de regionale samenwerkingsafspraken, voor:
- directe doorverwijzing naar Spoedeisende Hulp of specialist voor diagnostiek en beleid
- verwijzing naar een afdeling Radiologie voor röntgenonderzoek:
- indien er geen aanwijzingen gevonden worden voor fractuur of (sub)luxatie zal de patiënt worden terugverwezen naar de huisarts
- bij een fractuur of (sub)luxatie zal de patiënt worden doorverwezen naar de Spoedeisende Hulp of betreffende specialist
- vermeld bij de verwijzing in ieder geval tijdstip en aard van het trauma(mechanisme); de locatie van de klachten en eventueel relevant eerder trauma aan de betreffende hand of pols
Handtherapie
Naar Samenvatting ›Overweeg verwijzing voor handtherapie bij een patiënt met vertraagd herstel:
- die behoefte heeft aan ondersteuning in het uitbreiden van de belastbaarheid
- wiens hulpvraag vooral betrekking heeft op functionele beperkingen zonder dat er redenen zijn om direct terug te verwijzen naar de operateur of behandelaar (zoals twijfel over de diagnose of vermoeden van complicaties).
Chronische posttraumatische klachten
Naar Samenvatting ›- Overweeg consultatie van of verwijzing naar de (behandelend) chirurg bij:
- afwijkend beloop van het herstel (eventueel na consultatie van een handtherapeut).
- vermoeden van bijkomend letsel, zoals instabiliteit door ligamentair letsel.
- Het herstel van fracturen en gewrichtsletsels in de hand duurt vaak langer dan gedacht en er is een aanzienlijk risico op blijvende standafwijkingen, stijfheid en functionele beperkingen, met name bij een te late of onjuiste diagnose en/of behandeling.
Beleid bij malletvinger
Naar Samenvatting ›Voorlichting en advies
Naar Samenvatting ›- Leg uit dat er een ruptuur is van de strekpees van de vinger, die ervoor zorgt dat de vinger niet meer kan strekken.
- Leg uit dat de aandoening zonder behandeling blijft bestaan en dat er een kans is op functionele beperkingen van de vinger.
- Benadruk dat een malletspalk in de eerste fase constant gedragen moet worden; tussentijds testen van de functie (door de arts of de patiënt zelf) kan het effect van de spalk tenietdoen.
Thuisarts
Naar Samenvatting ›Verwijs naar de informatie op thuisarts.nl. De informatie op Thuisarts is gebaseerd op deze NHG-Standaard.
Spalkbehandeling
Naar Samenvatting ›Gebruik het onderstaande behandelschema voor een tendinogene malletvinger of malletvinger met kleine avulsiefractuur.
Behandelschema
Naar Samenvatting ›- Fase 1: instrueer de patiënt de malletspalk 24 uur per dag te dragen gedurende 6-8 weken
- Fase 2: verricht na 6-8 weken controle
- bij volledige extensie in het DIP-gewricht: laat de patiënt de spalk 2 weken continueren, maar starten met oefenen (gradueel opbouwen van buigen en strekken; dit is het enige moment waarop de spalk af mag)
- bij onvolledige extensie in het DIP-gewricht: laat de spalk nog 4 weken continueren
- Fase 3:
- laat de patiënt doorgaan (of starten) met gradueel opbouwen van buigen en strekken
- instrueer de patiënt de malletspalk nog 2-4 weken ’s nachts en tijdens risicomomenten (sport) te dragen
- Na 12 weken is de vinger weer volledig belastbaar.
Praktische aanwijzingen
Naar Samenvatting ›- Het doel van de malletspalk is het verkrijgen van volledige extensie of hyperextensie in het DIP-gewricht.
- Zorg voor een adequaat sluitende spalk, zo nodig op maat gemaakt, bij voorkeur een geperforeerde thermoplastische spalk.
- Breng bij het aanleggen van de spalk het DIP-gewricht goed in extensie en zorg dat het PIP-gewricht vrij kan bewegen.
- Geef de patiënt verzorginstructies (niet nat laten worden, regelmatig (bijvoorbeeld om de dag) spalk reinigen en huid drogen, verder het afdoen tot een minimum beperken, vinger niet buigen).
Klachten bij een malletspalk komen vaak voor. Adequate aanmeting, goede adviezen en controle van de huid (en de therapietrouw) zijn daarom belangrijk. Er zijn diverse materialen beschikbaar. Geperforeerde thermoplastische spalken worden beter verdragen en geven minder huidcomplicaties dan aluminium spalken en voorgevormde plastic spalken (stackspalken). Er is geen verschil in effectiviteit.
Pijnstilling
Naar Samenvatting ›Adviseer zo nodig pijnmedicatie conform het beleid bij acute nociceptieve pijn in de NHG-Standaard Pijn (paracetamol en/of een (dermaal) NSAID).
Controles
Naar Samenvatting ›- Controleer de eerste 6-8 weken regelmatig de sluiting van de spalk, de onderliggende huid en de therapietrouw.
- Beoordeel na 6-8 weken of volledige extensie wel of niet mogelijk is, en zet verder beleid in (zie Behandelschema).
- Bij volledige extensie: controleer nadien alleen zo nodig.
- Bij onvolledige extensie: beoordeel na 4 weken opnieuw.
Consultatie en verwijzing
Naar Samenvatting ›Verwijzing voor mogelijke operatieve behandeling
Naar Samenvatting ›- Verwijs naar een trauma-, plastisch of orthopedisch chirurg (afhankelijk van de lokale afspraken) indien de avulsiefractuur > 30% van het gewrichtsoppervlak van het DIP-gewricht beslaat.
- Zorg, indien röntgendiagnostiek uitgesteld heeft plaatsgevonden en er een verwijsindicatie blijkt te bestaan, voor direct overleg met de tweede lijn om (operatieve) behandelvertraging te voorkomen.
- Overweeg consultatie van of verwijzing naar een trauma-, plastisch of orthopedisch chirurg (afhankelijk van de lokale afspraken) wanneer na mislukte spalktherapie een chronische malletvinger ontstaat met:
- functionele klachten, of
- verlies van extensie > 40°
- Een gefixeerde flexiecontractuur kan doorgaans niet meer functioneel worden gecorrigeerd, hierbij kan artrodese in een functionele stand een alternatief zijn.
Handtherapie
Naar Samenvatting ›Overweeg verwijzing naar een handtherapeut:
- voor het aanmeten van een spalk bij twijfel over adequate pasvorm en goed gebruik van de spalk
- voor begeleiding als zelfstandig oefenen niet haalbaar is, indien de patiënt daar behoefte aan heeft of wanneer het herstel stagneert.
Referenties
- NVPC. Richtlijn Ziekte van Dupuytren. Utrecht: Nederlandse Vereniging van Plastische Chirurgie, 2010. https://richtlijnendatabase.nl, geraadpleegd april 2020. Ga naar bron: NVPC. Richtlijn Ziekte van Dupuytren. Utrecht: Nederlandse Vereniging van Plastische Chirurgie, 2010. https://richtlijnendatabase.nl, geraadpleegd april 2020.
- NVAB. Handelen van de bedrijfsarts bij werknemers met klachten aan arm, schouder of nek. Utrecht: Nederlandse Vereniging voor Arbeids- en Bedrijfsgeneeskunde, 2014. https://nvab-online.nl, geraadpleegd april 2020. Ga naar bron: NVAB. Handelen van de bedrijfsarts bij werknemers met klachten aan arm, schouder of nek. Utrecht: Nederlandse Vereniging voor Arbeids- en Bedrijfsgeneeskunde, 2014. https://nvab-online.nl, geraadpleegd april 2020.
- NVPC. Primaire artrose van de duimbasis. Utrecht: Nederlandse Vereniging van Plastische Chirurgie, 2015. https://richtlijnendatabase.nl, geraadpleegd april 2020. Ga naar bron: NVPC. Primaire artrose van de duimbasis. Utrecht: Nederlandse Vereniging van Plastische Chirurgie, 2015. https://richtlijnendatabase.nl, geraadpleegd april 2020.
- NVN. Richtlijn Carpaletunnelsyndroom. Utrecht: Nederlandse Vereniging voor Neurologie, 2017. https://richtlijnendatabase.nl, geraadpleegd april 2020. Ga naar bron: NVN. Richtlijn Carpaletunnelsyndroom. Utrecht: Nederlandse Vereniging voor Neurologie, 2017. https://richtlijnendatabase.nl, geraadpleegd april 2020.
- NVvH/NVPC. Richtlijn handfracturen. Utrecht: Nederlandse Vereniging voor Heelkunde/Nederlandse Vereniging van Plastische Chirurgie, 2018. https://richtlijnendatabase.nl, geraadpleegd april 2020. Ga naar bron: NVvH/NVPC. Richtlijn handfracturen. Utrecht: Nederlandse Vereniging voor Heelkunde/Nederlandse Vereniging van Plastische Chirurgie, 2018. https://richtlijnendatabase.nl, geraadpleegd april 2020.
- WHO. International classification of functioning, disability and health (ICF). Geneva: WHO, 2001. www.who.int, geraadpleegd april 2020. Ga naar bron: WHO. International classification of functioning, disability and health (ICF). Geneva: WHO, 2001. www.who.int, geraadpleegd april 2020.
- NICE. Guideline Osteoarthritis: care and management (2014). National institute for health and care excellence. www.nice.org.uk/guidance/cg177, geraadpleegd april 2020. Ga naar bron: NICE. Guideline Osteoarthritis: care and management (2014). National institute for health and care excellence. www.nice.org.uk/guidance/cg177, geraadpleegd april 2020.
- Picavet HS, Schouten JS. Musculoskeletal pain in the Netherlands: prevalences, consequences and risk groups, the DMC(3)-study. Pain 2003;102:167-78.
- Nielen MM, Hek K, Schermer TR. Jaarcijfers aandoeningen: incidenties en prevalenties. Utrecht: Nivel Zorgregistraties Eerste Lijn, 2019. www.nivel.nl, geraadpleegd 11 december 2019. Ga naar bron: Nielen MM, Hek K, Schermer TR. Jaarcijfers aandoeningen: incidenties en prevalenties. Utrecht: Nivel Zorgregistraties Eerste Lijn, 2019. www.nivel.nl, geraadpleegd 11 december 2019.
- Bot SD, Van der Waal JM, Terwee CB, Van der Windt DA, Schellevis FG, Bouter LM, et al. Incidence and prevalence of complaints of the neck and upper extremity in general practice. Ann Rheum Dis 2005;64:118-23.
- Spahn G, Wollny J, Hartmann B, Schiele R, Hofmann GO. Metaanalyse zur Bestimmung von Risikofaktoren für das Karpaltunnelsyndrom (KTS), Teil II: Berufliche Risikofaktoren. Z Orthop Unfall 2012;150:516-24.
- Meems M, Truijens SE, Spek V, Visser LH, Pop VJ. Prevalence, course and determinants of carpal tunnel syndrome symptoms during pregnancy: a prospective study. BJOG 2015;122:1112-18.
- De Krom MC, Van Croonenborg JJ, Blaauw G, Scholten RJ, Spaans F. Richtlijn Diagnostiek en behandeling van het carpale-tunnelsyndroom. Ned Tijdschr Geneeskd 2008;152:76-81.
- Palmer KT, Harris EC, Coggon D. Carpal tunnel syndrome and its relation to occupation: a systematic literature review. Occup Med 2007;57:57-66.
- Osterman M, Ilyas AM, Matzon JL. Carpal tunnel syndrome in pregnancy. Orthop Clin North Am 2012;43:515-20.
- Padua L, Coraci D, Erra C, Pazzaglia C, Paolasso I, Loreti C, et al. Carpal tunnel syndrome: clinical features, diagnosis, and management. Lancet Neurol 2016;15:1273-84.
- Shiri R. Arthritis as a risk factor for carpal tunnel syndrome: a meta-analysis. Scand J Rheumatol 2016;45:339‐46.
- Manente G, Torrieri F, Di Blasio F, Staniscia T, Romano F, Uncini A. An innovative hand brace for carpal tunnel syndrome: a randomized controlled trial. Muscle Nerve 2001;24:1020-5.
- Ortiz-Corredor F, Enríquez F, Díaz-Ruíz J, Calambas N. Natural evolution of carpal tunnel syndrome in untreated patients. Clin Neurophysiol 2008;119:1373‐8.
- Burton CL, Chesterton LS, Chen Y, Van der Windt DA. Clinical course and prognostic factors in onservatively managed carpal tunnel syndrome: a systematic Review. Arch Phys Med Rehabil 2016;97:836-52.
- Padua L, Aprile I, Caliandro P, Carboni T, Meloni A, Massi S, et al. Symptoms and neurophysiological picture of carpal tunnel syndrome in pregnancy. Clin Neurophysiol 2001;112:1946-51.
- Padua L, Aprile I, Caliandro P, Mondelli M, Pasqualetti P, Tonali PA. Carpal tunnel syndrome in pregnancy: multiperspective follow-up of untreated cases. Neurology 2002;59:1643-6.
- Mondelli M, Rossi S, Monti E, Aprile I, Caliandro P, Pazzaglia C, et al. Long term follow-up of carpal tunnel syndrome during pregnancy: a cohort study and review of the literature. Electromyogr Clin Neurophysiol 2007;47:259-71.
- Sax TW, Rosenbaum RB. Neuromuscular disorders in pregnancy. Muscle Nerve 2006;34:559‐71.
- Head L, Gencarelli JR, Allen M, Boyd KU. Wrist ganglion treatment: systematic review and meta-analysis. J Hand Surg Am 2015;40:546-53.
- Gude W, Morelli V. Ganglion cysts of the wrist: pathophysiology, clinical picture, and management. Curr Rev Musculoskelet Med 2008;1:205-11.
- Watson HK, Rogers WD, Ashmead D. Reevaluation of the cause of the wrist ganglion. J Hand Surg Am 1989;14:812-7.
- Burke FD, Melikyan EY, Bradley MJ, Dias JJ. Primary care referral protocol for wrist ganglia. Postgrad Med J 2003;79(932):329-31.
- Psaila JV, Mansel RE. The surface ultrastructure of ganglia. J Bone Joint Surg Br 1978;60-B:228‐33.
- Dias JJ, Buch K. Palmar wrist ganglion: Does intervention improve outcome: a prospective study of the natural history and patient-reported treatment outcomes. J Hand Surg Am 2003;28:172-6.
- Dias JJ, Dhukaram V, Kumar P. The natural history of untreated dorsal wrist ganglia and patient reported outcome 6 years after intervention. J. Hand Sur Eur 2007;32:502-8.
- Dahaghin S, Bierma-Zeinstra SM, Reijman M, Pols HA, Hazes JM, Koes BW. Prevalence and determinants of one month hand pain and hand related disability in the elderly (Rotterdam study). Ann Rheum Dis 2005;64:99-104.
- Yu D, Peat G, Bedson J, Jordan KP. Annual consultation incidence of osteoarthritis estimated from population-based health care data in England. Rheumatol 2015;54:2051-60.
- Wilder FV, Barrett JP, Farina EJ. Joint-specific prevalence of osteoarthritis of the hand. Osteoarthritis Cartilage 2006;14:953-7.
- Zhang Y, Jordan JM. Epidemiology of osteoarthritis. Rheum Dis Clin North Am 2008;34:515-29.
- Mannoni A, Briganti MP, Di Bari M, et al. Prevalence of symptomatic hand osteoarthritis in community-dwelling older persons: the ICARe Dicomano study. Insufficienza Cardiaca negli Anzizni Residenti a Dicomano. Osteoarthritis Cartilage 2000;8:S11-3.
- Dillon CF, Hirsch R, Rasch EK, Gu Q. Symptomatic hand osteoarthritis in the United States: prevalence and functional impairment estimates from the third U.S. National Health and Nutrition Examination Survey, 1991-1994. Am J Phys Med Rehabil 2007;86:12-21.
- Peffers MJ, Balaskas P, Smagul A. Osteoarthritis year in review 2017: genetics and epigenetics. Osteoarthritis Cartilage 2018;26:304-11.
- Qin J, Barbour KE, Murphy LB, et al. Lifetime risk of symptomatic hand osteoarthritis: the Johnston County Osteoarthritis Project. Arthritis Rheumatol 2017;69:1204-12.
- Visser AW, Ioan-Facsinay A, De Mutsert R, et al. Adiposity and hand osteoarthritis: the Netherlands Epidemiology of Obesity study. Arthritis Res Ther 2014;16:R19.
- Harris PA, Hart DJ, Dacre JE, Huskisson EC, Spector TD. The progression of radiological hand osteoarthritis over ten years: a clinical follow-up study. Osteoarthritis Cartilage 1994;2:247-52.
- Botha-Scheepers S, Riyazi N, Watt I, Rosendaal FR, Slagboom E, Bellamy N, et al. Progression of hand osteoarthritis over two years: a clinical and radiological follow-up study. Ann Rheum Dis 2009;68:1260-4.
- Cvijetic S, Kurtagic N, Ozegovic DD. Osteoarthritis of the hands in the rural population: a follow-up study. Eur J Epidemiol 2004;19:687-91.
- Kwok WY, Vliet Vlieland TP, Rosendaal FR, Huizinga TW, Kloppenburg M. Limitations in daily activities are the major determinant of reduced health-related quality of life in patients with hand osteoarthritis. Ann Rheum Dis 2011;70:334-6.
- Hoogendam L, Van der Oest MJ, Tsehaie J, Wouters RM, Vermeulen GM, Slijper HP, et al.; Hand-Wrist Study Group. Psychological factors are more strongly associated with pain than radiographic severity in non-invasively treated first carpometacarpal osteoarthritis. Disabil Rehabil 2019 Nov 8:1-6.
- Weilby A. Triggervinger: Incidence in children and adults and the possibility of a predisposition in certain age groups. Acta Orthop Scand 1970;41:419-27.
- Grandizio LC, Beck JD, Rutter MR, Graham J, Klena JC. The incidence of trigger digit after carpal tunnel release in diabetic and nondiabetic patients. J Hand Surg Am 2014;39:280-5.
- Ota H, Iwatsuki K, Kurimoto S, Iida K, Hirata H. Progression from Injection to surgery for triggervinger: a statistical analysis. J Hand Surg Asian Pac 2017;22:194-9.
- Moore JS. Flexor tendon entrapment of the digits (triggervinger and trigger thumb). J Occup Environ Med 2000;42:526-45.
- Flatt AE. Notta's nodules and trigger digits. Proc (Bayl Univ Med Cent) 2007;20:143-5.
- Sempowski IP. The management of the occasional triggervinger. Can J Rural Med 2008;13:136-8.
- Ryzewicz M, Wolf JM. Trigger digits: principles, management, and complications. J Hand Surg Am 2006;31:135-46.
- Bauer AS, Bae DS. Pediatric trigger digits. J Hand Surg Am 2015;40:2304-9.
- Trezies AJ, Lyons AR, Fielding K, Davis TR. Is occupation an aetiological factor in the development of trigger finger? J Hand Surg Br 1998;23:539-40.
- Drossos K, Remmelink M, Nagy N, de Maertelaer V, Pasteels JL, Schuind F. Correlations between clinical presentations of adult trigger digits and histologic aspects of the A1 pulley. J Hand Surg Am 2009;34:1429-35.
- Lundin AC, Eliasson P, Aspenberg P. Triggervinger and tendinosis. J Hand Surg Eur 2012;37:233-6.
- Kumar P, Chakrabarti I. Idiopathic carpal tunnel syndrome and triggervinger: is there an association? J Hand Surg Eur 2009;34:58-9.
- Griggs SM, Weiss AP, Lane LB, Schwenker C, Akelman E, Sachar K. Treatment of triggervinger in patients with diabetes mellitus. J Hand Surg Am 1995;20:787-9.
- De la Parra-Marquez ML, Tamez-Cavazos R, Zertuche-Cedillo L, Martinez-Perez JJ, Velasco-Rodriguez V, Cisneros-Perez V. Factores de riesgo asociados a tenosinovitisestenosante. Estudio de casos y controles. Cir Cir 2008;76:317-21.
- Brozovich N, Agrawal D, Reddy G. A critical appraisal of adult triggervinger: pathophysiology, treatment, and future outlook. Plast Reconstr Surg Glob Open 2019;7:e2360.
- Lapidus PW, Fenton R. Stenosing tenovaginitis at the wrist and fingers; report of 423 cases in 369 patients with 354 operations. AMA Arch Surg 1952;64:475-87.
- Lapidus PW. Stenosing tenovaginitis. Surg Clin North Am 1953;1317-47.
- Bayat A, McGrouther DA. Management of Dupuytren's disease-clear advice for an elusive condition. Ann R Coll Surg Engl 2006;88:3-8.
- Lanting R, Van den Heuvel ER, Westerink B, Werker PM. Prevalence of dupuytren disease in the Netherlands. Plast Reconstr Surg 2013;132:394-403.
- Gudmundsson KG, Arngrimsson R, Sigfusson N, Bjornsson A, Jonsson T. Epidemiology of Dupuytren's disease: clinical, serological, and social assessment. The Reykjavik study. J Clin Epidemiol 2000;53:291-6.
- Townley WA, Baker R, Sheppard N, Grobbelaar AO. Dupuytren's contracture unfolded. BMJ 2006;332:397-400.
- Benson LS, Williams CS, Kahle M. Dupuytren's contracture. J Am Acad Orthop Surg 1998;6:24-35.
- Burge P. Genetics of Dupuytren's disease. Hand Clin 1999;15:63-71.
- Rayan GM. Dupuytren disease: anatomy, pathology, presentation, and treatment. J Bone Joint Surg Am 2007;89:189-98.
- Dolmans GH, Werker PM, Hennies HC, et al. Wnt signaling and Dupuytren's disease. N Engl J Med 2011;365:307-17.
- Nugteren, H, Nijman, J, De Jong, I, et al. The association between Peyronie's and Dupuytren's disease. Int J Impot Res 2011:142-5.
- Grazina R, Teixeira S, Ramos R, Sousa H, Ferreira A, Lemos R. Dupuytren’s disease: where do we stand? EFORT Open Rev 2019;4:63-9.
- Hindocha S. Risk factors, disease associations, and Dupuytren diathesis. Hand Clin 2018;34:307-14.
- Walker-Bone K, Palmer KT, Reading I, Coggon D, Cooper C. Prevalence and impact of musculoskeletal disorders of the upper limb in the general population. Arthritis Rheum 2004;51:642-51.
- Moore JS. De Quervain's tenosynovitis. Stenosing tenosynovitis of the first dorsal compartment. J Occup Environ Med 1997;39:990-1002.
- Clarke MT, Lyall HA, Grant JW, Matthewson MH. The histopathology of de Quervain's disease. J Hand Surg Br 1998;23:732-4.
- Stahl S, Vida D, Meisner C, Stahl AS, Schaller HE, Held M. Work related etiology of de Quervain’s tenosynovitis: a case-control study with prospectively collected data pathophysiology of musculoskeletal disorders. BMC Musculoskelet Disord 2015;16:1-10.
- Petit Le Manac'h A, Roquelaure Y, Ha C, Bodin J, Meyer G, Bigot F, et al. Risk factors for de Quervain's disease in a French working population. Scand J Work Environ Health 2011;37:394-401.
- Doyle, JR. Extensor tendons: acute injuries. In: Green, DP, Pederson, CW, Hotchkiss, RN, editors. Green’s operative hand surgery. 4th ed. New York, NY: Churchill Livingstone, 1999. p. 195-8.
- Handoll HH, Vaghela MV. Interventions for treating mallet finger injuries. Cochrane Database Syst Rev 2004:CD004574.
- Rockwell WB, Butler PN, Byrne BA. Extensor tendon: anatomy, injury, and reconstruction. Plast Reconstr Surg 2000;106:1592-1673.
- Myers H, Thomas E, Dziedzic K. What are the important components of the clinical assessment of hand problems in older adults in primary care? Results of a Delphi study. BMC Musculoskelet Disord 2010;11:178.
- Newton AW, Hawkes DH, Bhalaik V. Clinical examination of the wrist. Orthop Trauma 2017;31:237-47.
- Rainbow MJ, Kamal RN, Moore DC, Akelman E, Wolfe SW, Crisco JJ. Subject-specific carpal ligament elongation in extreme positions, grip, and the dart trower's motion. J Biomech Eng 2015;137:111006.
- Stevens JC, Smith BE, Weaver AL, Bosch EP, Deen HG Jr, Wilkens JA. Symptoms of 100 patients with electromyographically verified carpal tunnel syndrome. Muscle Nerve 1999;22:1448-56.
- Gupta SK, Benstead TJ. Symptoms experienced by patients with carpal tunnel syndrome. Can J Neurol Sci 1997;24: 338-42.
- Burton C, Chesterton LS, Davenport G. Diagnosing and managing carpal tunnel syndrome in primary care. Br J Gen Pract 2014;64:262-3.
- De Krom MC, Kester AD, Knipschild PG, Spaans F. Risk factors for carpal tunnel syndrome. Am J Epidemiol 1990;132:1102-10.
- Katz JN, Larson MG, Sabra A, Krarup C, Stirrat CR, Sethi R, et al. The carpal tunnel syndrome: diagnostic utility of the history and physical examination findings. Ann Intern Med 1990;112:321-7.
- Valdes K, Lastayo P. The value of provocative tests for the wrist and elbow: a literature review. J Hand Ther 2013;26:32-43.
- Jaeschke R, Guyatt GH, Sackett DL. Users' guides to the medical literature. III. How to use an article about a diagnostic test. B. What are the results and will they help me in caring for my patients? The Evidence-Based Medicine Working Group. JAMA 1994;271:703-7.
- Phalen GS, Gardner WJ, La londe AA. Neuropathy of the median nerve due to compression beneath the transverse carpal ligament. J Bone Joint Surg Am 1950;32A:109-12.
- Tinel, J. Le signe du fourmillement dans les lésions des nerfs périphériques. Presse Médicale 1915;47:388-9.
- Graham B, Regehr G, Naglie G, Wright JG. Development and validation of diagnostic criteria for carpal tunnel syndrome. J Hand Surg Am 2006;31:919.
- Claes F, Bernsen H, Meulstee J, Verhagen WI. Carpal tunnel syndrome diagnosed by general practitioners: an observational study. Neurol Sci 2012;33:1079-81.
- Jordan R, Carter T, Cummins C. A systematic review of the utility of electrodiagnostic testing in carpal tunnel syndrome. Br J Gen Pract 2002;52:670-73.
- Martić V. Concordance of clinical and neurophysiologic diagnoses of carpal tunnel syndrome. Vojnosanit Pregl 2015;72:247-50.
- Burke FD, Bradley MJ. A proposal justifying an alternative referral practice from primary care for three common hand surgery diagnoses. Postgrad Med J 2007;83:616-7.
- Minotti P, Taras JS. Ganglion cysts of the wrist. J Am Soc Surg Hand 2002;2:102-7.
- Wright TW, Cooney WP, Ilstrup DM. Anterior wrist ganglion. J Hand Surg Am 1994;19:954-8.
- Greendyke SD, Wilson M, Shepler TR. Anterior wrist ganglia from the scaphotrapezial joint. J Hand Surg Am 1992;17:487-90.
- Pomerance JF. Painful basal joint arthritis of the thumb, Part I: anatomy, pathophysiology, and diagnosis. Am J Orthop 1995;24:401-8.
- Glickel SZ. Clinical assessment of the thumb trapeziometacarpal joint. Hand Clin 2001;17:185-95.
- Poole JU, Pellegrini VD Jr. Arthritis of the thumb basal joint complex. J Hand Ther 2000;13:91-107.
- Merritt MM, Roddey TS, Costello C, Olson S. Diagnostic value of clinical grind test for carpometacarpal osteoarthritis of the thumb. J Hand Ther 2010;23:261-8.
- Burton RI. Basal joint arthrosis of the thumb. Orthop Clin North Am 1973;4:331-8.
- Quinell RC. Conservative management of triggervinger. Practitioner 1980;224:187-90.
- Tubiana R, Michon J, Thomine JM. Scheme for the assessment of deformities in Dupuytren's disease. Surg Clin North Am 1968;48:979-84.
- Iselin M. Chirurgie der Hand. Vol. 1. Stuttgart: Thieme, 1965.
- Hueston JT. A simple test is described for the selection of patients with Dupuytren’ s contracture, for operation. Hand 1982;14:100-3.
- Goubau JF, Goubau L, Van Tongel A, Van Hoonacker P, Kerckhove D, Berghs B. The wrist hyperflexion and abduction of the thumb (WHAT) test: a more specific and sensitive test to diagnose de Quervain tenosynovitis than the Eichhoff’s Test. J Hand Surg Eur 2014;39:286-92.
- Wu F, Rajpura A, Sandher D. Finkelstein’s test is superior to Eichhoff’s test in the investigation of de Quervain’s disease. J. Hand Microsurg 2018;10:116-8.
- Eichhoff E. Zur pathogenese der tendovaginitis stenosans. Bruns Beit Klin Chir 1927;CXXXIX:746-55.
- Finkelstein H. Stenosing tendovaginitis of the radial styloid process. JBJS 1930;12:509-40.
- Brunelli G. Le test de Finkelstein contre le test de Brunelli dans la tenosynovite de De Quervain. Chir Main 2003;22:43-5.
- Elliott BG. Finkelstein's test: a descriptive error that can produce a false positive. J Hand Surg Br 1992;17:481-2.
- Chesterton LS, Blagojevic-Bucknall M, Burton C, Dziedzic KS, Davenport G, et al. The clinical and cost-effectiveness of corticosteroid injection versus night splints for carpal tunnel syndrome (INSTINCTS trial): an open-label, parallel group, randomised controlled trial. Lancet 2018;392:1423-33.
- Jiménez del Barrio S, Bueno Gracia E, Hidalgo García C, Estébanez de Miguel E, Tricás Moreno JM, Rodríguez Marco S, et al. Conservative treatment in patients with mild to moderate carpal tunnel syndrome: a systematic review. Neurologia 2018;33:590-601.
- Page M, Massy-Westropp N, O’Connor D, Pitt V. Splinting for carpal tunnel syndrome. Cochrane Database Syst Rev 2012:CD010003.
- So H, Chung VC, Cheng JCK, Yip RM. Local steroid injection versus wrist splinting for carpal tunnel syndrome: a randomized clinical trial. Int J Rheum Dis 2018;21:102-7.
- Celiker R, Arslan S, Inanici F. Corticosteroid injection versus nonsteroidal antiinflammatory drug and splinting in carpal tunnel syndrome. Am J Phys Med Rehabil 2002;81:182-6.
- De Kleermaeker FG, Boogaarts HD, Meulstee J, Verhagen WI. Minimal clinically important difference for the Boston Carpal Tunnel Questionnaire: new insights and review of literature. J Hand Surg Eur 2019;44:283-9.
- Huisstede BM, Hoogvliet P, Randsdorp MS, Glerum S, Van Middelkoop M, Koes BW. Carpal tunnel syndrome, Part I: effectiveness of nonsurgical treatments-a systematic review. Arch Phys Med Rehabil 2010;91:981-1004.
- Premoselli S, Sioli P, Grossi A, Cerri C. Neutral wrist splinting in carpal tunnel syndrome: a 3- and 6-month clinical and neurophysiologic follow-up evaluation of night-only splint therapy. Eura Medicophys 2006;42:121-6.
- Nobuta S, Sato K, Nakagawa T, Hatori M, Itoi E. Effects of wrist splinting for carpal tunnel syndrome and motor nerve conduction measurements. Ups J Med Sci 2008;113:181-92.
- Chen PC, Chuang CH, Tu YK, Bai CH, Chen CF, Liaw M. A Bayesian network meta-analysis: comparing the clinical effectiveness of local corticosteroid injections using different treatment strategies for carpal tunnel syndrome. BMC Musculoskelet Disord 2015;16:363.
- Jenkins PJ, Duckworth AD, Watts AC, McEachan JE. Corticosteroid injection for carpal tunnel syndrome: a 5-year survivorship analysis. Hand 2012;7:151-6.
- Dammers JW, Veering MM, Vermeulen M. Injection with methylprednisolone proximal to the carpal tunnel: randomised double blind trial. BMJ 1999;319:884-6.
- O'Gradaigh D, Merry P. Corticosteroid injection for the treatment of carpal tunnel syndrome. Ann Rheum Dis 2000;59:918-9.
- Armstrong T, Devor W, Borschel L, Contreras R. Intracarpal steroid injection is safe and effective for short-term management of carpal tunnel syndrome. Muscle Nerve 2004;29:82-8.
- Peters-Veluthamaningal C, Winters JC, Groenier KH, Meyboom-de Jong B. Randomised controlled trial of local corticosteroid injections for carpal tunnel syndrome in general practice. BMC Fam Pract. 2010 Jul 29;11:54.
- Karadaş Ö, Tok F, Akarsu S, Tekin L, Balaban B. Triamcinolone acetonide vs procaine hydrochloride injection in the management of carpal tunnel syndrome: randomized placebo-controlled study. J Rehabil Med. 2012 Jun;44:601-4.
- Atroshi I, Flondell M, Hofer M, Ranstam J. Methylprednisolone injections for the carpal tunnel syndrome: a randomized, placebo-controlled trial. Ann Intern Med 2013;159:309-17.
- Karimzadeh A, Bagheri S, Raeissadat SA, et al. The comparison of the effectiveness between different doses of local methylprednisolone injection versus triamcinolone in carpal tunnel syndrome: a double-blind clinical trial. J Pain Res 2019;12:579-84.
- KNMP Kennisbank, geraadpleegd op 10 oktober 2023.
- Ring D, Lozano-Calderón S, Shin R, Bastian P, Mudgal C, Jupiter J. A prospective randomized controlled trial of injection of dexamethasone versus triamcinolone for idiopathic triggervinger. J Hand Surg Am 2008;33:516-524.
- Geneesmiddeleninformatiebank. Utrecht: College ter Beoordeling van Geneesmiddelen, 2020. https://www.geneesmiddeleninformatiebank.nl, geraadpleegd 2 april 2020. Ga naar bron: Geneesmiddeleninformatiebank. Utrecht: College ter Beoordeling van Geneesmiddelen, 2020. https://www.geneesmiddeleninformatiebank.nl, geraadpleegd 2 april 2020.
- Stephens MB, Beutler AI, O'Connor FG. Musculoskeletal injections: a review of the evidence. Am Fam Physician 2008;78:971-6.
- Habib GS, Badarny S, Rawashdeh H. A novel approach of local corticosteroid injection for the treatment of carpal tunnel syndrome. Clin Rheumatol 2006;25:338-40.
- Dammers JW, Roos Y, Veering MM, Vermeulen M. Injection with methylprednisolone in patients with the carpal tunnel syndrome: a randomised double blind trial testing three different doses. J Neurol 2006;253:574-7.
- Klokkari D, Mamais I. Effectiveness of surgical versus conservative treatment for carpal tunnel syndrome: a systematic review, meta-analysis and qualitative analysis. Hong Kong Physiother J 2018;38:91-114.
- Huisstede BM, Van den Brink J, Randsdorp MS, Geelen SJ, Koes BW. Effectiveness of surgical and postsurgical interventions for carpal tunnel syndrome-a systematic review. Arch Phys Med Rehabil 2018;99:1660-80.
- Shi Q, Bobos P, Lalone EA, Warren L, MacDermid JC. Comparison of the short-term and long-term effects of surgery and nonsurgical intervention in treating carpal tunnel syndrome: a systematic review and meta-analysis. Hand 2020;15:13-22.
- Hui AC, Wong SM, Andréu JL, Ly-Pen D. Surgery versus steroid injection in carpal tunnel syndrome: comment on the article by Ly-Pen et al [2] (multiple letters). Arthritis Rheum 2005;52:2578.
- Ly-Pen D, Andréu JL, De Blas G, Sánchez-Olaso A, Millán I. Surgical decompression versus local steroid injection in carpal tunnel syndrome: a one-year, prospective, randomized, open, controlled clinical trial. Arthritis Rheum 2005;52:612-9.
- Ismatullah, I. Local steroid injection or carpal tunnel release for carpal tunnel syndrome – which is more effective? Journal of Postgraduate Medical Institute 2013;27:194-9.
- Bohannon RW. Minimal clinically important difference for grip strength: a systematic review. J Phys Ther Sci 2019;31:75-8.
- Gerritsen AM, De Vet HC, Scholten RJ, Bertelsmann FW, De Krom MC, Bouter LM. Splinting vs surgery in the treatment of carpal tunnel syndrome: a randomized controlled trial. JAMA. 2002 Sep 11;288(10):1245-51.
- Ucan H, Yagci I, Yilmaz L, Yagmurlu F, Keskin D, Bodur H. Comparison of splinting, splinting plus local steroid injection and open carpal tunnel release outcomes in idiopathic carpal tunnel syndrome. Rheumatol Int. 2006;27:45-51.
- Jarvik JG, Comstock BA, Kliot M, Turner JA, Chan L, Heagerty PJ, et al. Surgery versus non-surgical therapy for carpal tunnel syndrome: a randomised parallel-group trial. Lancet 2009;374:1074-81.
- Vasiliadis HS, Sakellaridou ME, Shrier I, Salanti G, Scholten RJ. Open release for carpal tunnel syndrome. Cochrane Database Syst Rev 2014:CD008265.
- Hassan M, Ali MT, Nadeem A. Comparison of surgical excision versus aspiration and injection of steroid of wrist ganglion. Pakistan J Med Heal Sci 2017;11:1412-4.
- Amirfeyz R, McNinch R, Watts A, Rodrigues J, Davis TR, Glassey N, Bullock J. Evidence-based management of adult trigger digits. J Hand Surg Eur 2017;42:473-80.
- Lunsford D, Valdes K, Hengy S. Conservative management of triggervinger: a systematic review. J Hand Ther 2019;32:212-21.
- Kroon FP, Carmona L, Schoones JW, Kloppenburg M. Efficacy and safety of non-pharmacological, pharmacological and surgical treatment for hand osteoarthritis: a systematic literature review informing the 2018 update of the EULAR recommendations for the management of hand osteoarthritis. RMD Open 2018;4:e000734.
- Meenagh GK, Patton J, Kynes C, Wright GD. A randomised controlled trial of intra-articular corticosteroid injection of the carpometacarpal joint of the thumb in osteoarthritis. Ann Rheum Dis 2004;63:1260-3.
- Heyworth BE, Lee JH, Kim PD, Lipton CB, Strauch RJ, Rosenwasser MP. Hylan versus corticosteroid versus placebo for treatment of basal joint arthritis: a prospective, randomized, double-blinded clinical trial. J Hand Surg Am 2008;33:40-8.
- Mandl LA, Wolfe S, Daluiski A, Hotchkiss RN, Lyman SL, Katz JN. A randomized controlled trial of hylan G-F 20 for the treatment of carpometacarpal osteoarthritis. Arthritis Rheum 2012;64:S475-6.
- Spolidoro Paschoal NO, Natour J, Machado FS, De Oliveira HA, Furtado RN. Effectiveness of triamcinolone hexacetonide intraarticular injection in interphalangeal joints: a 12-week randomized controlled trial in patients with hand osteoarthritis. J Rheumatol 2015;42:1869-77.
- Franchignoni F, Vercelli S, Giordano A, Sartorio F, Bravini E, Ferriero G. Minimal clinically important difference of the disabilities of the arm, shoulder and hand outcome measure (DASH) and its shortened version (QuickDASH). J Orthop Sports Phys Ther 2014;44:30-9.
- Parker S, Riley N, Dean B; Oxford Upper Limb Collaborative. Management of osteoarthritis at the base of the thumb. Bone Joint J 2020;102-B:600-5.
- Fiorini HJ, Tamaoki MJ, Lenza M, Gomes Dos Santos JB, Faloppa F, Belloti JC. Surgery for triggervinger. Cochrane Database Syst Rev 2018:CD009860.
- Hansen RL, Søndergaard M, Lange J. Open surgery versus ultrasound-guided corticosteroid injection for triggervinger: a randomized controlled trial with 1-year follow-up. J Hand Surg Am 2017;42:359-66.
- Sato ES, Gomes dos santos JB, Belloti JC, Albertoni WM, Faloppa F. Treatment of triggervinger: randomized clinical trial comparing the methods of corticosteroid injection, percutaneous release and open surgery. Rheumatology 2012;51:93-9.
- Chang CJ, Chang SP, Kao LT, Tai TW, Jou IM. A meta-analysis of corticosteroid injection for trigger digits among patients with diabetes. Orthopedics 2018;41:e8-14.
- Ball C, Izadi D, Verjee LS, Chan J, Nanchahal J. Systematic review of non-surgical treatments for early Dupuytren's disease. BMC Musculoskelet Disord 2016;17:345.
- Cavaleri R, Schabrun SM, Te M, Chipchase LS. Hand therapy versus corticosteroid injections in the treatment of de Quervain’s disease: a systematic review and meta-analysis. J Hand Ther 2016;29:3-11.
- Alla SR, Deal ND, Dempsey IJ. Current concepts: malletvinger. Hand 2014;9:138-44.
- Moher D, Liberati A, Tetzlaff J, Altman DG, The PRISMA Group (preferred reporting items for systematic reviews and meta-Analyses): The PRISMA Statement. PLoS Med 2009;6:e1000097. https://doi.org/10.1371/journal.pmed.1000097, geraadpleegd april 2020. Ga naar bron: Moher D, Liberati A, Tetzlaff J, Altman DG, The PRISMA Group (preferred reporting items for systematic reviews and meta-Analyses): The PRISMA Statement. PLoS Med 2009;6:e1000097. https://doi.org/10.1371/journal.pmed.1000097, geraadpleegd april 2020.