Virushepatitis en andere leveraandoeningen
Richtlijnen diagnostiek
Naar Volledige tekst ›Anamnese
Naar Volledige tekst ›- Risicocontact of -groep (zie tabel 1 en tabel 2)
- Duur en beloop van eventuele klachten
- Doorgemaakte hepatitis A, B, C of E en eventuele behandeling
- Vaccinatie tegen hepatitis A of B
- Gebruik van medicatie, alcohol, drugs, kruiden of vitamine A
- Aanwezigheid van diabetes mellitus, hypertensie of afwijkend lipidenspectrum
Lichamelijk onderzoek
Naar Volledige tekst ›- Inspectie: mate van ziek zijn; sclerae (geel)
- Percussie en palpatie van de lever-, galblaas- en miltregio
- Bij vermoeden niet-alcoholische steatosis hepatis: gewicht, lengte, middelomtrek, bloeddruk
- Bij vermoeden van cirrose: huidinspectie (spider naevi, erythema palmare), gynaecomastie, flapping tremor, abdomen (ascites, veneuze collateralen buikwand)
Aanvullend onderzoek
Naar Volledige tekst ›|
Indicatie |
Bepalingen |
Toelichting |
Evaluatie |
|---|---|---|---|
|
Vermoeden hepatitis A |
IgM-anti-HAV |
Direct aantoonbaar |
Positieve uitslag bewijzend voor acute hepatitis A |
|
Vermoeden hepatitis B, acuut * § |
HBsAg Indien positief: herhaal na 6 maanden † |
Aantoonbaar ongeveer 1 maand na besmetting Het lab bepaalt ook altijd het anti-HB-core |
Positieve uitslag HBsAg: bewijzend voor hepatitis B Negatieve uitslag HBsAg bij positieve anti-HB-core: functioneel genezen hepatitis B |
|
Vermoeden hepatitis B, chronisch* § |
HBsAg |
|
Risicocontact > 6 maanden geleden óf risicocontact onbekend óf HBsAg positief > 6 maanden geleden: bewijzend voor chronische hepatitis B |
|
Vermoeden hepatitis C, acuut*
|
HCV-RNA Indien positief: herhaal na 3 maanden |
Aantoonbaar 7 dagen na besmetting |
Aanwezigheid HCV-RNA: bewijzend voor hepatitis C |
|
Vermoeden hepatitis C, chronisch * § |
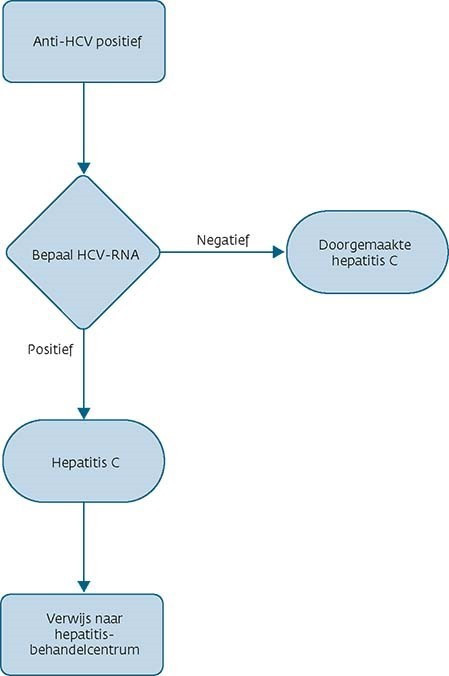
Anti-HCV‡ Indien positief: HCV-RNA |
Aantoonbaar 10 weken na besmetting |
Positieve uitslag: bewijzend voor (doorgemaakte) besmetting met HCV Aanwezigheid HCV-RNA: bewijzend voor hepatitis C Afwezigheid HCV-RNA bij positieve anti-HCV: bewijzend voor doorgemaakte of genezen hepatitis C |
|
Vermoeden hepatitis E |
IgM-anti-HEV |
Direct aantoonbaar |
Positieve uitslag: bewijzend voor acute hepatitis E |
|
* Acute hepatitis B of C: risicocontact < 6 maanden geleden. Chronische hepatitis B of C: risicocontact ≥ 6 maanden geleden. § Overweeg spreekuurbezoekers afkomstig uit intermediair- en hoog-endemische landen voor hepatitis-B- en -C, diagnostiek naar deze aandoeningen aan te bieden, ook als er geen klachten zijn. † Zie voor vervolgdiagnostiek bij positieve HBsAg: stroomschema 1. ‡ Zie voor vervolgdiagnostiek bij positieve anti-HCV: stroomschema 2. |
|||
Verhoogd ALAT
Bij een verhoogd ALAT (1,5 tot 10 maal de normaalwaarde) zie stroomschema 3.
Evaluatie
Naar Volledige tekst ›Zie voor hepatitis A, C en E tabel 3.
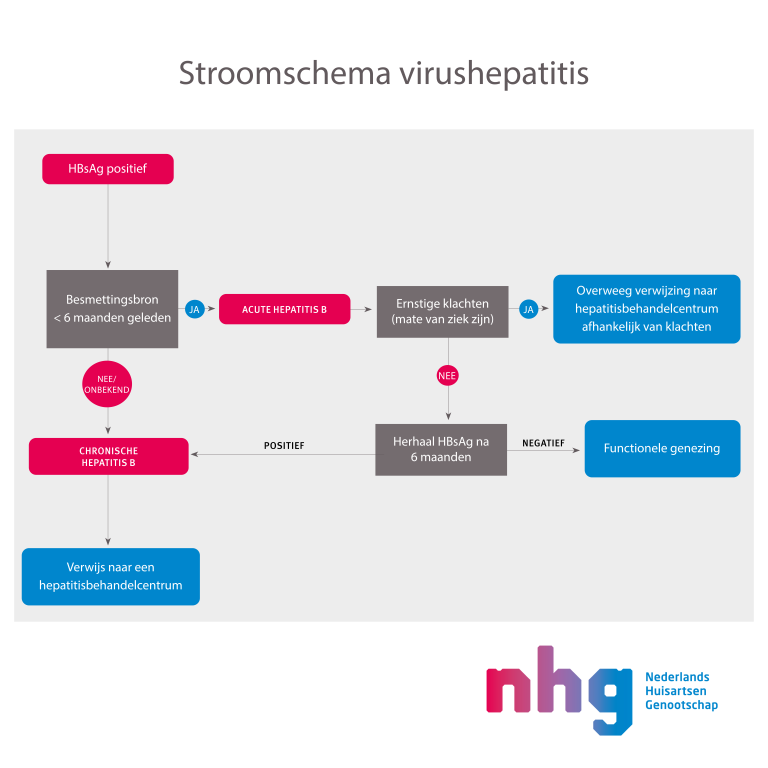
Acute hepatitis B
- risicocontact < 6 maanden geleden
- HBsAg positief
Chronische hepatitis B
- risicocontact ≥ 6 maanden geleden
- HBsAg positief
Functioneel genezen hepatitis B
- HBsAg negatief
- anti-HB-core positief
Overige leveraandoeningen
- Overweeg als ALAT bij herhaling is verhoogd (1,5 tot 10 maal normaalwaarde) bij negatieve uitslag virushepatitisserologie: leverschade door geneesmiddel- of alcoholgebruik of niet-alcoholische steatosis hepatis.
- Overweeg bij zeer hoge ALAT-waarden (> 10 maal normaalwaarde) acute leverschade door intoxicatie (alcohol en/of drugs) of toxische reactie door geneesmiddelen.
Richtlijnen beleid
Naar Volledige tekst ›Aangifteplicht
Meld acute hepatitis A, B en C en chronische hepatitis B en C binnen 1 werkdag bij de GGD.
Algemene voorlichting virushepatitis
- Benadruk belang van het vermijden van risicocontacten met de naasten.
- Bij hepatitis B en C: laat patiënt seksuele partner(s) tot een half jaar geleden waarschuwen.
- Benadruk belang vaccinatie partner bij hepatitis B.
Hepatitis A en E
Spreek vervolgcontact af naar behoefte.
Hepatitis B
- Acute hepatitis B
- spreek vervolgcontact af naar behoefte
- controleer na 6 maanden HBsAg; zie ook stroomschema 1.
- Chronische hepatitis B
- verwijs naar hepatitisbehandelcentrum
Hepatitis C
Verwijs naar hepatitisbehandelcentrum, tenzij acute hepatitis C < 3 maanden bestaat. In dat geval kan gedurende 3 maanden spontane genezing worden afgewacht.
Overige leveraandoeningen
- Verwijs direct bij een ALAT > 10 maal de normaalwaarde, tenzij er een duidelijke verklaring is met verwacht spontaan herstel.
- Voor overig beleid: zie de hoofdtekst.
Belangrijkste wijzigingen
Naar Samenvatting ›- Bij alle patiënten met chronische hepatitis B is levenslange controle nodig.
- Het onderscheid tussen actieve en inactieve chronische hepatitis B is vervallen.
- Bij een positieve anti-HCV is bepaling van het HCV-RNA nodig om te differentiëren tussen een actieve en een doorgemaakte hepatitis C.
- De behandeling van hepatitis B en C is gecentraliseerd in hepatitisbehandelcentra.
- De paragrafen over niet-alcoholische vetlever (NAFLD) en hepatotoxiciteit van geneesmiddelen zijn uitgebreid met aanbevelingen voor het beleid.
Kernboodschappen
Naar Samenvatting ›- Verwijs alle patiënten met chronische hepatitis B naar een hepatitisbehandelcentrum.
- Chronische hepatitis B en functioneel genezen hepatitis B kunnen worden ge(re)activeerd door gebruik van sterke immunosuppressiva.
- Verwijs alle patiënten met hepatitis C voor behandeling naar een hepatitisbehandelcentrum.
- Overweeg diagnostiek naar hepatitis B en C aan te bieden aan spreekuurbezoekers afkomstig uit intermediair- en hoog-endemische landen voor deze aandoeningen, ook als er geen klachten zijn.
- Verricht nadere diagnostiek naar leveraandoeningen als het ALAT bij herhaling > 1,5-10 maal boven de normaalwaarde ligt.
- Verwijs patiënten met een ALAT van > 10 maal de normaalwaarde direct.
- Goede samenwerking tussen huisartsen, hepatitisbehandelcentra (zie kader Hepatitisbehandelcentrum), verslavingsartsen en GGD’s is van belang om te komen tot goede diagnostiek, voorlichting en behandeling van patiënten met virushepatitis.
Hepatitisbehandelcentrum
Naar Samenvatting ›Sinds 2012 is de behandeling van virale hepatitis gecentraliseerd in hepatitisbehandelcentra in een aantal ziekenhuizen. Centralisatie was nodig omdat de behandeling steeds complexer is geworden. Door centralisatie kan optimale zorg worden geleverd aan patiënten met hepatitis B en C door behandelteams met kennis en expertise op het gebied van virushepatitis. De hepatitisbehandelaar verbonden aan deze centra kan, afhankelijk van de regionale afspraken, een maag-darm-leverarts of een internist-infectioloog zijn. Zie de volledige en actuele lijst op de website van de Nederlandse Vereniging van Maag-Darm-Leverartsen.
Inleiding
Naar Samenvatting ›Scope
Naar Samenvatting ›- Richtlijnen voor de diagnostiek en het beleid bij het vermoeden van virushepatitis en bij een aantal andere leveraandoeningen, namelijk levercelschade door alcoholmisbruik, gebruik van geneesmiddelen of drugs en niet-alcoholische vetlever (non-alcoholic fatty liver disease, NAFLD).
- Richtlijnen voor het beleid bij een bij herhaling verhoogd ALAT (1,5-10 maal boven de normaalwaarde). De standaard geeft daarnaast richtlijnen voor de preventie van virushepatitis.
- In Nederland zijn vooral infecties met het hepatitis-A-virus (HAV), het hepatitis-B-virus (HBV), het hepatitis-C-virus (HCV) en het hepatitis-E-virus (HEV) de oorzaak van virushepatitis. De standaard richt zich op de diagnostiek en het beleid bij al deze hepatitiden, maar vooral op de chronische hepatitis B en C.
Buiten de scope
Naar Samenvatting ›Zeldzame leveraandoeningen, zoals hepatitis D, auto-immuunhepatitis en hemochromatose, vallen buiten het bestek van deze standaard.
Samenwerking en afstemming
Naar Samenvatting ›Deze standaard is in samenwerking met de Nederlandse Internisten Vereniging (NIV) en Nederlandse Vereniging van Maag-Darm-Leverartsen (NVMDL) herzien en baseert zich voor de behandelindicaties voor hepatitis B en C op de richtlijnen over hepatitis B en C van de NIV en de NVMDL, en op het Richtsnoer HBV en het Richtsnoer HCV uit 2020 van deze verenigingen.
Achtergronden
Naar Samenvatting ›Epidemiologie
Naar Samenvatting ›Hepatitis A
Naar Samenvatting ›De incidentie van hepatitis A in de Nederlandse populatie neemt af; in 2003 waren er circa 900 gemelde nieuwe gevallen, in 2013 waren het er 109 (zie Hepatitis C).
Elk jaar steeg in de maanden augustus, september en oktober het aantal aangiftes van hepatitis A bij kinderen. Kinderen liepen de infectie op tijdens de vakantie in het geboorteland van hun ouders, met name in Marokko en Turkije.
Op grond hiervan hebben veel GGD’s hun vaccinatiebeleid aangepast; zij bieden vaccinatie tegen hepatitis A aan bij kinderen van ouders die op vakantie gaan naar het land van herkomst zoals Turkije of Marokko. Het aantal meldingen van hepatitis A is sindsdien sterk gedaald, in de periode 2003-2014 van 900 naar 109 per jaar, zie Hepatitis C.
Hepatitis B
Naar Samenvatting ›- De incidentie van hepatitis B is in Nederland licht gedaald. In 2013 werden 1267 nieuwe gevallen van hepatitis B gemeld: 140 met een acute hepatitis B en 1127 met een chronische hepatitis B. In 2003 was het aantal gemelde gevallen 1877.
- In Nederland hebben naar schatting 40.000 mensen een chronische hepatitis B. Het betreft veelal eerstegeneratiemigranten uit een land waar hepatitis B intermediair- of hoog-endemisch is. Deze groep patiënten heeft de infectie meestal op jonge leeftijd opgelopen.
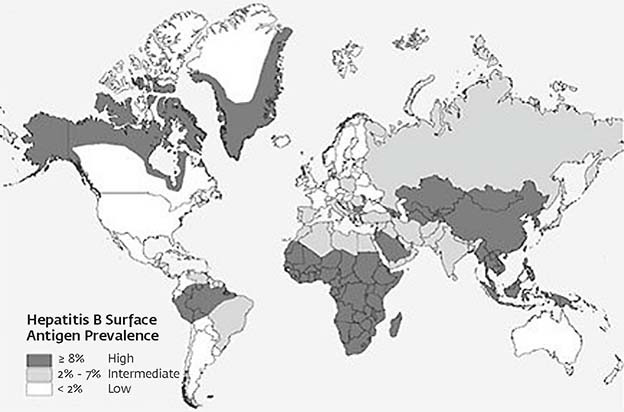
- In de Nederlandse bevolking vindt besmetting meestal op volwassen leeftijd plaats, via onbeschermd seksueel contact. De World Health Organization (WHO) maakt op basis van de prevalentie van het hepatitis-B-dragerschap onderscheid tussen laag-endemische (< 2%), intermediair-endemische (2-8%) en hoog-endemische landen (> 8%).
- Nederland behoort tot de laag-endemische landen. De landen rond de Middellandse Zee (met uitzondering van Frankrijk en Italië) en de landen in Oost-Europa behoren tot de intermediair-endemische landen. De Afrikaanse sub-Saharalanden en veel landen in Azië, met name Zuidoost-Azië, behoren tot de hoog-endemische landen.
- In Nederland vormen de eerstegeneratiemigranten uit China, Marokko en Turkije de grootste groep met chronische hepatitis B.
Hepatitis C
Naar Samenvatting ›- De incidentie van acute hepatitis C in Nederland stijgt de laatste jaren: in 2003 werden 15 gevallen van acute hepatitis C gemeld, in 2013 waren dat er 64. De stijging wordt vooral gezien onder hiv-seropositieve mannen die seks hebben met mannen (MSM).
- In Nederland hebben naar schatting 28.100 patiënten chronische hepatitis C. Co-infecties met hepatitis B of hiv komen regelmatig voor.
- De wereldwijde prevalentie van hepatitis C is grotendeels vergelijkbaar met die van hepatitis B.
Exacte prevalentiecijfers over virushepatitis in de huisartsenpraktijk zijn niet bekend omdat een onderscheid tussen de verschillende virushepatitiden op basis van de subcoderingen niet mogelijk is. Voor de incidentie en prevalentiecijfers van de verschillende virushepatitiden in de algemene populatie is gebruik gemaakt van de infectieziektenregistratie bij het RIVM.
In 2013 zijn in Nederland 109 gevallen van hepatitis A gemeld. Men schat dat circa 30% van de klinische gevallen wordt gemeld, waarmee de incidentie van hepatitis A zou uitkomen rond de 0,02 per 1000 patiënten per jaar. De incidentie neemt elk jaar af, in 2003 werden nog circa 900 gevallen gemeld. In de afgelopen jaren blijkt circa 40% van de gemelde gevallen van hepatitis A in Nederland in het buitenland besmet, waarvan 1/3 tijdens een reis in Marokko. Bij kinderen jonger dan 15 jaar gaat het vrijwel altijd om kinderen van migranten die op vakantie zijn geweest in het land van herkomst van de ouders. Bij personen van 15 jaar en ouder die een hepatitis-A-infectie in het buitenland hebben opgelopen, gaat het meestal om reizigers naar (sub)tropische gebieden die voor vertrek niet zijn gevaccineerd.
Er is een afname in het aantal gemelde gevallen van hepatitis B. In 2003 werden 1877 gevallen van hepatitis B gemeld; in 2013 waren dit er 1267: 140 acute en 1127 chronische gevallen. Deze cijfers zijn lager dan het werkelijke aantal nieuwe gevallen omdat er sprake is van onderdiagnostiek. In meer dan de helft van de gevallen (58%) van acute hepatitis B is het virus overgedragen via onbeschermd seksueel contact. De incidentie van hepatitis B in soa-klinieken is het hoogst onder eerstegeneratiemigranten (1%); onder tweedegeneratie-immigranten (0,1%) en autochtonen (0,07%) is de incidentie lager. De incidentie van acute hepatitis B wordt geschat op 0,7 per 100.000 inwoners: 1,2 voor mannen en 0,3 voor vrouwen.
Van de Nederlandse bevolking maakte 2,1% ooit een infectie met het HBV door. De prevalentie van chronische hepatitis B in de bevolking, dat wil zeggen dragerschap van HBsAg en van HBV-DNA, bedraagt ongeveer voor beide 0,2% [95%-BI –0,1 tot 0,4]. Dit betekent dat ongeveer 40.000 Nederlanders chronisch drager zijn van het hepatitis-B-virus. Van deze groep zou ruim 30% voor behandeling in aanmerking komen.
De prevalentie van HBsAg-dragerschap onder zwangere vrouwen is circa 0,3%. Van de zwangere draagsters is circa 88% van allochtone afkomst. In risicogroepen, zoals mannen die seks hebben met mannen (MSM) of injecterende drugsgebruikers, is de prevalentie van een doorgemaakte of chronische hepatitis-B-infectie hoger.
In instellingen voor verstandelijk gehandicapten is de prevalentie van chronische hepatitis B 39 per 1000 bewoners; een kwart van de bewoners heeft ooit een hepatitis-B-infectie doorgemaakt.
Het aantal meldingen van acute hepatitis C was in 2013 64. Dit is een stijging ten opzichte van 2003 toen 15 gevallen werden gemeld. Onbeschermd seksueel contact bij MSM was de belangrijkste oorzaak van de overdracht van hepatitis C (n = 51); hiervan was 71% (n = 36) hiv-positief. De prevalentie van HCV in de algemene bevolking (15-79 jaar) is onbekend, maar wordt geschat op 0,22% [95%-BI 0,07 tot 0,37%], wat neerkomt op ongeveer 28.100 patiënten. Circa 70% van de patiënten met HCV is geboren in een land dat intermediair- of hoog-endemisch is voor HCV. De prevalentie van HCV-antistoffen in Nederland bij personen van allochtone herkomst komt vermoedelijk overeen met de gevonden prevalentie in het land van herkomst (Marokko, Turkije, Egypte, Afrika bezuiden de Sahara). De prevalentie van antistoffen tegen HCV bij injecterende drugsgebruikers loopt, afhankelijk van de duur van het injecterend drugsgebruik, op tot 70-80%. Ook onder niet-injecterende drugsgebruikers is de prevalentie van HCV hoog: 10-15%. Van de Nederlandse hemofiliepatiënten heeft meer dan de helft antistoffen tegen HCV. Van de 4000 dialysepatiënten heeft ongeveer 3% antistoffen. Afname van injecterend drugsgebruik in Nederland in combinatie met programma’s gericht op het reduceren van het aantal nieuwe patiënten met HCV heeft ertoe geleid dat het aantal nieuwe infecties in deze groep sinds midden jaren 90 sterk is afgenomen.
Co-infecties van HBV, HCV en hiv komen regelmatig voor. In Nederland heeft 8% van de patiënten met een doorgemaakte hepatitis-C-infectie tevens een hiv-infectie.
Nederland behoort tot de laag-endemische landen, waar de prevalentie van dragerschap minder dan 2% bedraagt. Dit geldt ook voor de andere landen in Noordwest-Europa.
Hepatitis B
In het grootste deel van de wereld is hepatitis B intermediair-endemisch (prevalentie 2-8%), of hoog-endemisch (prevalentie ≥ 8%). De cijfers over de wereldwijde prevalentie zijn afkomstig van de WHO.
Hepatitis C
Als endemisch hepatitisgebied beschouwt men landen met een prevalentie > 2%, als hoog-endemisch gebied landen met een prevalentie van > 10%. Hepatitis C heeft een prevalentie > 10% in Egypte, Burundi, Kameroen, Guinee, Bolivia, Mongolië en Rwanda. Patiënten die geboren zijn in een hoog-endemisch gebied komen in aanmerking voor hepatitis-C-diagnostiek.
De cijfers over de prevalentie van hepatitis C zijn berekend in een meta-analyse (n = 232 onderzoeken), die de grondslag vormt voor het landenoverzicht van hepatitis C.
Hepatitis E
Naar Samenvatting ›De incidentie van hepatitis E in Nederland stijgt: in 2013 waren er 67 meldingen en in 2014 waren er 205.
Overige virale oorzaken van hepatitis
Naar Samenvatting ›De incidentie van mononucleosis infectiosa (epstein-barrvirus (EBV)) in 2013 is voor mannen 0,9 per 1000 patiënten en voor vrouwen 1,3 per 1000 patiënten. De incidentie van het cytomegalovirus (CMV) is onbekend.
Hepatitis D treedt alleen op als co- of superinfectie van hepatitis B en is in Nederland zeldzaam.
De symptomen van Hepatitis E zijn vergelijkbaar met die van hepatitis A. Het is onduidelijk wat de exacte incidentie en prevalentie van hepatitis E in Nederland is. Het is geen meldingsplichtige ziekte, waardoor het RIVM afhankelijk is van vrijwillige meldingen. In 2013 waren er 67 vrijwillige meldingen en in 2014 205. Het was voorheen een importziekte, maar hepatitis E wordt nu ook gediagnosticeerd bij patiënten zonder een reisanamnese. De ziekte is endemisch in Aziatische, Afrikaanse en Midden-Amerikaanse landen. In een retrospectief onderzoek in Nederland bij 139 patiënten met een onverklaarde ALAT-stijging waren 16 (11,5%) serummonsters positief voor hepatitis E IgM. Er zijn bij gezonde patiënten geen hygiënemaatregelen of behandeling noodzakelijk.
Tot op heden is er geen bewijs voor het bestaan van hepatitis F en G.
De incidentie van EBV in de hoofdtekst is afkomstig van de Continue Morbiditeitsregistratie van het Nivel (zie www.nivel.nl). Het is niet bekend welk percentage hiervan ook hepatitis veroorzaakt. Incidentiecijfers van CMV in Nederland zijn niet bekend.
Overige leveraandoeningen
Naar Samenvatting ›Verhoogde transaminasewaarden komen naar schatting voor bij 1-4% van de algemene bevolking. Niet-alcoholische vetlever (NAFLD) is de meest voorkomende oorzaak van asymptomatische, licht verhoogde transaminasewaarden. De prevalentie van NAFLD ligt in populatieonderzoeken tussen de 15 en 30% en neemt toe met de leeftijd. De incidentie van cirrose en andere leveraandoeningen in de huisartsenpraktijk is 0,6 per 1000 per jaar en de prevalentie 4,4 per 1000 per jaar. Cijfers over levercelschade door alcohol of door geneesmiddelen zijn niet bekend.
Het gaat hierbij om een verhoogd ALAT dat niet past bij acute levercelschade. Als bovengrens geldt grofweg een licht verhoogd ALAT (meer dan 1,5 de bovengrens van normaal, en minder dan 10 maal de referentiewaarde). Verhoogde transaminasewaarden komen voor bij circa 1-4% van de asymptomatische populatie. Enkele onderzoeken geven inzicht in de mogelijke oorzaken.
Mathiesen onderzocht in Zweden 150 patiënten met licht verhoogde transaminasewaarden die meer dan 6 maanden bestonden. Het ging uitsluitend om personen zonder klachten of symptomen. Het onderzoek bestond uit laboratoriumonderzoek, echografie en een leverbiopsie. De volgende aandoeningen werden gevonden: niet-alcoholische steatosis hepatis 40%, chronische virale hepatitis C 15,3%, waarschijnlijke alcoholische leveraandoening 8%, niet-alcoholische steatohepatitis 2%, auto-immuunhepatitis 1,3%, primaire biliaire cirrose 1,3% en alfa-antitrypsinedeficiëntie 0,7%.
Daniel onderzocht in de Verenigde Staten 1124 patiënten met verhoogde transaminasewaarden (verhoging ten minste 1,5 boven de normaalwaarde op ten minste 2 momenten gedurende meer dan 6 maanden) met of zonder klachten. Bij degenen zonder klachten bij wie bovendien geen aanwijzingen bestonden voor infectieuze hepatitis, auto-immuunhepatitis, erfelijke leverziekte of levercelschade ten gevolge van alcohol of geneesmiddelen, vond hij de volgende oorzaken: niet-alcoholische steatosis hepatis 48%, niet-alcoholische steatohepatitis 35%, fibrose 5%, cirrose 1,5%, geen afwijkingen 10%.
Pendino et al. onderzochten in 2002-2003 personen van 12 jaar en ouder via een steekproef bestaande uit 20% van de bewoners van een stadje in Zuid-Italië. Bij de proefpersonen werden onder meer de leverfuncties, lipiden, glucose, HBV- en HCV-status bepaald en werd de alcoholintake nagevraagd. Indien er geen virusinfectie werd vastgesteld maar wel een abnormale leverfunctie, bepaalde men opnieuw de leverfunctie. Tevens werd een echografie van de bovenbuik verricht en aanvullende diagnostiek om andere oorzaken ter verklaring van de levercelschade op te sporen. Bij de 1645 onderzochte personen was de prevalentie van HBsAg 0,8% en de prevalentie van anti-HCV 6,5% (de prevalentie was vooral hoog bij 50-plussers). De overall prevalentie van abnormale leverfuncties was 12,7% [95%-BI 11,1 tot 14,3]. Als waarschijnlijke oorzaak werden vastgesteld: overmatig alcoholgebruik 45,6%, waarschijnlijk niet-alcoholische steatosis hepatis 24%, HCV 18,6%, HBV 1%, alcohol plus HCV en/of HBV 8,8%, zeldzame ziekten 2%.
Meer recente maar kleinere observationele onderzoeken laten vergelijkbare prevalentiecijfers zien.
Concluderend behoren tot de meestvoorkomende oorzaken van licht verhoogde ALAT-waarden overmatig alcoholgebruik, niet-alcoholische steatosis hepatis, niet-alcoholische steatohepatitis, chronische hepatitis B, chronische hepatitis C, medicatie, toxines en cirrose. Minder vaak voorkomende oorzaken zijn: auto-immuunhepatitis, hemochromatose, ziekte van Wilson en alfa-1-antitrypsinedeficiëntie. Niet-hepatische oorzaken zijn onder meer: coeliakie, hemolyse, myopathie, hyperthyreoïdie en flinke lichamelijke inspanning.
Goede cijfers over de incidentie en prevalentie van leveraandoeningen zijn moeilijk te geven. De in de hoofdtekst genoemde incidentie- en prevalentiecijfers van levercirrose en andere leveraandoeningen in de huisartsenpraktijk (ICPC code D97) zijn afkomstig uit de zorgregistraties van het Nivel. De prevalentiecijfers van NAFLD zijn bij populatieonderzoeken 15 tot 30%. Bij een Nederlands bevolkingsonderzoek bij patiënten van 65 jaar en ouder was de prevalentie 35%.
Etiologie en pathofysiologie
Naar Samenvatting ›Virushepatitis
Naar Samenvatting ›- Alle virushepatitiden kunnen zich manifesteren als een acute ziekte. Een acute hepatitis kan een klinisch of subklinisch beloop hebben. Dit laatste treedt vooral op bij hepatitis-B- of ‑C‑infectie.
- Hepatitis B en C hebben meestal een chronisch en asymptomatisch beloop.
- De klinische verschijnselen van acute hepatitis veroorzaakt door de verschillende typen hepatitisvirus zijn gelijk.
- Een klinisch manifeste acute hepatitis begint met een prodromaal stadium (duur 3-10 dagen) met malaise, moeheid, verminderde eetlust en koorts.
- Ook kunnen in deze fase misselijkheid en braken optreden, evenals pijn rechts in de bovenbuik, huiduitslag en artralgieën.
- Hierna volgt de icterische fase, die gepaard gaat met geelzucht, lichte temperatuursverhoging, de karakteristieke donkere urine en soms ontkleurde ontlasting. Ook jeuk ten gevolge van de cholestase komt in deze fase frequent voor.
- De acute fase duurt in de regel 1-3 weken. De geelzucht kan echter enkele maanden aanhouden evenals de malaise en moeheid. Vaak is er in deze periode een intolerantie voor vet, alcohol en tabak. Hierna volgt de herstelfase.
- De verschijnselen bij een subklinisch beloop zijn aspecifiek. Soms is er moeheid.
- Patiënten met chronische hepatitis B of C kunnen last hebben van moeheid, maar vaker zijn er geen klachten. Meestal krijgen zij pas symptomen in een vergevorderd stadium van de ziekte, waarbij levercirrose of levercelcarcinoom is ontstaan. In de meeste gevallen hebben deze patiënten in de voorafgaande jaren geen symptomen gehad van acute hepatitis.
Hepatitis A
Naar Samenvatting ›- Een acute hepatitis A-infectie komt vooral voor bij kinderen met een migratieachtergrond en bij volwassenen die ongevaccineerd naar endemische gebieden reizen (zie tabel 2).
- Bij jonge kinderen verloopt de ziekte meestal subklinisch. Vanaf de leeftijd van 5 jaar is de kans op klinische ziekteverschijnselen > 75%.
- Besmetting vindt plaats via de feco-orale weg (zie tabel 1). De incubatietijd is gemiddeld 28 dagen. Een patiënt is besmettelijk vanaf ca. 3-7 dagen vóór, tot 1 week na het ontstaan van de icterus.
- Hepatitis A geneest volledig zonder medicatie; complicaties of een fulminant beloop komen zelden voor.
De duur en ernst van een hepatitis-A-infectie nemen in het algemeen toe met de leeftijd. Amerikaanse onderzoekers constateerden bij patiënten met een hepatitis-A-infectie een symptomatisch beloop bij 0- tot 2-jarigen in 16% van de gevallen, bij 3- tot 4-jarigen in 50% en vanaf 5 jaar in 80%.
Overdracht van het hepatitis-A-virus vindt meestal plaats via feco-orale weg, voornamelijk door inname van (ongekookt) verontreinigd water of voedsel (vooral voedsel uit verontreinigd water zoals garnalen of schelpdieren). Ook kan besmetting plaatsvinden via oro-anaal seksueel contact. De besmettelijkheid hangt sterk samen met de concentratie van het virus in de feces of in het besmette voedsel. De periode van besmettelijkheid ligt vooral aan het einde van de incubatietijd en in de eerste week na het ontstaan van de icterus, maar ook anicterische, subklinische patiënten zijn besmettelijk.
Een zeldzame complicatie van een acute hepatitis A is acuut leverfalen, dat optreedt binnen twaalf weken na het begin van de icterische fase en gekenmerkt wordt door verschijnselen van encefalopathie. De kans op een ernstig beloop van hepatitis-A-infectie is verhoogd bij personen met een chronische leveraandoening en neemt toe met de leeftijd.
Hepatitis B
Naar Samenvatting ›Besmetting en incubatietijd
- Hepatitis B komt in Nederland vooral voor bij eerstegeneratiemigranten uit intermediair- en hoog-endemische landen en bij (ex-)drugsgebruikers (intraveneus), MSM, sekswerkers en personen met veel wisselende seksuele contacten (zie tabel 2).
- Besmettingsbronnen zijn virus bevattende lichaamsvloeistoffen, zoals bloed, sperma en vaginaal vocht van geïnfecteerde personen (tabel 1).
- In Nederland vindt besmetting vooral plaats via onbeschermd seksueel contact. Tot 40% van de niet-gevaccineerde seksuele partners van patiënten met hepatitis B raakt geïnfecteerd.
Acute hepatitis B
De incubatietijd is 2-3 maanden. Besmettelijkheid begint ca. 6 weken voor het begin van de klachten en houdt aan tot het hepatitis-B-oppervlakteantigeen (HBsAg) na ca. 4-6 maanden uit het lichaam verdwijnt.
Chronische hepatitis B
- Hepatitis B is chronisch als het HBsAg > 6 maanden aanwezig blijft. Het risico hierop is groter naarmate de patiënt jonger geïnfecteerd werd en loopt uiteen van < 5% voor volwassenen en kinderen > 5 jaar tot 90% voor kinderen die de infectie oplopen in hun eerste levensjaar.
- Onbehandeld ontstaat bij circa 20% van de volwassen patiënten met chronische hepatitis B met een behandelindicatie na 5-25 jaar levercirrose. Bij circa 10% van de patiënten met levercirrose ontstaat binnen 5 jaar een hepatocellulair carcinoom (HCC). Een HCC kan ook ontstaan zonder dat er sprake is van levercirrose.
- De laatste jaren zijn er nieuwe diagnostische mogelijkheden in de tweede lijn beschikbaar: de specialist bepaalt met behulp van aanvullend laboratoriumonderzoek, een echo abdomen en een fibroscan of er een indicatie voor behandeling of HCC-screening bestaat. De huisarts kan de fibroscan op dit moment niet aanvragen.
- De behandeling is gericht op klaring van het virus uit het bloed, gedefinieerd als seroconversie van het HBsAg en een niet-detecteerbare virusconcentratie.
- Doel is het voorkomen van complicaties, zoals cirrose en HCC
- De indicatie voor behandeling is afhankelijk van het ALAT, HBeAg en HBV-DNA, en risicofactoren voor HCC.
- De hepatitisbehandelaar stelt de indicatie voor de behandeling vast.
- Circa 35% van de patiënten bereikt functionele genezing. Bij de overige 65% wordt geprobeerd het risico op cirrose en HCC te verkleinen. Dit lukt bij 90% van deze patiëntengroep.
- De laatste jaren zijn er nieuwe virusremmende geneesmiddelen (nucleos(t)ide analogen: effectiever en met minder bijwerkingen) beschikbaar gekomen.
- Bij patiënten bij wie in het verleden de behandeling niet succesvol was, beoordeelt de hepatitisbehandelaar of zij weer in aanmerking komen voor behandeling.
- Een chronische hepatitis B kan worden ge(re)activeerd door gebruik van sterke immunosuppressiva, zoals biologicals, of chemotherapie.
Functioneel genezen hepatitis B
- Een hepatitis B is functioneel genezen bij de volgende uitslagen: HBsAg negatief én antistoffen tegen het hepatitis B-‘core’-antigeen (anti-HB-core) positief én anti-HBs positief. De anti-HBs concentratie kan later dusdanig dalen dat deze als negatief afgegeven wordt.
- Dit kan zowel voorkomen na een acute hepatitis B als na een chronische hepatitis B.
- Een functioneel genezen hepatitis B kan worden gereactiveerd door gebruik van sterke immunosuppressiva, zoals biologicals, of chemotherapie.
Zwangeren met hepatitis B
- De kans op overdracht van hepatitis B van moeder op kind tijdens de bevalling is afhankelijk van de mate van besmettelijkheid van de moeder en loopt uiteen van 18% bij moeders die HBeAg negatief zijn en een lage virusconcentratie hebben tot 80% bij HBeAg-positieve-moeders .
- Bij zwangeren met hepatitis B is het van belang het risico op overdracht van het virus van moeder op kind zoveel mogelijk te beperken door immunisatie van de pasgeborene en op indicatie door antivirale behandeling van de zwangere.
Het wel of niet optreden van klinische verschijnselen is ook bij hepatitis B afhankelijk van de leeftijd. Bij kinderen < 5 jaar is < 5% van de infecties symptomatisch, bij volwassenen 30-50%. De kans dat een hepatitis B-infectie chronisch wordt, is daarentegen groter naarmate de patiënt jonger is: 90% voor kinderen die de infectie oplopen in hun eerste levensjaar, 30% voor kinderen in de leeftijdsgroep 1-5 jaar en < 5% voor kinderen > 5 jaar en volwassenen.
Ten aanzien van de besmettingsweg wordt onderscheid gemaakt tussen horizontale en verticale transmissie. Horizontale transmissie van het hepatitis B-virus vindt plaats door bloed(producten) en besmette lichaamsvloeistoffen (sperma, vaginaal vocht) via beschadigde huid of slijmvliezen van de ontvanger, dus met name via parenterale weg en bij seksueel contact.
Het transmissiepercentage bij niet-geïmmuniseerde partners van heteroseksuele hepatitis B-patiënten kan oplopen tot 40%. In 2014 werd 57% van de acute hepatitis B veroorzaakt door een seksueel contact (21% MSM, 25% heteroseksueel). Via speeksel vindt zelden overdracht plaats. Alleen als de virale load in het serum heel hoog is (>107), valt transmissie niet uit te sluiten. Bij bijten en speeksel op het slijmvlies kan dit wel gebeuren, maar de grootte van het risico is onbekend. De besmettingskans na een prikaccident met een besmette naald wordt geschat op 1 tot 31%, afhankelijk van de HBV-DNA-concentratie en de HBeAg-status. Sinds 1975 vindt in Nederland donorscreening op HBV plaats. Besmetting via bloedtransfusie, dialyse of endoscopie is in Nederland daarom zeer zeldzaam, in het buitenland loopt men (veel) meer risico. Van patiënten die worden gedialyseerd of behandeld in verband met hemofilie, is door herhaald testen meestal al bekend of zij besmet zijn met HBV.
Zowel bij horizontale als verticale transmissie hangt de besmettelijkheid sterk af van de concentratie van de virusdeeltjes in de lichaamsvloeistof waarmee iemand in contact komt. In het bloed is deze concentratie in het algemeen hoog als de geïnfecteerde HBeAg-positief is. Het risico op infectie kan dan bij horizontale transmissie oplopen tot 40%.
Verticale transmissie van het hepatitis B-virus, van moeder op kind, vindt vooral plaats via perinataal bloedcontact. De kans op overdracht ligt, zonder passieve immunisatie en vaccinatie van de pasgeborene, rond de 80% bij een HBeAg-positieve moeder en rond de 18% bij moeders die alleen HBsAg-positief zijn.
Er is volledig herstel bij hepatitis B als seroconversie van het HBsAg optreedt: het verdwijnen van HBsAg en aantoonbaar worden van anti-HBs. Vanaf dat moment is de besmettelijkheid verdwenen en de aandoening functioneel genezen. Er is een chronische hepatitis-B-infectie als het HBsAg > 6 maanden aanwezig blijft.
Patiënten met een chronische hepatitis B-infectie die ook óf HBeAg-positief zijn, óf een verhoogd ALAT hebben, óf een hoog HBV-DNA hebben (voorheen actieve chronische hepatitis B), hebben een sterk verhoogde kans om cirrose en/of levercelcarcinoom (HCC) te ontwikkelen. Per jaar ontwikkelt gemiddeld 6% van deze patiënten levercirrose, met een cumulatieve vijfjaarsincidentie van 20%. Bij HBV-gerelateerde cirrose is de kans op HCC sterk verhoogd: het cumulatieve 5-jaarsrisico op HCC ligt in Europa rond de 10%. De kans dat een patiënt cirrose of HCC ontwikkelt, is groter als er een co-infectie bestaat met hepatitis C of hiv. Een HCC kan ook ontstaan zonder dat er sprake is van levercirrose (bij < 10% van de patiënten ontstond HCC na chronische hepatitis B) [Chayanupatkul 2017].
Hepatitis-B-antigenen (HBsAg) zijn ongeveer één maand na besmetting aantoonbaar. Deze blijven aantoonbaar bij een chronische hepatitis B. Bij genezing verdwijnen deze weer. Anti-HB-core is een antistof die verschijnt na ongeveer vijf weken en altijd aantoonbaar blijft, ook na klaring van het virus. Aanwezigheid van anti-HB-core in afwezigheid van HBsAg is bewijzend voor een doorgemaakte infectie. HBeAg is het hepatitis-B-e-antigeen dat behoort tot een deel van de kern van het hepatitis-B-virus. Indien dit antigeen aanwezig is, is de patiënt erg besmettelijk. Anti-HBe is een antistof tegen HBeAg. Deze kan na vier tot zeven maanden verschijnen; in dat geval is er sprake van een laag-viremische infectie. HBV-DNA is aantoonbaar vanaf ongeveer twee weken na besmetting en blijft aanwezig bij een chronische hepatitis B. Na klaring verdwijnt het HBV-DNA. Antistoffen tegen het hepatitis-B-virus (anti-HBs) zijn aanwezig na een doorgemaakte hepatitis B of een geslaagde vaccinatie.
De behandeling is gericht op HBsAg-seroconversie, met als doel minder kans op cirrose en hepatocellulair carcinoom en betere overlevingskansen. Als seroconversie niet wordt bereikt, is de behandeling gericht op het induceren van een inactieve fase. Dit geeft ook verbetering van de prognose voor de overleving en vermindering van het risico op cirrose en hepatocellulair carcinoom. De inactieve fase wordt afgemeten aan de volgende maten: normalisering van het ALAT, HBeAg-seroconversie (negatief worden HBeAg) en daling van HBV-DNA tot < 2000 IU/ml.
De patiënten kunnen worden behandeld met virusremmers en peginterferon. Het succes van de behandeling hangt af van de mate van levercelschade, de mate van virusreplicatie, het genotype van het virus, de keuze en de combinatie van middelen en de bijwerkingen die kunnen leiden tot verminderde therapietrouw. De effectiviteit van de behandeling is circa 35% voor het klaren van het virus en loopt op tot 90% voor het induceren van een inactieve fase.
De laatste jaren zijn er meer groepen virusremmers beschikbaar. Deze hebben de plek van peginterferon-alfa als eerste keus overgenomen. Het belangrijkste voordeel van deze nieuwere middelen is dat zij minder bijwerkingen geven; nadeel is dat zij langdurig moeten worden voorgeschreven om de respons te handhaven. Patiënten bij wie de behandeling in het verleden niet effectief was, komen mogelijk in aanmerking voor de behandeling met een van de nieuwe virusremmers.
Bij chemotherapie of een andere behandeling die ernstige immuunsuppressie geeft, zoals biologicals, kan een ‘genezen’ of chronische hepatitis B-infectie zonder behandelindicatie reactiveren. In zo’n geval is profylactische behandeling met een nucleoside- of nucleotideanaloog in een hepatitisbehandelcentrum aangewezen. Deze behandeling geeft een vier- tot zevenvoudige verlaging van de kans op opleving van de hepatitis en reactivering van het HBV.
Hepatitis C
Naar Samenvatting ›Besmetting en incubatietijd
Naar Samenvatting ›- Een acute hepatitis-C-infectie komt vooral voor bij volwassenen. De wijze van besmetting verloopt via bloed-bloedcontact (zie tabel 1). Het risico op overdracht van hepatitis C via seksueel contact is klein, behalve bij seksuele handelingen waarbij slijmvliesbeschadiging en bloedverlies voorkomen, zoals is beschreven bij MSM. Het risico bij MSM neemt vooral toe in geval van co-infectie met rectaal lymphogranuloma venereum of hiv.
- De incubatietijd is ca. 2 maanden. Het bloed van de geïnfecteerde kan al na een week besmettelijk zijn voor anderen.
- Bij 80% van de geïnfecteerden ontstaat een chronische infectie. Het virus is dan > 6 maanden aanwezig. Spontane genezing treedt vrijwel altijd binnen 3 maanden na de besmetting op.
- Patiënten met een chronische hepatitis C lopen meer risico om cirrose (circa 20%) en HCC te ontwikkelen; binnen 5 jaar ontwikkelt bij circa 17% van de patiënten met cirrose een HCC.
- Het risico op overdracht van HCV van moeder op kind tijdens de bevalling is < 10% en afhankelijk van de viral load en een eventuele co-infectie met hiv.
- Na een geslaagde behandeling is het mogelijk om opnieuw geïnfecteerd te raken met hepatitis C; antistoffen tegen hepatitis C zijn niet beschermend.
Een hepatitis-C-infectie verloopt op alle leeftijden meestal subklinisch: slechts 20 tot 30% van de patiënten heeft klachten en slechts 10 tot 15% ontwikkelt een icterus. De besmettingsweg van hepatitis C is via direct bloed-bloedcontact. Sinds 1992 worden bloeddonoren op hepatitis C onderzocht, zodat sindsdien het risico op overdracht door bloedproducten (volbloed, rode bloedcellen en bloedplaatjes en stollingsfactoren) in Nederland, West-Europa, de VS en Australië vrijwel uitgesloten is; in het buitenland is het risico, afhankelijk van de prevalentie, veel groter. Bij patiënten die worden gedialyseerd of behandeld in verband met hemofilie, is door herhaald testen meestal al bekend of zij besmet zijn met HCV.
Het risico op transmissie binnen het gezin of bij seksueel contact is klein. Een uitzondering hierop vormt de groep die seksuele technieken gebruikt waarbij slijmvliesbeschadiging en bloedverlies optreden, zoals beschreven bij MSM. Bij een co-infectie met rectaal lymphogranuloma venereum of hiv is het risico op besmetting groter.
Een hepatitis-C-infectie leidt in ongeveer 75 tot 85% van de gevallen tot een chronische hepatitis. Het beloop is wisselend en goede langetermijngegevens ontbreken omdat de infectie vaak een subklinisch begin heeft. Bij 3 tot 30% van de patiënten met chronische hepatitis C ontstaat binnen 20 jaar ernstige leverfibrose (een aandoening waarbij gezond leverweefsel langzaam wordt vervangen door littekenweefsel) of levercirrose (eindstadium van leverfibrose). Ook bij cirrose ten gevolge van een HCV-infectie is het risico op levercelcarcinoom sterk verhoogd: het cumulatieve 5-jaarsrisico op levercelcarcinoom in Europa wordt geschat op 17%.
Het risico op overdracht van HCV tijdens de bevalling ligt tussen de 3 en 7%. Overdracht vindt eigenlijk alleen plaats indien er HCV-RNA aantoonbaar is. Hoe hoger de concentratie van het HCV, hoe groter het risico op transmissie. Co-infectie met hiv vergroot het risico op perinatale overdracht van het virus 4 à 5 keer.
Behandeling hepatitis C
Naar Samenvatting ›- Bij alle patiënten met hepatitis C is behandeling geïndiceerd om cirrose en levercelcarcinoom te voorkomen. De behandeling is gericht op klaring van het virus tot niet-detecteerbare concentratie. De effectiviteit van de behandeling van chronische hepatitis C voor het klaren van het virus varieert van 60-100%.
- Bij patiënten bij wie een behandeling in het verleden niet succesvol was, wordt beoordeeld of deze in aanmerking komen voor behandeling met nieuwere geneesmiddelen, die effectief zijn en minder bijwerkingen hebben.
- Bij vrouwen met hepatitis C en een actuele kinderwens is het van belang het risico op overdracht van het virus van moeder op kind zoveel mogelijk te beperken. Dit gebeurt bij voorkeur door antivirale behandeling voorafgaand aan de zwangerschap. Tijdens zwangerschap is behandeling van hepatitis C niet mogelijk wegens de teratogene werking van de medicatie.
|
Risicocontacten |
Hepatitis A |
Hepatitis B |
Hepatitis C |
Hepatitis E |
|---|---|---|---|---|
|
Besmet voedsel en drinkwater |
Ja |
Nee |
Nee |
Ja |
|
Ontlasting en urine |
Ja |
Nee |
Nee |
Ja |
|
Bloed; alle lichaamsvloeistoffen met bloedbijmenging |
Nee |
Ja |
Ja |
Nee |
|
Prik-, snij-, spat- en bijtaccidenten |
Nee |
Ja |
Ja |
Nee |
|
Niet-steriel uitgevoerde medische ingreep in endemisch gebied |
Nee |
Ja |
Ja |
Nee |
|
Tatoeage, piercing of acupunctuur (uitgevoerd in endemisch gebied) |
Nee |
Ja |
Ja |
Nee |
|
Geboorte kind van een moeder die virusdrager is |
Nee |
Ja |
Ja |
Nee |
|
Ejaculaat en vaginaal vocht |
Nee |
Ja* |
Nee |
Nee |
|
Speeksel |
Nee |
Nee** |
Nee |
Nee |
|
* Met name bij onbeschermd seksueel contact met een persoon met hepatitis B of een grote kans hierop (afkomstig uit een endemisch land, MSM of sekswerkers met risicocontacten in de afgelopen 6 maanden). |
||||
|
Risicogroepen |
Hepatitis A |
Hepatitis B |
Hepatitis C |
Hepatitis E |
|---|---|---|---|---|
|
Personen met een beroepsrisico |
Jaa |
Jab |
Jab |
Nee |
|
Reizigers naar endemische gebieden |
Ja, vooral kinderen |
Jac |
Neec |
Ja |
|
(Gezins)contacten met besmette personen |
Ja |
Ja |
Need |
Nee |
|
Mensen met wisselende seksuele contactene |
Ja (bij oro-anaal contact) |
Ja |
Neef |
Nee |
|
Verstandelijk gehandicapten |
Ja |
Ja |
Nee |
Nee |
|
Kinderen in kinderopvangcentra en groep 1 en 2 |
Ja |
Nee |
Nee |
Nee |
|
Personen afkomstig uit endemisch gebied |
Nee |
Jac |
Ja c |
Nee |
|
Personen met een positieve familieanamnese voor chronische hepatitis, levercelcarcinoom |
Nee |
Ja |
Ja |
Nee |
|
(Ex-)drugsgebruikers (intraveneus) |
Nee |
Ja |
Ja |
Nee |
|
Ontvangers van bloed of bloedproducteng |
Nee |
Niet in NLg |
Niet in NLg |
Nee |
|
a) Personen die in aanraking komen met feces, zoals werkers in de zorg, leidsters in kindercentra, werkers in riool- en afvalwaterzuivering, enzovoort. |
||||
|
Groep |
|
|---|---|
|
Zwangeren |
Sinds 1989 controle in zwangerschap op dragerschap HBsAg |
|
Pasgeborenen van moeders uit intermediair- en hoog-endemische landen |
Sinds 2003 vaccinatie tegen HBV na geboorte en daarna in het kader van het rijksvaccinatieprogramma |
|
Alle pasgeborenen |
Sinds 2011 vaccinatie tegen HBV in het kader van rijksvaccinatieprogramma |
|
Bloedproducten |
Sinds 1975 screening op hepatitis B |
Doel van de behandeling is door klaring van het virus (HCV-RNA-klaring) het risico op cirrose en levercelcarcinoom te reduceren. Bij acute hepatitis C is een behandeling geïndiceerd als gedurende 3 maanden het HCV-RNA aantoonbaar is, omdat dan de kans op spontane genezing nihil is. De behandeling is dan in meer dan 90% van de gevallen effectief om het virus te klaren. Elke patiënt met chronische hepatitis C komt in aanmerking voor behandeling, tenzij de patiënt niet in staat is om de behandeling te ondergaan. De effectiviteit van de behandeling van chronische hepatitis C voor het klaren van het virus varieert tussen de 60 en 100%. Voor zowel acute als chronische hepatitis C hangt de effectiviteit van de behandeling af van de leeftijd van de patiënt, de mate van levercelschade, het genotype van het virus, de keuze/combinatie van de middelen, de bijwerkingen (vanwege therapietrouw) en eventuele co-infectie met hepatitis-B-virus of hiv. De behandelingsmogelijkheden bestaan uit virusremmers of peginterferon-alfa in combinatie. Bijwerkingen van peginterferon-alfa zijn griepverschijnselen en stemmingsveranderingen, zoals prikkelbaarheid en depressie. Daarnaast komen trombocytopenie en neutropenie veel voor.
De verwachting is dat door nieuwe, nu nog niet goedgekeurde virusremmers, de effectiviteit van de behandeling nog verder zal stijgen. Doordat er steeds nieuwe medicatie beschikbaar is voor de behandeling van hepatitis C verandert de behandeling met enige regelmaat. Om de behandelaars goed op de hoogte te houden van de laatste inzichten is door de NIV en NVMDL de website www.hcvrichtsnoer.nl opgezet. Hier staan de meeste recente aanbevelingen voor de behandeling van hepatitis C. De website wordt met enige regelmaat herzien. Behandeling tijdens zwangerschap is wegens teratogeniteit niet mogelijk.
De informatie in tabel 1 en tabel 2 is overgenomen van de LCI-richtlijnen hepatitis A, B en C. Voor meer informatie over wijze van besmetting bij hepatitis A, B en C wordt verwezen naar de website van het RIVM: www.rivm.nl/cib/infectieziekten.
Hepatitis E
Naar Samenvatting ›De ziekteverschijnselen en het beloop van hepatitis E komen overeen met die van hepatitis A. Hepatitis E kan leiden tot icterus of een verhoogd ALAT. Hygiënemaatregelen zijn niet noodzakelijk; patiënten zijn niet (erg) besmettelijk voor hun omgeving. Hepatitis E geneest meestal spontaan. Bij patiënten die een hoge dosis immunosuppressiva gebruiken, zoals na een orgaantransplantatie, kan de hepatitis-E-infectie chronisch worden en leiden tot cirrose.
Overige virale oorzaken van hepatitis
Naar Samenvatting ›Bij mononucleosis infectiosa en infectie met het CMV kan algehele malaise en een lichte hepatitis optreden. In enkele gevallen is er sprake van icterus.
Levercelschade door gebruik van geneesmiddelen of drugs
Naar Samenvatting ›- Verschillende geneesmiddelen zijn hepatotoxisch, wat kan leiden tot levercelbeschadiging, cholestase of mengvormen hiervan.
- De ernst en mate van reversibiliteit van de levercelschade kan sterk variëren.
- Mogelijke symptomen zijn icterus en algemene extrahepatische symptomen zoals subfebriele verhoging en huiduitslag. Daarnaast kunnen het ALAT en/of gamma-GT licht tot sterk verhoogd zijn.
- De levercelschade kan direct na het starten van de medicatie of pas na langere tijd (maanden tot jaren) tot uiting komen.
- Specifiek kan incidenteel levercelschade optreden bij het gebruik van:
- sommige antibiotica (amoxicilline met clavulaanzuur, macroliden, nitrofurantoïne, tuberculosemiddelen)
- anti-epileptica, antimycotica (itraconazol en terbinafine)
- benzbromaron, allopurinol (in het bijzonder bij verminderde nierfunctie)
- analgetica (onder meer paracetamol)
- statines
- Daarnaast kunnen enkele vrij verkrijgbare geneesmiddelen (zoals vitamine A), kruiden (zilverkaars), alternatieve geneesmiddelen en drugs levercelschade veroorzaken.
Er zijn twee soorten geneesmiddelenhepatotoxiciteit: voorspelbare (intrinsieke) en niet-voorspelbare (idiosyncratische). Intrinsieke hepatotoxiciteit is dosisafhankelijk en treedt snel op nadat met het geneesmiddel is begonnen. Idiosyncratische hepatotoxiciteit is (relatief) onafhankelijk van de dosis, treedt vaak pas op na weken tot maanden (5-90 dagen) en berust nogal eens op een immunologische reactie. In de praktijk is het onderscheid vaak niet te maken. De meestvoorkomende leveraandoeningen veroorzaakt door geneesmiddelen zijn steatose (zie ook Niet-alcoholische vetlever), toxische hepatitis, cholestase en cholestatische hepatitis. De volgende risicofactoren geven een verhoogd risico op geneesmiddelenhepatotoxiciteit: alcoholgebruik, oudere leeftijd, zwangerschap, interactie met andere geneesmiddelen en in de voorgeschiedenis een vergelijkbare reactie op hetzelfde geneesmiddel.
Zeer veel geneesmiddelen kunnen hepatotoxiciteit veroorzaken. Het boek commentaren medicatiebewaking geeft een uitgebreid overzicht. Het Nederlands Bijwerkingencentrum Lareb verzamelt bijwerkingen van geneesmiddelen. (De standaard vermeldt in de hoofdtekst een opsomming van geneesmiddelen, die regelmatig hepatotoxiciteit veroorzaken en door de huisarts worden voor geschreven. Het is niet mogelijk om een complete en actuele lijst te geven. Ook is de vraag of bij starten met bepaalde geneesmiddelen controle van het ALAT is geïndiceerd buiten beschouwing gelaten.
De huisarts kan zelf meerdere vrij toegankelijke en actuele bronnen raadplegen, zoals het Farmacotherapeutisch Kompas en Lareb. Op www.lareb.nl en www.farmacotherapeutischkompas.nl is het mogelijk om per geneesmiddel te zoeken op bijwerkingen. De geneesmiddelen die het vaakst leiden tot levercelschade en verhoogde transaminasewaarden zijn: antibiotica, anti-epileptica en statines. Daarnaast is bekend dat antimycotica en analgetica regelmatig levercelschade veroorzaken.
Levercelschade door alcoholmisbruik
Naar Samenvatting ›Alcoholmisbruik kan op den duur leiden tot levercelschade (zie ook NHG-Standaard Problematisch alcoholgebruik). Eerst ontstaat alcoholische vetlever. Deze is reversibel bij verminderen of staken van het alcoholgebruik. Voortgezet alcoholmisbruik kan leiden tot alcoholische hepatitis en tot levercirrose en levercelcarcinoom. Alcoholische vetlever geeft hooguit aspecifieke klachten en kan gepaard gaan met een stijging van het ALAT.
Niet-alcoholische vetlever
Naar Samenvatting ›- Bij niet-alcoholische vetlever (NAFLD) treedt vetstapeling in de lever op. Dit komt vooral voor bij patiënten met diabetes mellitus type 2, dyslipidemie en obesitas.
- Patiënten met NAFLD hebben een verhoogd risico op hart- en vaatziekten (tweemaal verhoogd) en op sterfte (1,5 maal verhoogd) in vergelijking met de algemene populatie.
- NAFLD geeft geen klachten; het gaat vaak om een toevalsbevinding die aan het licht komt door een (licht) verhoogd ALAT bij laboratoriumonderzoek of doordat leververvetting gezien wordt bij een echografie van het abdomen.
- De diagnose NAFLD is pas mogelijk nadat andere (regelmatig voorkomende) oorzaken zijn uitgesloten.
Bij niet-alcoholische steatosis hepatis (NAFLD) is er vetstapeling in de lever zonder dat er sprake is van overmatig alcoholgebruik, hepatotoxische medicatie of een erfelijke aandoening. De diagnose NAFLD wordt gesteld per exclusionem, nadat eerst andere belangrijke oorzaken van leverfunctiestoornissen zijn uitgesloten. Een klein deel van de patiënten met NAFLD heeft of ontwikkelt niet-alcoholische steatohepatitis (NASH). Dit kan op termijn leiden tot leverfibrose en bij een klein deel van de patiënten met cirrose tot levercelcarcinoom. NASH kan alleen worden vastgesteld door middel van een leverbiopsie. Volgens de huidige schattingen ligt de prevalentie van NAFLD in de algemene bevolking rond de 20% en van NASH rond de 2-3%. Bij een NASH is er sprake van een leverontsteking. NAFLD is geassocieerd met obesitas, dyslipidemie en diabetes mellitus.
Een meta-analyse onderzocht het natuurlijke beloop van NAFLD. In totaal zijn 40 onderzoeken over het natuurlijke beloop geïncludeerd. De belangrijkste conclusies zijn:
- 7 onderzoeken (n = 18.048) toonden een verhoogd risico aan op het eindpunt sterfte in de NAFLD-groep in vergelijking met de algemene populatie, gecorrigeerd voor andere risicofactoren: gepoolde OR 1,57 (95%-BI 1,18 tot 2,10).
- De belangrijkste oorzaken van de sterfte in de NAFLD-groep waren een maligniteit (28%), ischemische hartaandoeningen (25%) en leveraandoeningen (13%).
- 8 onderzoeken (n = 11.018, NAFLD echografisch aangetoond) toonden een verhoogd risico aan op cardiovasculaire events, gecorrigeerd voor andere cardiovasculaire risicofactoren: gepoolde OR 2,05 (95%-BI 1,81 tot 2,31).
- De meta-analyse maakt in een subgroepanalyse onderscheid tussen NAFLD en NASH voor het risico op sterfte (5 onderzoeken, n = 559). In de NASH-groep was het risico op sterfte door alle oorzaken hoger dan in de NAFLD-groep: OR 1,81 (95%-BI 1,24 tot 2,66) evenals het risico op sterfte door een leverziekte: OR 5,71 (95%-BI 2,31 tot 14,13). Er was geen verschil in risico op sterfte door hart- en vaatziekten tussen de beide groepen, OR 0,91 (95%-BI 0,42 tot 1,98).
- Bij een NASH is het risico op verdere progressie van de fibrose na 4 en 6 jaar respectievelijk 25 tot 30% en 50%.
Onderzoek van Matteoni (n = 132) liet zien dat 25% van de patiënten met een NASH cirrose ontwikkelt in een periode van 3-8 jaar. Bij patiënten met NAFLD gaat een verhoogd ALAT gepaard met een groter risico op het optreden van een belangrijke cardiovasculaire gebeurtenis dan bij patiënten met een normaal ALAT.
Conclusie
NAFLD gaat gepaard met een verhoogd risico op cardiovasculaire aandoeningen (grofweg 2 keer) en totale sterfte (grofweg 1,5 keer).
De gouden standaard voor het aantonen van NAFLD is een leverbiopsie. Een leverbiopsie is voor de huisarts niet beschikbaar. Daarnaast is het verrichten van een leverbiopsie niet wenselijk gezien het risico op complicaties (bloedingen en pijn in 1-3% van de gevallen) en op mortaliteit (0,01%). Gezien de risico’s van een leverbiopsie en het ontbreken van consequenties voor het beleid, wordt deze optie hier verder niet besproken.
Echografie is wel beschikbaar voor de huisarts. Een meta-analyse (46 onderzoeken, n = 4715, leeftijd 11 tot 89 jaar) vergeleek onder meer echografie met de gouden standaard leverbiopsie voor het aantonen van NAFLD. De kwaliteit van het bewijs is afgewaardeerd met één niveau naar matig vanwege de kans op vertekening van de resultaten. Bij slechts 65% van de onderzoeken was er een prospectieve opzet en slechts bij 62% was de onderzoekspopulatie representatief. Er waren 28 onderzoeken (n = 3190) over echografie beschikbaar. De patiënten met NAFLD zijn onderverdeeld in 3 groepen naar de mate van steatose. Bij groep 1 was er maximaal 10% steatose. Bij groep 2 minimaal 10% en maximaal 25% steatose. Bij groep 3 minimaal 25% steatose. De sensitiviteit van echografie was respectievelijk 73,3%, 90,5% en 85,7%. De specificiteit was respectievelijk 84,4%, 69,6% en 85,2%.
Conclusie
De sensitiviteit van echografie varieert tussen de 73 en 91% (kwaliteit van het bewijs matig). Daarmee lijken de testeigenschappen van echografie voldoende om steatose aan te tonen in de huisartsenpraktijk.
Richtlijnen diagnostiek
Naar Samenvatting ›Patiëntgroepen en risico’s
Naar Samenvatting ›- Er zijn weinig klachten dan wel symptomen specifiek voor een leveraandoening. Wees bij de volgende patiëntengroepen bedacht op een leveraandoening:
- patiënten met icterus, bij wie geen verdenking bestaat op pathologie van de galblaas, galwegen of pancreas
- patiënten met klachten die een risicocontact hebben gehad of die behoren tot een risicogroep voor hepatitis B of C (zie tabel 1 en tabel 2)
- patiënten met algehele malaise bij wie tevens verdenking bestaat op levercelschade door alcoholmisbruik of recent drugsgebruik
- patiënten met algehele malaise bij wie tevens verdenking bestaat op levercelschade door geneesmiddelen, omdat recent een behandeling met een geneesmiddel is gestart of de dosering is gewijzigd
- Veel personen met een (chronische) leveraandoening hebben geen klachten. Overweeg daarom het risico van een leveraandoening bij spreekuurbezoekers, indien:
- de patiënt risicocontacten heeft (gehad) voor (chronische) hepatitis B of C (zie tabel 1)
- de patiënt behoort tot een risicogroep voor (chronische) hepatitis B of C (zie tabel 2)
- er sprake is van problematisch alcoholgebruik of drugsgebruik
- bij het lichamelijk onderzoek een vergrote lever wordt aangetroffen (die niet kan worden toegeschreven aan hartfalen)
- de transaminasewaarden verhoogd zijn (zie Aanvullend onderzoek)
Goed wetenschappelijk onderzoek naar de voorspellende waarde in de huisartsenpraktijk van (combinaties van) klachten, symptomen en kenmerken die met leveraandoeningen geassocieerd worden, is niet gevonden. Wetenschappelijk onderbouwde richtlijnen voor anamnese en lichamelijk onderzoek voor de vaststelling of uitsluiting van een leveraandoening of voor het maken van een onderscheid tussen de verschillende leveraandoeningen kunnen daarom niet worden geformuleerd. Om die reden geeft deze standaard een globaal raamwerk voor de diagnostiek.
Anamnese
Naar Samenvatting ›Ga de volgende klachten en risicofactoren meer of minder uitgebreid na, afhankelijk van de vermoede leverproblematiek:
- duur en beloop van eventuele klachten
- (seksueel) risicocontact in het verleden (zie tabel 1)
- patiënt behoort tot een risicogroep (zie tabel 2)
- leveraandoeningen, hepatitis of levercelcarcinoom in de familie of bij de partner
- recent verblijf in een land waar hepatitis A veel voorkomt
- doorgemaakte hepatitis A, B of C en eventuele behandeling
- vaccinatie tegen hepatitis A of B
- gebruik van medicatie, kruiden, vitamine A (met name recent gestart of in gewijzigde dosering, zie Levercelschade door gebruik van geneesmiddelen of drugs voor de meest voorkomende geneesmiddelen die hepatoxiciteit veroorzaken)
- gebruik van alcohol of drugs
- aanwezigheid van diabetes mellitus, hypertensie of afwijkend lipidenspectrum in de voorgeschiedenis
Lichamelijk onderzoek
Naar Samenvatting ›Verricht het volgende onderzoek:
- mate van ziek zijn
- inspectie van de sclerae op gele kleur
- percussie en palpatie van de lever-, galblaas- en miltregio
- bij vermoeden van niet-alcoholische vetlever:
- gewicht en lengte en/of middelomtrek
- bloeddruk
- bij vermoeden van cirrose:
- huidinspectie (icterus, ‘spider’-naevi, erythema palmare)
- gynaecomastie, wapperende tremor
- onderzoek abdomen (ascites, splenomegalie en veneuze collateralen in de buikwand)
Aanvullend onderzoek
Naar Samenvatting ›Virushepatitis
Naar Samenvatting ›- Volwassen patiënten (> 16 jaar) met icterus bij wie geen verdenking bestaat op pathologie van de galblaas, galwegen of pancreas:
- ALAT en serologie voor acute hepatitis A, indien negatief: serologie voor hepatitis E, en op indicatie voor acute hepatitis B en C
- Kinderen (0-16 jaar) met icterus: de diagnostiek vindt plaats op basis van risicoschatting en is vooral gericht op hepatitis A:
- ALAT en serologie op acute hepatitis A
- indien serologie op acute hepatitis A negatief: serologie op EBV, CMV en hepatitis E
- indien deze testen ook negatief: serologie voor acute hepatitis B en op indicatie acute hepatitis C
- Patiënten met algehele malaise bij wie tevens verdenking bestaat op virushepatitis (behorend tot een risicogroep of vanwege risicocontact voor virushepatitis):
- ALAT en serologie op hepatitis B, op indicatie chronische hepatitis C
- Spreekuurbezoekers zonder klachten maar met een risicocontact in de voorgeschiedenis: maak op grond van afkomst en gedrag (nu of in het verleden) een inschatting of onderzoek nodig is:
- ALAT en serologie op hepatitis B, op indicatie serologie naar acute of chronische hepatitis C (afhankelijk van tijdsduur na risicocontact)
- Spreekuurbezoekers afkomstig uit intermediair- en hoog-endemische landen zonder klachten (zie tabel 2): overweeg om de patiënt aan te bieden om eenmalig te testen:
- ALAT en serologie op hepatitis B en chronische hepatitis C
- Patiënten bij wie in het verleden de diagnose hepatitis B of C is gesteld, die niet (succesvol) zijn behandeld of niet onder controle zijn van een hepatitisbehandelcentrum:
- ALAT en serologie hepatitis B of C
De werkgroep heeft besproken of de huisarts actief alle patiënten met een verhoogd risico op chronische hepatitis B en C in de eigen praktijk moet opsporen via het HIS, omdat behandeling voor patiënten met chronische hepatitis B of C gezondheidswinst oplevert. De werkgroep heeft besloten dit niet aan te bevelen op de volgende gronden:
- Opsporing via het HIS is met de huidige registraties slecht uitvoerbaar. Een deel van de patiënten wordt gemist, een ander deel onterecht geïdentificeerd als patiënt met een mogelijk verhoogd risico. Dit leidt tot een grote workload bij praktijken en onnodige onrust bij een deel van de patiënten.
- Opsporing van hoogrisicopatiënten is een taak van meerdere instanties, waaronder zeker ook van de GGD, verslavingszorg en het RIVM.
- Opsporing lijkt alleen doelmatig bij een geïntegreerde aanpak.
De werkgroep heeft daarom besloten het actief aanbieden van diagnostiek naar hepatitis B en C bij patiënten met een verhoogd risico op chronische hepatitis B en C te beperken tot spreekuurbezoekers.
Aanbeveling
Overweeg om spreekuurbezoekers afkomstig uit intermediair- en hoog-endemische landen zonder klachten aan te bieden om eenmalig te testen op chronische hepatitis B en C.
Overige overwegingen
Naar Samenvatting ›- Bij een besmetting door een seksueel risicocontact is nadere diagnostiek naar soa’s nodig, zie NHG Standaard Het soa-consult.
- Overweeg om bij spreekuurbezoekers afkomstig uit intermediair en hoog-endemische landen ook een hiv-test aan te vragen.
- Het laboratorium doet over het algemeen routinematig een aantal vervolgbepalingen:
- Als hepatitis B-serologie wordt aangevraagd, bepalen laboratoria naast het HBsAg ook altijd antistoffen tegen het anti-HB-core (zie tabel 4). De reden hiervoor is dat circa 3 maanden na het begin van een hepatitis B-infectie bij spontane klaring het HBsAg verdwijnt, terwijl het anti-HBs soms nog niet positief is (het zogeheten ‘open-core-window’). Het anti-HB-core blijft positief, ook na verdwijnen van HBsAg, zodat dan in elk geval bekend is dat een besmetting met HBV heeft plaatsgevonden.
- Als hepatitis C-serologie wordt aangevraagd bij een risicocontact ≥ 10 weken, bepaalt het laboratorium bij een positief anti-HCV automatisch het HCV-RNA.
- Bij gebruik van een probleemgeoriënteerd laboratoriumformulier doet het laboratorium bij positieve virushepatitisserologie automatisch de benodigde vervolgbepalingen.
- Als de aangevraagde hepatitisserologie negatief is, ga dan andere oorzaken van de klachten na (alcohol, medicijngebruik, eventuele infectie met EBV, CMV of HEV). Het is ook mogelijk dat de periode tussen besmetting en bepaling van de serologie te kort is geweest. Herhaal de bepalingen naar hepatitis B en/of C zo nodig na 1 maand, bij een sterk vermoeden van een acute virushepatitis (klachten en bekend besmettingsmoment).
- Bij een reëel besmettingsgevaar met negatieve serologie en bij vervolgdiagnostiek bij positieve virushepatitisserologie, verricht het laboratorium vaak automatisch verdere bepalingen. Ga na bij het preferente laboratorium wat gebruikelijk is, of hier regionaal afspraken over zijn gemaakt en welke gegevens het laboratorium nodig heeft om automatische vervolgdiagnostiek te kunnen uitvoeren.
- Noteer altijd de relevante achtergrondinformatie op het aanvraagformulier, zoals indicatie, eerste ziektedag, klachten, datum mogelijk besmettingsmoment en vaccinatiestatus.
- Laat bij acute klachten en bij nadere diagnostiek naar een verhoogd ALAT spijtserum afnemen.
|
Indicatie |
Eerste bepaling |
Vervolg bij positieve eerste test |
Uitleg bij de bepaling |
Interpretatie |
|---|---|---|---|---|
|
Algemeen |
ALAT |
|
|
Verhoging kan passen bij leveraandoening. |
|
Hepatitis A, acuut |
IgM-anti-HAV |
|
Hepatitis-A-antistoffen |
Bewijzend voor acute hepatitis A |
|
Hepatitis B, |
HBsAg* |
|
Hepatitis-B-oppervlakteantigeen |
Aantoonbaar ca. 1 maand na de besmetting |
|
|
HBsAg > 6 maanden na besmetting |
Hepatitis B-oppervlakteantigeen |
Risicocontact > 6 maanden geleden óf risicocontact onbekend óf HBsAg positief > 6 maanden geleden: bewijzend voor chronische hepatitis B |
|
|
Hepatitis-B-vaccinatie |
Anti-HBs |
|
Antistoffen tegen HBsAg |
Bewijzend voor een geslaagde vaccinatie |
|
Hepatitis C, acuut |
HCV-RNA |
|
Hepatitis-C-RNA |
Aantoonbaar 7 dagen na besmetting |
|
|
HCV-RNA |
|
Herhaal na 3 maanden vanwege kans op spontane genezing en inzetten behandeling gebeurt pas na 3 maanden. |
|
|
Hepatitis C, chronisch |
Anti-HCV‡ |
|
Antistoffen tegen HCV |
Aantoonbaar 10 weken na besmetting |
|
|
HCV-RNA |
|
Aanwezigheid bewijzend voor een hepatitis C |
|
|
Hepatitis C in het verleden |
HCV-RNA |
|
|
Aanwezigheid bewijzend voor een chronische hepatitis C |
|
Hepatitis E |
IgM-anti-HEV |
|
|
Positieve uitslag bewijzend voor acute hepatitis E |
|
* Zie voor handelwijze bij een positief HBsAg bijlage: stroomschema 1. |
||||
Levercelschade door een geneesmiddel, drugs of alcohol
Naar Samenvatting ›Bepaal het ALAT bij patiënten met klachten van algehele malaise bij gebruik van een mogelijk hepatotoxisch geneesmiddel, drugs of bij overmatig alcoholgebruik.
Verhoogd ALAT (1,5-10 maal boven de normaalwaarde)
Naar Samenvatting ›Onderzoek het volgende bij patiënten met ALAT-waarden van 1,5-10 maal boven de normaalwaarde.
- Bepaal het ALAT opnieuw na circa 4 weken en vraag spijtserum aan.
- Indien opnieuw verhoogd: aanvullend onderzoek conform stroomschema 3.
- Overweeg bij patiënten met een verhoogd risico op vetlever echografie van de lever, om NAFLD aan te tonen.
- Inventariseer bij (risico op) NAFLD het cardiovasculair risico, zie hiervoor NHG-Standaard Cardiovasculair risicomanagement (CVRM).
ALAT en ASAT (alanine- respectievelijk aspartaataminotransferase) zijn transaminasen die in de lever maar ook in andere weefsels actief zijn. ALAT komt hoofdzakelijk voor in levercellen en in mindere mate in skeletspieren, de hartspier en nier- en pancreasweefsel. ASAT komt voor in levercellen, de hartspier en de skeletspieren, en in mindere mate in andere organen. Voor levercelbeschadiging is de ALAT-bepaling het meest specifiek. Een geringe verhoging van ALAT (tot 1,5 maal van de normaalwaarde) heeft vaak geen klinische betekenis bij een patiënt die verder niet ziek is; 5% van de gezonde personen valt immers buiten de referentiewaarden (gedefinieerd als gemiddelde ± 2 SD’s).
Acute levercelschade, bijvoorbeeld ten gevolge van virushepatitis, is waarschijnlijk bij een ALAT > 300 U/l (sensitiviteit 96%, specificiteit 94%) en een ASAT > 200 U/l (sensitiviteit 91%, specificiteit 95%).
De hoogste waarde van ALAT is bij virushepatitis tien- tot honderdmaal de bovengrens van normaal, bij alcoholische hepatitis twee- tot achtmaal en bij levercelschade door intoxicatie of ischemie meer dan veertigmaal tot zelfs meer dan honderdmaal de bovengrens van normaal.
De ernst van de levercelschade wordt beter weerspiegeld door de protrombinetijd dan door de hoogte van de transaminasewaarden (die eerder gerelateerd zijn aan de oorzaak van de levercelschade). Een protrombinetijd van meer dan vier seconden boven de referentiewaarde duidt op ernstige levercelschade.
Gamma-GT is een gevoelige maar aspecifieke maat voor levercelschade of leveraandoeningen; bepaling ervan heeft geen toegevoegde waarde om de oorzaak van de levercelschade te achterhalen.
Conclusie
De bepaling van het ALAT lijkt het meest geschikt voor de initiële diagnostiek naar leveraandoeningen, gezien de hogere specificiteit van het ALAT voor leveraandoeningen in vergelijking met de andere leverenzymen. Het risico op een leveraandoening is pas verhoogd vanaf een ALAT anderhalf maal boven de normaalwaarde. Het risico neemt toe met de hoogte van het ALAT en als het ALAT bij herhaling verhoogd is.
Voor beantwoording van de vraag ‘Wat is de juiste afkapwaarde van ALAT voor het uitsluiten van een leveraandoening bij patiënten in de eerste lijn?’ is een systematische literatuursearch uitgevoerd. Er is één onderzoek gevonden dat gedeeltelijk op deze vraag ingaat. In dit prospectieve cohortonderzoek, uitgevoerd in Engeland in de eerste lijn, was het doel een effectieve strategie in de eerste lijn te ontwikkelen om de diagnose virale hepatitis te stellen bij patiënten met verhoogde leverenzymen. Hiervoor zijn 1236 asymptomatische volwassenen patiënten geïncludeerd met verhoogde leverenzymen (ALAT, ASAT, alkalische fosfatase, bilirubine of GGT boven de normaalwaarde; de normaalwaardes zijn niet beschreven). Virale hepatitis werd bij 13 patiënten aangetoond (9 HBV en 4 HCV). Bij 8 van deze 13 patiënten was het ALAT verhoogd, bij 6 patiënten meer dan 2 keer de bovengrens van de normaalwaarde. Bij de 13 patiënten zijn de leverenzymen na gemiddeld 1 maand opnieuw bepaald, bij 11 waren deze wederom afwijkend en bij 2 waren de bepalingen incompleet. Van de 13 patiënten waren 11 afkomstig uit een hoog-endemisch hepatitisland. Met de data uit deze groep zijn zeven strategieën vergeleken. De eindpunten voor de verschillende strategieën waren de kosten in de eerste lijn en de sensitiviteit en positief voorspellende waarde voor het aantonen van hepatitis B of C. De resultaten zijn weergegeven in tabel 5. Met de sensitiviteit wordt bedoeld: het percentage hepatitispatiënten dat met de strategie (en daaropvolgende serologie) daadwerkelijk werd gevonden (casussen gevonden/hepatitis casussen). Met positief voorspellende waarde wordt bedoeld: het percentage hepatitispatiënten van de deelnemers bij wie de betreffende teststrategie positief was (casussen gevonden/serologie testen).
| * | n | Hepatitiscasussen | Serologietesten | Casussen gevonden | Sensitiviteit(%) | Positief voorspellende waarde %(95%-BI) | Kosten per ontdekte patiënt (£) |
|---|---|---|---|---|---|---|---|
| A | 1124 | 11 | 955 | 11 | 100 | 1,15 (0,64-2,05) | 4965 |
| B | 1064 | 12 | 418 | 8 | 67 | 1,91 (0,97-3,73) | 2270 |
| C | 1064 | 12 | 77 | 6 | 50 | 7,79 (3,62-15,98) | 558 |
| D | 1208 | 13 | 170 | 11 | 85 | 6,47 (3,65-11,21) | 641 |
| E | 1041 | 12 | 16 | 5 | 42 | 31,25 (14,16-55,60) | 142 |
| F | 1041 | 12 | 215 | 11 | 92 | 5,12 (2,88-8,93) | 868 |
| G | 1236 | 13 | 1236 | 13 | 100 | 1,05 (0,62-1,79) |
3853 |
| * Serologische bepaling van HBV en HCV werd uitgevoerd op indicatie volgens de volgende strategieën: A. Bij een bij herhaling afwijkende leverenzymwaarde. B. Bij eenmalig afwijkend ALAT. |
|||||||
Het onderzoek kent een aantal beperkingen. De grootste beperking is dat de vraag niet helemaal aansluit bij de zoekvraag. Er is een beperkt aantal patiënten met hepatitis (n = 13). De normaalwaardes van de leverenzymen zijn niet vermeld.
Conclusie
Het land van herkomst is een belangrijke risicofactor voor de aanwezigheid van virushepatitis. Er is geen duidelijke afkapwaarde voor het ALAT. Bij een ALAT hoger dan 2 keer de normaalwaarde neemt in vergelijking met een net verhoogde ALAT de positief voorspellende waarde voor de aanwezigheid van virushepatitis toe, maar wordt de helft van het aantal virushepatitiden gemist.
Van conclusie naar aanbeveling
De werkgroep kiest er op pragmatische gronden en ervaring voor om een ALAT van 1,5 maal boven de normaalwaarde als afkapwaarde voor aanvullend onderzoek te hanteren, waarbij die ALAT herhaald (2 maal) bepaald en afwijkend is. Het herhalen ALAT past in de werkwijze van de huisarts. Hiermee wordt voorkomen dat alle minimaal verhoogde ALATs worden geanalyseerd die eigenlijk nog binnen de normaalwaardes vallen, zie Verhoogd ALAT (1,5-10 maal boven de normaalwaarde). Door te kiezen voor een afkapwaarde van 1,5 maal boven de normaalwaarde wordt geen virushepatitis gemist. Daarnaast kiest de werkgroep ervoor om bij patiënten uit de risicogroep of met risicocontact voor virushepatitis sneller hepatitisserologie te laten bepalen vanwege de grotere voorafkans op hepatitis.
Aanbeveling
Bij een ALAT 1,5-10 maal boven de normaalwaarde herhaalt de huisarts de bepaling. Indien het ALAT blijvend verhoogd is, doet de huisarts aanvullend onderzoek op basis van risicogroepen, risicocontacten, alcohol- en medicijngebruik en verhoogd risico op steatosis (DM type 2, dyslipidemie of obesitas), zie stroomschema 3. Zie voor ALAT-waarden > 10 maal de normaalwaarde (zie Consultatie en verwijzing).
Evaluatie
Naar Samenvatting ›Virushepatitis
Naar Samenvatting ›Acute hepatitis A
Naar Samenvatting ›Klachten, icterus en IgM-anti-HAV positief.
De sensitiviteit en specificiteit van enkele veelgebruikte tests op respectievelijk hepatitis A, B en C zijn als volgt.
- IgM-anti-HAV: afhankelijk van het soort assay waarmee de IgM-anti-HAV werd bepaald, werd in een populatie van enerzijds Chinese mensen met een acute hepatitis en anderzijds controlepersonen (mensen zonder leveraandoening) een sensitiviteit van 91 tot 98% gevonden en een specificiteit van 96 tot 100% voor het aantonen van een hepatitis-A-virusinfectie.
- HBsAg: In een onderzoek over de gevoeligheid van immunoassays voor de detectie van HBsAg waren de specificiteit en sensitiviteit respectievelijk 99,8% en 95,9%.
- Anti-HCV: In een onderzoek over de gevoeligheid van immunoassays voor de detectie van anti-HCV varieerde de specificiteit tussen de 96,5% en 98,8%. De sensitiviteit was telkens 100%.
Foutpositieve uitslagen van hepatitis A, B en C door kruisreacties met antistoffen voor CMV, EBV of HEV kunnen vóórkomen, zodat men bij de interpretatie van de uitslag rekening moet houden met het klinisch beeld en risicogedrag van de patiënt.
Hepatitis B
Naar Samenvatting ›Maak onderscheid tussen:
- Acute hepatitis B:
- Risicocontact < 6 maanden geleden óf HBsAg negatief < 6 maanden geleden
- HBsAg positief
- anti-HB-core positief
- Chronische hepatitis B:
- Risicocontact > 6 maanden geleden óf risicocontact onbekend óf HBsAg positief > 6 maanden geleden
- HBsAg positief
- anti-HB-core positief
- Hepatitis B-vaccinatie:
- anti-HBs positief
- Functioneel genezen hepatitis B:
- HBsAg negatief
- anti-HB-core positief
- anti-HBs positief of anti-HBs negatief, nadat deze eerder positief was
Hepatitis C
Naar Samenvatting ›- Acute hepatitis C:
- risicocontact < 6 maanden geleden
- HCV-RNA positief
- Chronische hepatitis C:
- risicocontact > 6 maanden geleden
- anti-HCV positief én
- HCV-RNA positief
- Genezen of doorgemaakte hepatitis C:
- anti-HCV positief én
- HCV-RNA negatief
Het virus-RNA (HCV-RNA) is zeven dagen na besmetting aantoonbaar en blijft aantoonbaar bij een chronische hepatitis C. Bij spontane genezing of een geslaagde behandeling verdwijnt het HCV-RNA. Antilichamen tegen het hepatitis-C-virus (anti-HCV) zijn aantoonbaar na ongeveer tien weken en blijven aanwezig, ook na genezing [RIVM 2012].
Overige
Naar Samenvatting ›Infectie met EBV of CMV. Het verdere beleid bij deze infecties valt buiten het bestek van deze standaard.
Overige aandoeningen
Naar Samenvatting ›- Overweeg bij patiënten met een bij herhaling licht verhoogd ALAT (1,5-10 maal boven de normaalwaarde) en negatieve virushepatitisserologie de volgende diagnoses:
- Levercelschade door een geneesmiddel; vaak is de relatie niet eenduidig en kan de diagnose pas worden gesteld indien het ALAT na staken van het geneesmiddel daalt.
- Levercelschade door alcoholgebruik; de diagnose is waarschijnlijker indien na staken van het alcoholgebruik het ALAT daalt. Het ALAT is meestal na 3 maanden genormaliseerd.
- Niet-alcoholische vetlever; dit wordt vermoed bij een (licht) verhoogd ALAT (1,5-10 maal boven de normaalwaarde) met daarbij obesitas, diabetes mellitus of dyslipidemie. Het vermoeden wordt ondersteund door een vergrote lever bij lichamelijk onderzoek of aanwijzingen voor steatose bij echografie van de lever. Niet-alcoholische vetlever is een diagnosis per exclusionem; andere oorzaken zijn onwaarschijnlijk dan wel uitgesloten.
- Overweeg bij (zeer) hoge waarden van ALAT (arbitrair > 10 maal de normaalwaarde) acute levercelschade door intoxicatie of een toxische reactie ten gevolge van geneesmiddelen.
- Overweeg bij icterus met normale ALAT én negatieve hepatitisserologie hemolytische anemie of het syndroom van Gilbert. Het verdere beleid valt buiten het bestek van deze standaard.
- Overweeg de diagnose cirrose bij een of meerdere tekenen hiervan bij het lichamelijk onderzoek.
Richtlijnen beleid
Naar Samenvatting ›Virushepatitis
Naar Samenvatting ›Algemene voorlichting virushepatitis
Naar Samenvatting ›- Leg uit dat virushepatitis een besmettelijke virusinfectie van de lever is.
- Moeheid is soms ernstig en kan langdurig aanhouden (enkele maanden), maar bedrust is niet nodig.
- Tijdens de acute fase wordt het gebruik van alcohol (op pathofysiologische gronden) en geneesmiddelen die voornamelijk door de lever worden afgebroken ontraden. Bij een stringente indicatie kan de dosering van het geneesmiddel worden aangepast in overleg met de apotheker.
- Specifieke dieetadviezen zijn niet nodig, maar in de herstelperiode is er soms een intolerantie voor vet en is het beter geen alcohol te gebruiken.
De Nederlandse Leverpatiënten Vereniging (NLV) heeft in 2014 een rapport uitgebracht over het patiëntenperspectief van leverpatiënten bij een aantal leveraandoeningen, waaronder hepatitis C. De belangrijkste aanbevelingen bij hepatitis C voor de huisarts waren: de diagnose wordt face-to-face aan de patiënt overgebracht, op de wijze van een slechtnieuwsgesprek; de behandelaar zet zich in voor het slechten van het sociale taboe en de stigma’s die er heersen rondom patiënten met hepatitis C; en als de patiënt daar behoefte aan heeft, wordt het transmissiemoment onderzocht.
Preventie besmetting van anderen
Naar Samenvatting ›Geef patiënten met hepatitis B en C de volgende adviezen, ter voorkoming van besmetting van anderen.
- Geef adviezen ter voorkoming van contact met bloed van niet-geïnfecteerden. Adviseer de patiënt er zorg voor te dragen dat anderen niet in contact komen met voorwerpen waar mogelijk zijn bloed aan zit: tandenborstels, scheerapparatuur, naalden, spuiten, verbandmateriaal, maandverband en medische gebruiksartikelen.
- Daarnaast dient de patiënt op te letten bij huidlaesies zoals wondjes, open eczeem en impetigo.
- Aan het gezamenlijk gebruik van tafelbestek, de badkamer, kleren en aan gewoon ‘aanraakcontact’ is geen risico verbonden.
- Bespreek de consequenties ten aanzien van een eventuele zwangerschap (overdracht van moeder op kind).
- Motiveer de patiënt om met de seksuele contacten van het afgelopen half jaar te bespreken dat deze zich dienen te laten testen.
- Wijs de patiënt ook op thuisarts.nl.
- Ten aanzien van werk, school of dagverblijf zijn bij normaal sociaal contact geen speciale maatregelen nodig. In specifieke situaties moet overleg plaatsvinden tussen de direct verantwoordelijken zoals de bedrijfsarts of arbodienst en/of adviserend deskundigen voor een inschatting van het risico op bloed-bloedcontact. Dit geldt vooral indien de geïnfecteerde werkt in de gezondheidszorg en daar risicovolle handelingen verricht, of indien het een kind betreft met risicogedrag, zoals bijten.
De hygiënische maatregelen bij hepatitis B en C zijn gebaseerd op de adviezen van de LCI. Onderzoek naar het effect van dergelijke maatregelen is niet gevonden.
In 2012 heeft de commissie Preventie iatrogene transmissie van HBV, HCV en hiv van het Centrum voor Infectieziektenbestrijding een richtlijn gepubliceerd ter preventie van iatrogene hepatitis B. Daarnaast zijn er algemenere richtlijnen over patiënten met hepatitis B, hepatitis C en hiv die in de gezondheidszorg werken.
Er zijn twee soorten risico’s. Het eerste is dat een zorgverlener besmet met HBV, HCV of hiv een patiënt besmet; het tweede dat een patiënt/cliënt een zorgverlener besmet.
Bij een besmette zorgverlener bepaalt de commissie Preventie iatrogene transmissie van HBV, HCV en hiv of deze mag werken. Hierbij speelt een rol hoe risicovol de handelingen zijn: hoe invasiever de handelingen, hoe risicovoller. Ook de hoogte van de viral load van de zorgverlener is van belang voor het risico: hoe hoger, hoe meer besmettingsgevaar.
In de specifieke situatie waarin een werkende het risico loopt besmet te worden, bijvoorbeeld door een kind met chronische hepatitis B dat bijtgedrag vertoont, bepaalt de GGD op basis van een risicoanalyse of vaccinatie van de werkende geïndiceerd is.
Transmissiemoment en stigma’s
Naar Samenvatting ›- Probeer samen met de patiënt het transmissiemoment te achterhalen; dit geldt vooral bij hepatitis B en C.
- Ga bij hepatitis B en C in op taboes en stigma’s die mogelijk bij de patiënt of zijn omgeving leven (zie Algemene voorlichting virushepatitis). Hier zijn soms meerdere consulten voor nodig.
Thuisarts
Naar Samenvatting ›Verwijs naar de informatie over leverontsteking op thuisarts.nl, die is gebaseerd op deze NHG-Standaard.
Hepatitis A
Naar Samenvatting ›Voorlichting en advies
Naar Samenvatting ›Bij hepatitis A is het beloop vrijwel altijd gunstig. Geef ter voorkoming van besmetting van anderen de volgende specifieke adviezen.
Patiënten met hepatitis A
Naar Samenvatting ›- Raad de patiënt aan thuis te blijven van school of werk tot 1 week na het ontstaan van de icterus. Overleg met de GGD bij twijfel over het toestaan van crèchebezoek; hoogstwaarschijnlijk heeft besmetting van andere crèchebezoekers al plaatsgevonden en zijn er asymptomatische patiënten.
- Adviseer gedurende deze periode strikte hygiëne. Dit betekent:
- contact met feces vermijden, handen wassen met zeep na toiletgebruik en vóór het bereiden van eten, eventueel gebruik van zeeppompjes
- toilet, trekker/spoelknop en deurknop minstens ieder dagdeel huishoudelijk schoonmaken en indien mogelijk eigen toilet gebruiken
- bij verzorging van een baby met hepatitis A: wegwerpluiers gebruiken en het aankleedkussen huishoudelijk reinigen na iedere verzorging; na verzorging handen wassen met water en zeep
Het advies om thuis te blijven van school tot één week na het ontstaan van de icterus geldt voor kinderen vanaf de basisschoolleeftijd. Op een crèche of kinderdagverblijf kunnen kinderen met hepatitis A toegelaten worden na overleg met de GGD. Gezien het veelvuldig voorkomen van een asymptomatisch beloop bij kinderen tot 4 jaar leidt wering van een enkel kind niet tot onderbreking van de transmissie. Een uitzondering geldt voor een kind dat met een symptomatische hepatitis A van vakantie terugkomt en dus nog geen andere kinderen besmet kan hebben.
De hygiënische maatregelen bij hepatitis A zijn gebaseerd op de adviezen van de LCI.
Personen uit de directe omgeving van een patiënt met hepatitis A
Naar Samenvatting ›Adviseer strikte hygiëne tot 1 week na begin van de klachten van de patiënt (koorts of icterus). Daarnaast wordt immunisatie van personen uit de directe omgeving geadviseerd. Deze wordt uitgevoerd door of met de GGD afgestemd. Vaccinatie met hepatitis-A-vaccin als post-expositieprofylaxe binnen 8 dagen (tot maximaal 14 dagen) na contact met de patiënt heeft vrijwel altijd de voorkeur (zie Richtlijnen ter preventie van virushepatitis).
Vaccinatie heeft vrijwel altijd de voorkeur. Dit geeft in 95 tot 100% van de gevallen afdoende respons; de duur van de bescherming na een eerste dosis is ten minste 1 jaar, na de tweede vaccinatie ten minste 15 jaar, waarschijnlijk zelfs tot 25 jaar. Passieve immunisatie tegen hepatitis A geeft bij 90% van de geïmmuniseerden effectieve bescherming. De werkingsduur is 4 tot 6 weken bij een standaarddosering.
Thuisarts
Naar Samenvatting ›Verwijs naar de informatie over leverontsteking op thuisarts.nl, die is gebaseerd op deze NHG-Standaard.
Controles
Naar Samenvatting ›Controle van de leverfuncties is niet nodig omdat dit geen consequenties heeft voor het beleid.
Hepatitis B
Naar Samenvatting ›Voorlichting en advies
Naar Samenvatting ›Geef ter voorkoming van besmetting van anderen, naast de algemene adviezen, de volgende specifieke adviezen.
Patiënten met hepatitis B
Naar Samenvatting ›- Bespreek de besmettelijkheid van bloed en lichaamsvloeistoffen bij hepatitis B en hoe overdracht naar anderen te vermijden.
- Ontraad onbeschermde seksuele contacten en motiveer de patiënt om met zijn contacten te bespreken dat deze zich laten vaccineren (zie NHG Standaard Het soa-consult).
Personen uit de directe omgeving van een patiënt met hepatitis B
Naar Samenvatting ›- Nodig eventueel de partner uit op het spreekuur.
- Geef adviezen om contact met het bloed van de patiënt te voorkomen en onbeschermde seksuele contacten te vermijden.
- Adviseer vaccinatie aan partners en zo nodig gezinsleden van patiënten met hepatitis B (zie Richtlijnen ter preventie van virushepatitis).
Thuisarts
Naar Samenvatting ›Verwijs naar de informatie over leverontsteking op thuisarts.nl, die is gebaseerd op deze NHG-Standaard.
Controles
Naar Samenvatting ›Acute hepatitis B
Naar Samenvatting ›- Spreek contact af naar behoefte.
- Bepaal na 6 maanden opnieuw het HBsAg en eventueel aanvullend onderzoek conform tabel 4 (zie eventueel stroomschema 1 in de bijlage). Bespreek met de patiënt de optie om al eerder door te verwijzen naar een hepatitisbehandelcentrum of mdl-arts indien regionaal afgesproken.
Consultatie en verwijzing
Naar Samenvatting ›Acute hepatitis B
Naar Samenvatting ›Verwijs een ernstig zieke patiënt met acute hepatitis B naar een hepatitisbehandelcentrum of mdl-arts indien regionaal afgesproken.
Chronische hepatitis B
Naar Samenvatting ›- Verwijs alle patiënten met chronische hepatitis B naar een hepatitisbehandelcentrum.
- Verwijs ook patiënten met in het verleden vastgesteld chronische (meestal ‘inactieve’) hepatitis B naar een hepatitisbehandelcentrum.
- Voor deze groep patiënten zijn waarschijnlijk nieuwe diagnostische of therapeutische middelen beschikbaar.
- Bij bekende chronische hepatitis B is nieuw laboratoriumonderzoek in de eerste lijn niet nodig.
- De huisarts kan zelf invullen hoe hij dit beleid vormgeeft (bijvoorbeeld afhankelijk van de praktijkpopulatie), mogelijkheden zijn aankaarten bij spreekuurbezoekers of opsporing via een uitdraai van het HIS.
- Verwijs ook patiënten met in het verleden vastgesteld chronische (meestal ‘inactieve’) hepatitis B naar een hepatitisbehandelcentrum.
- Leg uit waarom verwijzing en controles bij patiënten met chronische hepatitis B noodzakelijk zijn (voorkomen van cirrose en HCC). De hepatitisbehandelaar stelt vast of er een behandelindicatie bestaat en of er een indicatie bestaat voor HCC-screening.
- Vermeld de episode in een verwijsbrief aan zorgverleners voor wie deze informatie relevant is. Dit is van belang vanwege het risico op (re)activatie bij sterke immuunsuppressieve behandelingen (zie Etiologie en pathofysiologie hepatitis B).
De hepatitisbehandelaar bepaalt met behulp van aanvullend laboratoriumonderzoek (onder andere bloedbeeld, levertesten/enzymen, albumine, INR, HBsAg, anti-HB-core, HBeAg, anti-HBe en HBV-DNA), een echo abdomen en een fibroscan of er een indicatie voor behandeling bestaat. Ook wordt bepaald of er een indicatie bestaat voor HCC-screening (halfjaarlijkse echografie van de lever).
Het Richtsnoer HBV geeft aan dat HCC-screening is geïndiceerd bij:
- Alle patiënten met chronische hepatitis B en cirrose
- De volgende groepen patiënten met chronische hepatitis B zonder cirrose:
- Oost-Aziatische mannen > 40 jaar
- Oost-Aziatische vrouwen > 50 jaar
- patiënten afkomstig uit Sub-Saharaans Afrika > 20 jaar
- patiënten met een positieve familieanamnese voor HCC
De werkgroep heeft dit verwijsbeleid opgesteld omdat de behandeling op het gebied van virushepatitis de laatste jaren snel verandert, het vaststellen van het juiste follow-upbeleid complex en tijdsintensief is en huisartsen momenteel de fibroscan niet kunnen aanvragen. De werkgroep heeft zich gebaseerd op het Richtsnoer HBV. De aanbevelingen in het Richtsnoer HBV zijn primair gebaseerd op de aanbevelingen van de European Association for the Study of the Liver (EASL), zoals weergegeven in de EASL-richtlijn Clinical practice guidelines on the management of hepatitis B virus infection, gepubliceerd in 2017 [EASL 2017], zie verder de Totstandkoming Richtsnoer HBV.
Zwangeren met hepatitis B
Naar Samenvatting ›- Verwijs zwangeren met een chronische hepatitis B naar een hepatitisbehandelcentrum. De behandeling van deze patiënten is erop gericht om het risico op overdracht van moeder op kind te verminderen.
- Als bij het bloedonderzoek in het eerste trimester, uitgevoerd door de verloskundig zorgverlener, hepatitis B wordt aangetoond, draagt de verloskundig zorgverlener zorg voor het vervolgbeleid (zie Prenatale Screening Infectieziekten en Erytrocytenimmunisatie (PSIE).
- Zie voor het beleid ter preventie van overdracht van moeder naar kind bij de bevalling de Richtlijnen ter preventie van virushepatitis.
Functioneel genezen hepatitis B
- Als de patiënt cirrose heeft, vinden de benodigde controles plaats bij de specialist. Er zijn geen specifieke controles nodig bij de huisarts.
- Let op het risico op reactivatie bij sterke immuunsuppressieve behandelingen in de toekomst. Vermeld de episode in een verwijsbrief aan zorgverleners voor wie deze informatie relevant is.
- Zie Etiologie en pathofysiologie hepatitis B.
Bij zwangeren met chronische hepatitis B kan behandeling met een virusremmer het risico op transmissie van het virus en falen van vaccinatie bij de pasgeborene verminderen. Het hepatitisbehandelcentrum bepaalt de indicatie voor behandeling. Dit is van belang omdat de bescherming van de pasgeborene door passieve immunisatie in combinatie met vaccinatie niet 100% is . De voordelen van deze behandeling moeten worden afgewogen tegen de risico’s ervan. Behandeling vindt in dat geval plaats vanaf week 32 tot aan de bevalling. Voor de uniformiteit en de implementatie van de standaard heeft de werkgroep ervoor gekozen om de verwijscriteria voor zowel zwangere als niet-zwangere patiënten met chronische hepatitis B gelijk te houden.
Terugverwijzing naar de huisarts
Naar Samenvatting ›- De meeste patiënten met chronische hepatitis B worden gecontroleerd bij de hepatitisbehandelaar.
- Na onderlinge afstemming tussen de hepatitisbehandelaar en de huisarts, kan de huisarts optioneel bij individuele patiënten de controles overnemen. De overname vindt plaats in samenspraak met de patiënt, huisarts en hepatitisbehandelaar.
- In de ontslagbrief van de hepatitisbehandelaar is duidelijk vermeld welke controles nodig zijn en wanneer consultatie van of verwijzing naar de hepatitisbehandelaar noodzakelijk is.
Controles bij patiënten die, na afstemming tussen de patiënt, huisarts en hepatitisbehandelaar, zijn terugverwezen naar de huisarts, bestaan over het algemeen uit:
- 1-2 x per jaar bepaling van de ALAT
- 1-2 x per jaar bepaling van het HBV-DNA
- 1 x per 3 jaar bepaling van het HBsAg
Dit gaat bijvoorbeeld om patiënten zonder relevante comorbiditeit, bij wie geen indicatie voor HCC-screening bestaat. De ontslagbrief van de hepatitisbehandelaar vermeldt de specifieke controles bij de individuele patiënt.
Consultatie (bijvoorbeeld via teleconsultatie) of verwijzing naar de hepatitisbehandelaar is over het algemeen nodig bij:
- ALAT > 1,5 x de normaalwaarde
- HBV-DNA ≥ 2000 IU/mL
Als het HBsAg positief blijft en er geen reden is voor consultatie of verwijzing gaan de controles over het algemeen (levenslang) door. Bij een negatieve HBsAg is er sprake van een functioneel genezen hepatitis B.
Aangifteplicht en bronopsporing
Naar Samenvatting ›- Acute hepatitis A, B en C, en chronische hepatitis B en C zijn meldingsplichtig. Dit houdt in dat de huisarts of het laboratorium na het stellen van de diagnose de ziekte binnen 1 werkdag moet melden aan de GGD. Zie voor de specifieke meldingscriteria per infectieziekte de LCI-richtlijnen.
- De GGD is verantwoordelijk voor de bron- en contactopsporing, de voorlichting aan de patiënt over besmettelijkheid en (waar mogelijk) de bescherming van de contacten.
- Voor hepatitis A geldt dat het contactonderzoek zich voornamelijk richt op personen die van dezelfde toiletvoorziening gebruikmaken als de patiënt. Contacten van een patiënt met hepatitis A die hiervoor in aanmerking komen, worden zo nodig gevaccineerd of passief geïmmuniseerd. Hierover vindt afstemming plaats tussen de GGD en de huisarts.
- Bij acute hepatitis B wordt bronopsporing uitgevoerd (zie ook NHG Standaard Het soa-consult). Contacten van een patiënt met acute of chronische hepatitis B die hiervoor in aanmerking komen, worden zo nodig gescreend en/of gevaccineerd. De huisarts en de GGD maken afspraken wie de uitvoering doet.
- Brononderzoek bij acute hepatitis C is vooral van belang om eventuele iatrogene verspreiding van hepatitis C (transfusie, transplantatie, procedurefouten) te achterhalen om deze in de toekomst te kunnen voorkomen (zie Besmetting en incubatietijd). Bij hepatitis C is contactonderzoek meestal niet nodig, behalve bij MSM die de besmetting via seksueel contact hebben opgelopen of bij familieleden met een bijzondere indicatie zoals vermeld in de LCI-richtlijn.
De arts die bij iemand een acute virushepatitis vaststelt, of een chronische hepatitis B of C, is wettelijk verplicht dit binnen één werkdag aan de GGD te melden (zie www.wetten.overheid.nl, geraadpleegd december 2014). De arts doet dit ook wanneer hij gegronde reden heeft te vermoeden dat iemand een virushepatitis heeft en de betreffende persoon weigert het onderzoek te ondergaan dat nodig is ter vaststelling van die ziekte.
Na de melding bepaalt de GGD of er maatregelen nodig zijn. Aanwijzingen voor contactonderzoek staan beschreven in de protocollen van de LCI.
Hepatitis C
Naar Samenvatting ›Voorlichting en advies
Naar Samenvatting ›Patiënten met hepatitis C
Naar Samenvatting ›Geef ter voorkoming van besmetting van anderen, naast de algemene adviezen, de volgende specifieke adviezen:
- Ontraad bij chronische hepatitis C alcoholgebruik ten zeerste vanwege de kans op blijvende levercelschade.
- Bespreek de besmettelijkheid van bloed bij hepatitis C en hoe overdracht naar anderen te vermijden is. Het risico op overdracht van hepatitis C bij seksueel contact is klein, behalve bij (met hiv geïnfecteerde) MSM die seksuele risicocontacten hebben waarbij verwonding optreedt (zie Besmetting en incubatietijd).
Tozun et al. concludeerden dat matig alcoholgebruik tijdens de herstelfase van een acute hepatitis geen effect had op het beloop. Patiënten met een chronische hepatitis-C-infectie dienen echter het advies te krijgen hun alcoholconsumptie te staken of maximaal te beperken teneinde progressie van de ziekte zo veel mogelijk tegen te gaan. In een aantal onderzoeken is aangetoond dat het nuttigen van alcohol bij een persisterende hepatitis-C-infectie het beloop of ontstaan van cirrose aanzienlijk versnelt.
Personen uit de directe omgeving van een patiënt met hepatitis C
Naar Samenvatting ›Geef adviezen gericht op het voorkomen van contact met bloed van de patiënt (zie Algemene voorlichting virushepatitis).
Consultatie en verwijzing
Naar Samenvatting ›- Verwijs alle patiënten met acute en chronische hepatitis C naar een hepatitisbehandelcentrum, ook als in het verleden de behandeling niet succesvol was (zie Behandeling hepatitis C). Bij een besmetting < 3 maanden geleden kan een spontane genezing worden afgewacht, omdat eventuele behandeling van acute hepatitis C pas na 3 maanden wordt ingezet.
- Overleg tijdens de behandeling over elke wijziging of start van medicijnen met de behandelend specialist. De hepatitis-C-medicijnen zijn namelijk zeer interactiegevoelig.
Hepatitis E
Naar Samenvatting ›Voorlichting en advies
Naar Samenvatting ›- Bij hepatitis E is het beloop vrijwel altijd gunstig.
- Adviezen ter voorkoming van besmetting van anderen zijn niet nodig.
Controles
Naar Samenvatting ›Controle van de leverfuncties is niet nodig omdat dit geen consequenties heeft voor het beleid.
Levercelschade door geneesmiddelen
Naar Samenvatting ›- Het beleid bij hepatotoxiciteit wordt bepaald door de mate van ALAT-stijging, de indicatie voor het geneesmiddel en de beschikbaarheid van alternatieven.
- Het is veilig om een geneesmiddel door te gebruiken tot arbitrair een stijging van het ALAT tot 1,5 maal de normaalwaarde. Bij hogere ALAT-waarden is staken van het gebruik van het desbetreffende geneesmiddel doorgaans afdoende om herstel van de lever te bewerkstelligen.
- Soms is staken niet (direct) mogelijk, omdat er een dwingende behandelnoodzaak is en een alternatief ontbreekt, bijvoorbeeld bij anti-epileptica. Maak in dat geval met de oorspronkelijk voorschrijver van het verdachte geneesmiddel een afweging tussen de voor- en nadelen van de behandeling.
Voorlichting en advies
Naar Samenvatting ›- Leg uit dat het geneesmiddel (mogelijk) schade aan de lever geeft, wat kan resulteren in fibrose en cirrose van de lever. De schade verdwijnt doorgaans na staken van het geneesmiddel.
- Bespreek met de patiënt de voor- en nadelen van stoppen, vervangen of continueren van het geneesmiddel.
Medicamenteuze behandeling
Naar Samenvatting ›- Beoordeel de indicatie, de noodzaak om het geneesmiddel te continueren en de beschikbaarheid van alternatieven.
- Staak het geneesmiddel tenzij er een dringende behandelindicatie bestaat en er geen alternatieven voorhanden zijn.
- Overleg bij twijfel met de (behandelend) voorschrijver en verwijs zo nodig.
Controles
Naar Samenvatting ›- Bepaal het ALAT 1 maand na staken van het geneesmiddel.
- Indien het ALAT is gedaald tot 1,5 maal de normaalwaarde kan bij een adequate indicatie gestart worden met een geneesmiddel met een ander metabolisme, eventueel in overleg met de apotheker en/of de behandelend specialist.
- Controleer het ALAT driemaal. Indien het ALAT lager blijft dan 1,5 maal de normaalwaarde is verdere controle niet nodig. Indien het ALAT stijgt, beoordeel dan opnieuw de indicatie en de beschikbaarheid van alternatieven (zie Medicamenteuze behandeling levercelschade door geneesmiddelen).
- Controleer het ALAT elke 3 maanden bij doorzetten medicijngebruik. Als het ALAT lager blijft dan 1,5 maal de normaalwaarde, controleer dan voortaan elk half jaar. Staak bij gelijk blijven van het ALAT na ca. 3 jaar de controles. Een waarde van grofweg 1,5 maal de normaalwaarde is acceptabel.
Consultatie en verwijzing
Naar Samenvatting ›- Overleg met of verwijs naar de behandelend specialist of een mdl-arts of internist met specifiek aandacht voor leveraandoeningen:
- bij een ALAT ≥ 10 maal de normaalwaarde: direct
- bij twijfel over voortzetten medicatie of voor het instellen op een ander geneesmiddel
- bij een persisterende verhoging van het ALAT (≥ 1,5 maal boven de normaalwaarde) ondanks staken van het hepatotoxisch geneesmiddel en indien een andere verklaring niet waarschijnlijk lijkt
Levercelschade door alcohol
Naar Samenvatting ›Voorlichting en advies
Naar Samenvatting ›Leg patiënten met levercelschade door alcohol uit dat door alcoholgebruik te stoppen de leverfunctie vaak zal herstellen.
Niet-medicamenteuze behandeling
Naar Samenvatting ›Stimuleer de patiënt te stoppen met alcoholgebruik en vervolg na een maand, en vervolgens 3-maandelijks, het ALAT totdat dit gedaald is tot < 1,5 maal de normaalwaarde. Ga bij een persisterend verhoogd ALAT (1,5-10 maal de referentiewaarde) nogmaals na of de patiënt het alcoholgebruik heeft gestaakt. Is dit het geval, overweeg dan of een andere oorzaak waarschijnlijk is (zie stroomschema 3 in de bijlage). Zie voor de behandeling van overmatig alcoholgebruik NHG-Standaard Problematisch alcoholgebruik.
Niet-alcoholische vetlever
Naar Samenvatting ›Voorlichting en advies
Naar Samenvatting ›Leg patiënten met NAFLD uit dat er een verhoogde vetopslag bestaat in de lever, wat op termijn de functie van de lever negatief kan beïnvloeden. Daarnaast is er een verhoogd risico op hart- en vaatziekten (circa tweemaal verhoogd) en sterfte (circa 1,5 maal) (zie Etiologie en pathofysiologie: Niet-alcoholische vetlever). Het doel van de behandeling is het voorkomen van cirrose en fibrose. Zie voor het verminderen van het risico op hart- en vaatziekten NHG-Standaard Cardiovasculair risicomanagement (CVRM).
Niet-medicamenteuze behandeling
Naar Samenvatting ›- Bespreek met obese patiënten de optie om 5-10% af te vallen. Afvallen is mogelijk effectief ter vermindering van de vetstapeling in de lever; het is in elk geval effectief ter vermindering van het risico op hart- en vaatziekten en diabetes. Zie voor het beleid bij afvallen NHG-Standaard Obesitas.
- Stimuleer de patiënt om voldoende te bewegen (zie Praktijkhandleiding Leefstijl).
Er is onvoldoende evidence om richtlijnen te formuleren over het beleid bij NAFLD. Mogelijk is ≥ 10% afvallen effectief ter vermindering van de vetstapeling in de lever. Bij obese patiënten is afvallen in elk geval wenselijk om het risico op comorbiditeit (DM type 2, hart- en vaatziekten) te verminderen. Omdat ≥ 10% afvallen voor de meeste obese patiënten niet realistisch is, kiest de werkgroep ervoor om in lijn met de NHG-Standaard Obesitas bij patiënten met obesitas en NAFLD te streven naar 5 tot 10% gewichtsverlies.
Aanbeveling
De huisarts adviseert patiënten met obesitas én NAFLD om 5 tot 10% af te vallen.
Achtergrond
We verrichtten een search met de volgende vraag: ‘Welke behandelingen zijn effectief in het verminderen van steatose bij NAFLD?’. Hierbij werd één richtlijn gevonden van The American Association for the study of liver diseases. Er werden geen andere systematische reviews gevonden. De auteurs van de richtlijn voerden een systematische review uit van de beschikbare onderzoeken gevonden in Medline (search tot juni 2011). Voor het opstellen van de conclusies en aanbevelingen maakten de auteurs gebruik gemaakt van de voorschriften van The American college of Physicians. De richtlijn bespreekt de effectiviteit van een aantal behandelingen zonder de effectgrootte, het aantal onderzoeken en het aantal patiënten te vermelden. De reden hiervoor werd niet vermeld. Hiermee is de bewijskracht van de richtlijn laag. Omdat er geen andere systematische reviews zijn gevonden, is er toch voor gekozen om deze richtlijn te gebruiken.
Resultaten
Leefstijladvies
Afvallen door een lagere calorische intake of in combinatie met meer bewegen geeft vermindering van de steatose. Een gewichtsverlies van 10% of meer zorgt voor vermindering van de steatosis.
Metformine
Metformine heeft geen effect op de leverhistologie bij NAFLD.
Vitamine E
Bij patiënten met NAFLD lijkt inname van vitamine E geassocieerd met verlaging van de aminotransferases en verbetering van de steasosis. Het effect is onduidelijk doordat de uitkomsten van de gevonden onderzoeken verschillen. Eindpunten zoals mortaliteit en morbiditeit worden niet vermeld. Een hoge dosis vitamine E (800 IU/ml) is geassocieerd met een verhoogde mortaliteit en een verhoogd risico op prostaatkanker.
Bariatrische chirurgie
Bariatrische chirurgie is geassocieerd met afname van de steatose, NASH en fibrose. De onduidelijkheid over het effect komt door een gebrek aan goed opgezette onderzoeken.
Statines
Er zijn geen goed opgezette RCT’s uitgevoerd.
Ursodeoxycholzuur en omega-3-vetzuren
Er zijn geen goed opgezette RCT’s uitgevoerd.
Conclusie
Er is weinig evidence over de effectiviteit van interventies bij NAFLD. Mogelijk is ≥ 10% afvallen effectief in het verminderen van NAFLD.
Controles
Naar Samenvatting ›- Stel een cardiovasculair risicoprofiel op volgens NHG-Standaard Cardiovasculair risicomanagement (CVRM).
- Bepaal bij de jaarlijkse controle ook het ALAT voor evaluatie van het effect van de behandeling.
Consultatie en verwijzing
Naar Samenvatting ›Overweeg verwijzing naar een mdl-arts bij een persisterend verhoogd ALAT 1,5-10 maal boven de normaalwaarde ondanks behandeling, bij onzekerheid over de diagnose of voor nadere diagnostiek naar de aanwezigheid van cirrose of zeldzame oorzaken.
Overige leveraandoeningen
Naar Samenvatting ›Consultatie en verwijzing
Naar Samenvatting ›Overleg met of verwijs naar een mdl-arts of internist met specifieke aandacht voor leveraandoeningen bij een patiënt:
- met een ALAT > 10 maal de normaalwaarde: direct, tenzij er een duidelijke verklaring is en spontaan herstel is te verwachten
- met een ALAT die bij herhaling 1,5-10 maal boven de normaalwaarde ligt en bij wie meer duidelijkheid is gewenst of vanwege de mogelijkheid van zeldzame aandoeningen zoals auto-immuunhepatitis of hemochromatose
- met cirrose, voor aanvullende diagnostiek en eventuele behandeling
De werkgroep heeft ervoor gekozen om bij een ALAT hoger dan tien keer de normaalwaarde direct te verwijzen naar de mdl-arts of internist. Deze arbitraire waarde is gekozen op basis van consensus en ervaring. Het is aannemelijk dat bij een ALAT hoger dan tienmaal de normaalwaarde het risico op een ernstige en levensbedreigende aandoening toeneemt, tenzij de verhoging is toe te schrijven aan een infectieuze hepatitis en spontaan herstel te verwachten valt.
Richtlijnen ter preventie van virushepatitis
Naar Samenvatting ›Algemeen
Naar Samenvatting ›- Het preventieve beleid bij virushepatitis wordt uitgevoerd in overleg met de GGD. Dit bestaat op indicatie uit passieve immunisatie, door middel van toediening van immunoglobuline, en vaccinatie.
- Passieve immunisatie of vaccinatie ter preventie van hepatitis C is niet mogelijk.
- Zie voor preventie van en beleid na contact met (mogelijk besmet) bloed de Richtlijn Infectiepreventie in de huisartsen- en verloskundigenpraktijk.
De werkgroep volgt in deze standaard de vaccinatieadviezen van RIVM en GGD. Zowel voor hepatitis A als voor hepatitis B zijn effectieve vaccins beschikbaar met hooguit lichte bijwerkingen.
Preventie hepatitis A
Naar Samenvatting ›- Adviseer personen uit risicogroepen (zie tabel 2) vaccinatie als risicocontacten (blijven) plaatsvinden.
- Andere indicaties voor vaccinatie zijn:
- pre-expositieprofylaxe (bijvoorbeeld reizigers naar risicogebieden, beroepsblootstelling)
- chronische hepatitis B of C
- een niet-virale chronische leverziekte en post-expositieprofylaxe
- Vaccinatie met hepatitis-A-vaccin als post-expositieprofylaxe is effectief indien het wordt gegeven aan patiënten < 40 jaar binnen 14 dagen na de eerste ziektedag van de indexpatiënt. Patiënten > 40 jaar worden passief geïmmuniseerd.
- Passieve immunisatie als post-expositieprofylaxe is zinvol bij contacten van patiënten met hepatitis A tot 28 dagen na de eerste ziektedag van de indexpatiënt.
De keuze voor actieve of passieve bescherming is onder meer afhankelijk van de leeftijd. Zie voor uitgebreide informatie het protocol van de LCI. Bij vaccinatie tegen hepatitis A heeft 2 weken, 4 weken en 12 maanden na de eerste dosis respectievelijk 75 tot 100%, 94 tot 100% en 94 tot 100% van de gevaccineerden beschermende antistofgehalten.
Vaccinatie tegen hepatitis A wordt aanbevolen bij chronische hepatitis B en C en bij personen met een niet-virale chronische leverziekte met een verhoogd risico op een hepatitis-A-infectie. De verhoogde besmettingskans is een gevolg van reizen, beroepsuitoefening of een epidemie. Deze patiënten hebben een verhoogd risico op een fulminante hepatitis door het HAV.
Mocht tot vaccinatie worden overgegaan, dan dient voorafgaand aan de vaccinatie diagnostiek plaats te vinden om vast te stellen of er niet reeds hepatitis-A-antistoffen aanwezig zijn.
Preventie hepatitis B
Naar Samenvatting ›Rijksvaccinatieprogramma
Naar Samenvatting ›Kinderen geboren vanaf 2003 met een verhoogd risico op hepatitis B zijn via het rijksvaccinatieprogramma gevaccineerd tegen hepatitis B. Sinds 1 augustus 2011 worden alle nieuwgeboren kinderen gevaccineerd tegen hepatitis B.
Gezondheidszorgmedewerkers
Naar Samenvatting ›Gezondheidszorgmedewerkers, zoals huisartsen en doktersassistenten, die geregeld met bloed in aanraking komen, wordt hepatitis B-vaccinatie aangeboden, omdat zij tot een risicogroep behoren. Binnen de groep gezondheidszorgmedewerkers wordt onderscheid gemaakt tussen risicovormers en risicolopers. Dit heeft namelijk gevolgen voor de benodigde postvaccinatietiter. Zie voor de uitvoering en interpretatie hiervan de Richtlijn hepatitis B van het Landelijk Centrum voor Infectieziekten (LCI).
Specifieke groepen en situaties
Naar Samenvatting ›- MSM en sekswerkers zijn voor kosteloze hepatitis-B-vaccinatie te verwijzen naar de GGD.
- Ook bij patiënten met een chronische leveraandoening wordt de vaccinatie vergoed.
- Vaccinatie en soms ook passieve immunisatie tegen hepatitis B is verder geïndiceerd na een prikaccident (zie Landelijke richtlijn prikaccidenten voor de indicaties en termijn van toediening) en na een incidenteel onveilig seksueel contact met een patiënt die bekend is met hepatitis B.
- Na vaccinatie dient de anti-HBs-titer alleen te worden bepaald bij risicofactoren voor non-respons (mannen > 40 jaar, BMI > 30 en zware rokers). Zie voor de uitvoering en interpretatie hiervan de Richtlijn hepatitis B van het Landelijk Centrum voor Infectieziekten (LCI).
In de Landelijke richtlijn Preventie transmissie van hepatitis B van medisch personeel naar patiënten staat onder meer het volgende:
- Risicohandelingen zijn die handelingen waarbij de kans op bloed-bloedcontact tussen gezondheidszorgwerker en patiënt groot is. Het betreft vooral handelingen waarbij de (gehandschoende) handen binnen lichaamsholten of wonden in contact kunnen komen met scherpe instrumenten, naalden of scherpe weefseldelen (bijvoorbeeld botpunten of gebitselementen), terwijl de handen of vingertoppen soms niet zichtbaar zijn.
- Risicovormers zijn onder andere: tandartsen, mondhygiënisten, orthodontisten, orthodontie-assistenten, en sommige tandartsassistenten; verloskundigen; bepaalde medische specialisten, bepaalde verpleegkundigen, bepaalde paramedische medewerkers.
- Elke risicovormer moet gevaccineerd zijn tegen hepatitis B, met controle van de respons (titer) 4-8 weken na de laatste vaccinatie, die >100 IE/L moet zijn.
Informatie over gezondheidszorgmedewerkers die geen risicovormer zijn, is onder meer te vinden in de LCI-richtlijn hepatitis B, paragraaf Interpretatie van de anti-HBs-titer na vaccinatie, met uitzondering van risicovormers in de gezondheidszorg. Voor risicolopend personeel wordt een titer van >10 UI/L aangehouden als bescherming, het volgende draaiboek is daarop van toepassing:
Praktijkrichtlijn voor bedrijfsartsen: hepatitis B-vaccinatie van risicolopend personeel dat geen risicovormer is.
De meest huisartsen en praktijkmedewerkers zijn geen risicovormers, maar risicolopers.
De werkgever is verantwoordelijk voor de bescherming tegen arbeidsgerelateerde risico’s, inclusief vaccinaties (Arbobesluit 4.85). Mensen die werken in de zorg of op een andere manier risico lopen op contact met menselijk bloed of bloedproducten tijdens de beoefening van hun werk dienen door hun werkgever te worden gevaccineerd.
GGD-en en arbodiensten zijn gespecialiseerd in het vaccineren van medewerkers in de gezondheidszorg, met speciale aandacht voor de risicovormers.
Zie voor de volledige lijst het protocol van de LCI (LCI-richtlijn Hepatitis B op www.rivm.nl).
Meer informatie:
- Landelijke richtlijn preventie transmissie van hepatitis B van medisch personeel naar patiënten.
- Praktijkrichtlijn voor bedrijfsartsen: hepatitis B-vaccinatie van risicolopend personeel dat geen risicovormer is.
- LCI-richtlijn Hepatitis B
Bij bloed-bloedcontact, zoals een prikaccident, bestaat het risico op overdracht van HBV, HCV of hiv. Het risico hierop is bij een prikaccident grofweg 30% voor HBV, 3% voor HCV en 0,3% voor hiv. Voor een uitgebreid en actueel overzicht zie de Landelijke Richtlijn Prikaccidenten op www.rivm.nl.
Elke medewerker in een huisartsenpraktijk die risico loopt met humaan bloed in contact te komen dient gevaccineerd zijn tegen hepatitis B. Ook leerlingen en stagiairs dienen als werknemers te worden beschouwd.
Zie voor meer informatie het Draaiboek seksaccidenten van het RIVM op www.rivm.nl.
Voorkomen overdracht bij de bevalling
Naar Samenvatting ›Het beleid ter voorkoming van overdracht van het hepatitis-B-virus bij de bevalling is als volgt.
- De huisarts ontvangt bericht van de GGD als bij de screening van een zwangere een positieve HBsAg is gevonden. Zie voor het beleid tijdens de zwangerschap Richtlijnen beleid.
- Bij een zwangere HBsAg-positieve vrouw moet de pasgeborene direct na de partus passief geïmmuniseerd en gevaccineerd worden, door degene die de bevalling heeft geleid. De verdere vaccinatie wordt uitgevoerd op het consultatiebureau.
In het geval van een positieve uitslag van de HBsAg-screeningstest in de zwangerschap ontvangen de huisarts en het RIVM Regionale Coördinatie Programma (RCP) een kopie. Een pasgeborene met een HBsAg-positieve moeder ontvangt hepatitis-B-immunoglobuline (HBIg) en hepatitis B-vaccin. Deze kunnen tijdens hetzelfde contactmoment gegeven worden, de volgorde is niet van belang. Wel moeten de injecties in verschillende ledematen worden gegeven. Het HBIg moet in elk geval binnen 2 uur worden gegeven, terwijl de maximumtermijn voor het toedienen van het hepatitis B-vaccin ruimer is gesteld (binnen 48 uur). Zie het draaiboek Prenatale screening Infectieziekten en Erytrocytenimmunisatie van het RIVM op rivm.nl voor de details. Overigens biedt vaccinatie, zelfs in combinatie met immunoglobulines, onvoldoende bescherming aan pasgeborenen als de moeder een hepatitis B-infectie heeft met hoge virusreplicatie. Daarom wordt aangeraden om bij zwangeren met chronische hepatitis B nog tijdens de zwangerschap te overleggen met of te verwijzen naar een hepatitisbehandelcentrum met de vraag of zij in aanmerking komen om te starten met antivirale therapie.
Bijlage
Naar Samenvatting ›Referenties
- Termorshuizen F, Van de Laar MJW. De epidemiologie van hepatitis A in Nederland, 1957-1998. Ned Tijdschr Geneeskd 1998;142:2364-8.
- Suijkerbuijk AW, Lindeboom R, Van Steenbergen JE, Sonder GJ, Doorduyn Y. Effect of hepatitis A vaccination programs for migrant children on the incidence of hepatitis A in The Netherlands. Eur J Publ Health 2009;19:240-4.
- RIVM. State of the infectious diseases in the Netherlands, 2013 (2014). Ga naar bron: RIVM. State of the infectious diseases in the Netherlands, 2013 (2014).
- RIVM. Sexually transmitted infections, including HIV, in the Netherlands in 2014 (2015b). Ga naar bron: RIVM. Sexually transmitted infections, including HIV, in the Netherlands in 2014 (2015b).
- LCI. Richtlijn Hepatitis A (2003). De Bilt: RIVM.
- LCI. Richtlijn Hepatitis A (2014). De Bilt: RIVM. Ga naar bron: LCI. Richtlijn Hepatitis A (2014). De Bilt: RIVM.
- Koedijk FDH, Op de Coul ELM, Van de Laar MJW. Chronische hepatitis B infecties in Nederland. Een overzicht van 2001-2003. Infectieziektenbulletin 2005;16:18-22. Ga naar bron: Koedijk FDH, Op de Coul ELM, Van de Laar MJW. Chronische hepatitis B infecties in Nederland. Een overzicht van 2001-2003. Infectieziektenbulletin 2005;16:18-22.
- LCI. Richtlijn Hepatitis B (2013). De Bilt: RIVM. Ga naar bron: LCI. Richtlijn Hepatitis B (2013). De Bilt: RIVM.
- Hahne SJ, De Melker HE, Kretzschmar M, Mollema L, Van Der Klis FR, Van Der Sande MA, et al. Prevalence of hepatitis B virus infection in the Netherlands in 1996 and 2007. Epidemiol Infect 2012;140:1469-80.
- Mostert MC, Richardus JH, De Man RA. Referral of chronic hepatitis B patients from primary to specialist care: making a simple guideline work. J Hepatol 2004;41:1026-30.
- Van Oeffelen AAM, van Aar F, van den Broek IVF et al. Sexually transmitted infections, including HIV, in the Netherlands in 2014. Bilthoven: RIVM-rapport nummer 2015-0041. 2015. Ga naar bron: Van Oeffelen AAM, van Aar F, van den Broek IVF et al. Sexually transmitted infections, including HIV, in the Netherlands in 2014. Bilthoven: RIVM-rapport nummer 2015-0041. 2015.
- Gezondheidsraad. Algemene vaccinatie tegen hepatitis B. Den Haag: Gezondheidsraad, 2001. Ga naar bron: Gezondheidsraad. Algemene vaccinatie tegen hepatitis B. Den Haag: Gezondheidsraad, 2001.
- Gezondheidsraad. Bescherming tegen Hepatitis B. Rijswijk: Gezondheidsraad, 1996; publicatie nr. 1996/15.
- RIVM. Staat van Infectieziekten in Nederland 2009 (2010). Ga naar bron: RIVM. Staat van Infectieziekten in Nederland 2009 (2010).
- Vriend HJ, Van Veen MG, Prins M, Urbanus AT, Boot HJ, Op De Coul EL. Hepatitis C virus prevalence in The Netherlands: migrants account for most infections. Epidemiol Infect 2013;141:1310-7.
- Vriend HJ, Op de Coul EL, Van de Laar TJ, Urbanus AT, Van der Klis FR, Boot HJ. Hepatitis c virus seroprevalence in The Netherlands. Eur J Public Health 2012;22:819-21.
- Van den Berg CH, Smit C, Bakker M, Geskus RB, Berkhout B, Jurriaans S, et al. Major decline of hepatitis C virus incidence rate over two decades in a cohort of drug users. Eur J Epidemiol 2007;22:183-93.
- Ruys TA, Reesink HW, Lange JM. Coinfectie met hepatitis-C-virus en HIV. Ned Tijdschr Geneeskd 2003;147:2056-60.
- Lott JA, Nolte FS, Gretch DR, Koff RS, Seeff LB. Laboratory guidelines for screening, diagnosis and monitoring of hepatic injury. Washington: The National Academy of Clinical Biochemistry; 2000.
- Lok ASF, McMahon BJ. Corrections to AASLD Guidelines on chronic hepatitis B. Hepatology 2007;45:1347.
- The EASL Jury. EASL International Consensus Conference on Hepatitis B. 13-14 September, 2002: Geneva, Switzerland. Consensus statement (short version). J Hepatol 2003;38:533-40.
- WHO. Fact sheet Hepatitis B (2015). Ga naar bron: WHO. Fact sheet Hepatitis B (2015).
- Averhoff FM, Glass N, Holtzman D. Global burden of hepatitis C: considerations for healthcare providers in the United States. Clin Infect Dis 2012;55 Suppl 1:S10-5.
- Mohd Hanafiah K, Groeger J, Flaxman AD, Wiersma ST. Global epidemiology of hepatitis c virus infection: New estimates of age-specific antibody to hcv seroprevalence. Hepatology 2013;57:1333-42.
- RIVM. Infectieziekten Bulletin. 2015;26. (2015a) Ga naar bron: RIVM. Infectieziekten Bulletin. 2015;26. (2015a)
- LCI. Richtlijn Hepatitis E (2011b). De Bilt: RIVM. Ga naar bron: LCI. Richtlijn Hepatitis E (2011b). De Bilt: RIVM.
- Andriesse GI, Donmez M, Vissers J, Van Wijngaarden P. Acute hepatitis, maar niet A, B of C: overweeg E. Ned Tijdschr Geneeskd 2010;154:A1865.
- American Gastroenterological Association. Medical position statement: evaluation of liver chemistry tests. Gastroenterology 2002;123:1364-6.
- Mathiesen UL, Franzen LE, Fryden A, Foberg U, Bodemar G. The clinical significance of slightly to moderately increased liver transaminase values in asymptomatic patients. Scand J Gastroenterol 1999;34:85-91.
- Daniel S, Ben-Menachem T, Vasudevan G, Ma CK, Blumenkehl M. Prospective evaluation of unexplained chronic liver transaminase abnormalities in asymptomatic and symptomatic patients. Am J Gastroenterol 1999;94:3010-4.
- Pendino GM, Mariano A, Surace P, Caserta CA, Fiorillo MT, Amante A, et al. Prevalence and etiology of altered liver tests: a population-based survey in a Mediterranean town. Hepatology 2005;41:1151-9.
- Ekstedt M, Franzen LE, Mathiesen UL, Thorelius L, Holmqvist M, Bodemar G, et al. Long-term follow-up of patients with NAFLD and elevated liver enzymes. Hepatology 2006;44:865-73.
- Soderberg C, Stal P, Askling J, Glaumann H, Lindberg G, Marmur J, et al. Decreased survival of subjects with elevated liver function tests during a 28-year follow-up. Hepatology 2010;51:595-602.
- Stepanova M, Rafiq N, Younossi ZM. Components of metabolic syndrome are independent predictors of mortality in patients with chronic liver disease: a population-based study. Gut 2010;59:1410-5.
- Nielen MMJ, Spronk I, Davids R, Zwaanswijk M, Verheij RA, Korevaar JC. Verantwoording incidentie en prevalentie cijfers van gezondheidsproblemen in de Nederlandse huisartsenpraktijk in 2012 (2013). Ga naar bron: Nielen MMJ, Spronk I, Davids R, Zwaanswijk M, Verheij RA, Korevaar JC. Verantwoording incidentie en prevalentie cijfers van gezondheidsproblemen in de Nederlandse huisartsenpraktijk in 2012 (2013).
- Bedogni G, Miglioli L, Masutti F, Tiribelli C, Marchesini G, Bellentani S. Prevalence of and risk factors for nonalcoholic fatty liver disease: The dionysos nutrition and liver study. Hepatology 2005;42:44-52.
- Browning JD, Szczepaniak LS, Dobbins R, Nuremberg P, Horton JD, Cohen JC, et al. Prevalence of hepatic steatosis in an urban population in the united states: Impact of ethnicity. Hepatology 2004;40:1387-95.
- Speliotes EK, Massaro JM, Hoffmann U, Vasan RS, Meigs JB, Sahani DV, et al. Fatty liver is associated with dyslipidemia and dysglycemia independent of visceral fat: The Framingham Heart Study. Hepatology 2010;51:1979-87.
- Li H, Wang YJ, Tan K, Zeng L, Liu L, Liu FJ, et al. Prevalence and risk factors of fatty liver disease in Chengdu, Southwest China. Hepatobiliary Pancreat Dis Int 2009;8:377-82.
- Fan JG, Farrell GC. Epidemiology of non-alcoholic fatty liver disease in china. J Hepatol 2009;50:204-10.
- Koehler EM, Schouten JNL, Hansen BE, Van Rooij FJA, Hofman A, Stricker BH, et al. Prevalence and risk factors of non-alcoholic fatty liver disease in the elderly: results from the Rotterdam study. J Hepatol 2012;57:1305-11.
- Hadler SC, McFarland L. Hepatitis in day care centers: epidemiology and prevention. Rev Infect Dis 1986;8:548-57.
- Hadler SC, Webster HM, Erben JJ, Swanson JE, Maynard JE. Hepatitis A in day-care centers. A community-wide assessment. N Engl J Med 1980;302:1222-7.
- Noskin GA. Prevention, diagnosis, and management of viral hepatitis. A guide for primary care physicians. Arch Fam Med 1995;4:923-34.
- Shapiro CN. Transmission of hepatitis viruses. Ann Intern Med 1994;120:82-4.
- Koff RS. Hepatitis A. Lancet 1998;351:1643-9.
- Bower WA, Nainan OV, Han X, Margolis HS. Duration of viremia in hepatitis A virus infection. J Infect Dis 2000;182:12-7.
- Moyer LA, Mast EE. Hepatitis B: virology, epidemiology, disease, and prevention, and an overview of viral hepatitis. Am J Prev Med 1994;10 Suppl:45-55.
- Ganem D, Prince AM. Hepatitis B virus infection--natural history and clinical consequences. N Engl J Med 2004;350:1118-29.
- Lai CL, Ratziu V, Yuen MF, Poynard T. Viral hepatitis B. Lancet 2003;362:2089-94.
- Gerberding JL. Management of occupational exposures to blood-borne viruses. N Engl J Med 1995;332:444-51.
- Van Damme P, Cramm M, Van der Auwera JC, Vranckx R, Meheus A. Horizontal transmission of hepatitis B virus. Lancet 1995;345:27-9.
- Van der Eijk AA, Niesters HG, Hansen BE, Pas SD, Richardus JH, Mostert M, et al. Paired, quantitative measurements of hepatitis B virus DNA in saliva, urine and serum of chronic hepatitis B patients. Eur J Gastroenterol Hepatol 2005;17:1173-9.
- Versteegh FG, Wauters EA, Roord JJ. Hepatitis B-virus op school; een risico? Ned Tijdschr Geneeskd 1991;135:508-11.
- Fattovich G, Brollo L, Giustina G, Noventa F, Pontisso P, Alberti A, et al. Natural history and prognostic factors for chronic hepatitis type B. Gut 1991;32:294-8.
- Bruix J, Sherman M. AASLD practice guideline: management of hepatocellular carcinoma (2011). Ga naar bron: Bruix J, Sherman M. AASLD practice guideline: management of hepatocellular carcinoma (2011).
- Llovet JM, Burroughs A, Bruix J. Hepatocellular carcinoma. Lancet 2003;362:1907-17.
- Chayanupatkul M, Omino R, Mittal S, Kramer JR, Richardson P, Thrift AP, et al. Hepatocellular carcinoma in the absence of cirrhosis in patients with chronic hepatitis B virus infection. J Hepatol 2017;66:355-62.
- Dufour DR, Lott JA, Nolte FS, Gretch DR, Koff RS, Seeff LB. Diagnosis and monitoring of hepatic injury. I. Performance characteristics of laboratory tests. Clin Chem 2000;46:2027-49.
- Yeh ML, Huang CF, Hsieh MY, Huang JF, Dai CY, Yu ML, et al. Comparison of the abbott realtime hbv assay with the roche cobas ampliprep/cobas taqman hbv assay for hbv DNA detection and quantification. J Clin Virol 2014;60:206-14.
- Manesis EK, Papatheodoridis GV, Sevastianos V, Cholongitas E, Papaioannou C, Hadziyannis SJ. Significance of hepatitis b viremia levels determined by a quantitative polymerase chain reaction assay in patients with hepatitis b e antigen-negative chronic hepatitis b virus infection. Am J Gastroenterol 2003;98:2261-7.
- NVMDL. Richtlijn behandeling van chronische hepatitis-B-virusinfectie (2012). Ga naar bron: NVMDL. Richtlijn behandeling van chronische hepatitis-B-virusinfectie (2012).
- Lok AS, McMahon BJ. Chronic hepatitis b: Update 2009. Hepatology 2009;50:661-2.
- Hadziyannis SJ, Papatheodoridis GV. Hepatitis B e antigen-negative chronic hepatitis B: Natural history and treatment. Semin Liver Dis 2006;26:130-41.
- Wong DK, Cheung AM, O’Rourke K, Naylor CD, Detsky AS, Heathcote J. Effect of alpha-interferon treatment in patients with hepatitis B e antigen-positive chronic hepatitis B. A meta-analysis. Ann Intern Med. 1993;119:312-23.
- Van der Eijk AA, Doorduijn JK, Janssen HL, Schalm SW, Niesters HG, De Man RA. Lamivudine ter voorkoming van opvlamming van chronische hepatitis B tijdens chemotherapie voor non-Hodgkin-lymfoom. Ned Tijdschr Geneeskd 2002;146:1140-4.
- Kohrt HE, Ouyang DL, Keeffe EB. Systematic review: lamivudine prophylaxis for chemotherapy-induced reactivation of chronic hepatitis B virus infection. Aliment Pharmacol Ther 2006;24:1003-16.
- Van der Poel CL, Cuypers HT, Reesink HW. Hepatitis C virus six years on. Lancet 1994;344:1475-9.
- Conry-Cantilena C, Van Raden M, Gibble J, Melpolder J, Shakil AO, Viladomiu L, et al. Routes of infection, viremia, and liver disease in blood donors found to have hepatitis C virus infection. N Engl J Med 1996;334:1691-6.
- Health Council of the Netherlands: Committee on Hepatitis C. Detection and treatment of people with hepatitis C. Rijswijk: Health Council of the Netherlands, 1997; publication no. 1997/19.
- Di Bisceglie AM. Hepatitis C. Lancet 1998;351:351-5.
- Poynard T, Yuen MF, Ratziu V, Lai CL. Viral hepatitis C. Lancet 2003;362:2095-100.
- Lauer GM, Walker BD. Hepatitis C virus infection. N Engl J Med 2001;345:41-52.
- Götz HM, Van Doornum G, Niesters HG, Den Hollander JG, Thio HB, De Zwart O. A cluster of acute hepatitis C virus infection among men who have sex with men- results from contact tracing and public health implications. AIDS 2005;19:969-74.
- Gambotti L, Batisse D, Colin-de-Verdiere N, Aroque-Astagneau E, Desenclos JC, Dominguez S, et al. Acute hepatitis C infection in HIV positive men who have sex with men in Paris, France, 2001-2004. EuroSurveill 2005;10:115-7.
- Van de Laar TJ, Van der Bij AK, Prins M, Bruisten SM, Brinkman K, Ruys TA, et al. Increase in HCV incidence among men who have sex with men in Amsterdam most likely caused by sexual transmission. J Infect Dis 2007;196:230-8.
- Orlent H, Vrolijk JM, De Man RA, Schalm SW. Behandeling van hepatitis C. Ned Tijdschr Geneeskd 2003;147:1208-13.
- Fattovich G, Stroffolini T, Zagni I, Donato F. Hepatocellular carcinoma in cirrhosis: incidence and risk factors. Gastroenterology 2004;127:S35-S50.
- Flamm SL. Chronic hepatitis C virus infection. JAMA 2003;289:2413-7.
- Davison SM, Mieli-Vergani G, Sira J, Kelly DA. Perinatal hepatitis C virus infection: diagnosis and management. Arch Dis Child 2006;91:781-5.
- NVMDL. Richtsnoer behandeling hepatitis-C-infectie (2015). Ga naar bron: NVMDL. Richtsnoer behandeling hepatitis-C-infectie (2015).
- Berden FA, Kievit W, Baak LC, Bakker CM, Beuers U, Boucher CA, et al. Dutch guidance for the treatment of chronic hepatitis C virus infection in a new therapeutic era. Neth J Med 2014;72:388-400.
- LCI. Richtlijn Hepatitis C (2011a). De Bilt: RIVM. Ga naar bron: LCI. Richtlijn Hepatitis C (2011a). De Bilt: RIVM.
- De Gier H, Borgsteede S. Commentaren Medicatiebewaking 2014/2015. Houten: Stichting Health Base, 2014.
- Lee WM. Drug-induced hepatotoxicity. N Engl J Med 2003;349:474-85.
- De Graaf L, Van Grootheest AC. Meldingen aan lareb over mogelijke systemische effecten bij gebruik van het hormoon bevattend iud mirena. Tijdschr Huisartsgeneeskd 2002;19:134-7.
- Pratt DS, Kaplan MM. Evaluation of abnormal liver-enzyme results in asymptomatic patients. N Engl J Med 2000;342:1266-71.
- Chalasani N, Younossi Z, Lavine JE, Diehl AM, Brunt EM, Cusi K, et al. The diagnosis and management of non-alcoholic fatty liver disease: practice guideline by the American Gastroenterological Association, American Association for the Study of Liver Diseases, and American College of Gastroenterology. Gastroenterology 2012;142:1592-609.
- Jansen PL. Niet-alcoholische steatohepatitis: diagnostiek, pathogenese, behandeling en prognose. Ned Tijdschr Geneeskd 2005;149:289-94.
- Bellentani S, Bedogni G, Miglioli L, Tiribelli C. The epidemiology of fatty liver. Eur J Gastroenterol Hepatol 2004;16:1087-93.
- Musso G, Gambino R, Cassader M, Pagano G. Meta-analysis: natural history of non-alcoholic fatty liver disease (NAFLD) and diagnostic accuracy of non-invasive tests for liver disease severity. Ann Med 2011;43:617-49.
- Matteoni CA, Younossi ZM, Gramlich T, Boparai N, Liu YC, McCullough AJ. Nonalcoholic fatty liver disease: a spectrum of clinical and pathological severity. Gastroenterology 1999;116:1413-9.
- Schindhelm RK, Diamant M, Dekker JM, Tushuizen ME, Teerlink T, Heine RJ. Alanine aminotransferase as a marker of non-alcoholic fatty liver disease in relation to type 2 diabetes mellitus and cardiovascular disease. Diabetes Metab Res Rev 2006;22:437-43.
- Schindhelm RK, Dekker JM, Nijpels G, Bouter LM, Stehouwer CD, Heine RJ, et al. Alanine aminotransferase predicts coronary heart disease events: a 10-year follow-up of the Hoorn Study. Atherosclerosis 2007;191:391-6.
- Rockey DC, Caldwell SH, Goodman ZD, Nelson RC, Smith AD. Liver biopsy. Hepatology 2009;49:1017-44.
- Bohte AE, Van Werven JR, Bipat S, Stoker J. The diagnostic accuracy of US, CT, MRI and 1H-MRS for the evaluation of hepatic steatosis compared with liver biopsy: a meta-analysis. Eur Radiol 2011;21:87-97.
- Oldenburg B, Van Berge Henegouwen GP. Beleid bij verhoogde serumwaarden van aminotransferasen zonder symptomen, in het bijzonder bij non-alcoholische steatohepatitis. Ned Tijdschr Geneeskd 1999;143:506-9.
- Arnold DT, Bentham LM, Jacob RP, Lilford RJ, Girling AJ. Should patients with abnormal liver function tests in primary care be tested for chronic viral hepatitis: Cost minimisation analysis based on a comprehensively tested cohort. BMC Fam Pract 2011;12:9.
- Shao ZJ, Xu DZ, Yan YP, Li JH, Zhang JX, Zhang ZY, et al. Detection of anti-HAV antibody with dot immunogold filtration assay. World J Gastroenterol 2003;9:1508-11.
- Krawczyk A, Hintze C, Ackermann J, Goitowski B, Trippler M, Gruner N, et al. Clinical performance of the novel DiaSorin LIAISON((R)) XL murex: HBsAg Quant, HCV-Ab, HIV-Ab/Ag assays. J Clin Virol 2014;59:44-9.
- Kim S, Kim JH, Yoon S, Park YH, Kim HS. Clinical performance evaluation of four automated chemiluminescence immunoassays for hepatitis C virus antibody detection. Journal of Clinical Microbiology. 2008;46:3919-23.
- Kalsbeek CJC, Platteel VJD. Leverzorg. Kwaliteitscriteria vanuit patiëntenperspectief.
- Commissie preventie iatrogene transmissie van HBV HeH. Landelijke richtlijn preventie transmissie van hepatitis B van medisch personeel naar patiënten (2012). Ga naar bron: Commissie preventie iatrogene transmissie van HBV HeH. Landelijke richtlijn preventie transmissie van hepatitis B van medisch personeel naar patiënten (2012).
- Reitsma AM, Closen ML, Cunningham M, Lombardo PA, Minich HN, Moreno JD, et al. Infected physicians and invasive procedures: safe practice management. Clin Infect Dis 2005;40:1665-72.
- European Association for the Study of the Liver. EASL 2017 Clinical practice guidelines on the management of hepatitis B virus infection. J Hepatol 2017;67:370-98.
- Tozun N, Forbes A, Anderson MG, Murray-Lyon IM. Safety of alcohol after viral hepatitis. Lancet 1991;337:1079-80.
- Poynard T, Bedossa P, Opolon P. Natural history of liver fibrosis progression in patients with chronic hepatitis C. The OBSVIRC, METAVIR, CLINIVIR, and DOSVIRC groups. Lancet 1997;349:825-32.
- Patel K, Muir AJ, McHutchison JG. Diagnosis and treatment of chronic hepatitis C infection. BMJ 2006;332:1013-7.
- Eddy DM. A manual for assessing health practices and designing practice guidelines. Philadelphia: American College of Physicians, 1996.
- Kager PA, Cobelens FGJ. Infecties bij reizigers. II. Immunisaties. Geneesmiddelenbulletin 2001;35:107-14.
- RIVM. Landelijke richtlijn prikaccidenten (2007). Ga naar bron: RIVM. Landelijke richtlijn prikaccidenten (2007).
- Werkgroep Infectiepreventie (WIP). In ontwikkeling: Richtlijn infectiepreventie in de huisartsen- en verloskundigenpraktijk (2016).
- RIVM. Draaiboek seksaccidenten (2013) Ga naar bron: RIVM. Draaiboek seksaccidenten (2013)