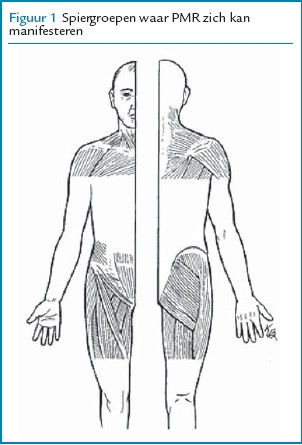
Polymyalgia rheumatica en arteriitis temporalis
Richtlijnen diagnostiek
Naar Volledige tekst ›Anamnese
Naar Volledige tekst ›Vraag bij vermoeden van Polymyalgia rheumatica (PMR) naar:
- pijn in nek, schouder- en/of heupgordel, ochtendstijfheid, ernst, invloed op het dagelijks leven;
- duur van de klachten.
Vraag naar klachten die kunnen wijzen op arteriitis temporalis:
- nieuw ontstane hoofdpijn, enkel- of dubbelzijdig;
- pijn bij het kauwen, pijn bij haren kammen;
- visusproblemen: gedeeltelijk of totaal gezichtsveldverlies, snel ontstane visusdaling, één- of dubbelzijdig, voorbijgaand of permanent, dubbelzien.
Besteed voor andere oorzaken van de klachten dan PMR of arteriitis temporalis aandacht aan:
- aanwezigheid van gezwollen gewrichten of peesscheden (Reumatoïde artritis (RA));
- temperatuur (infectie);
- malaise, verlies van eetlust, gewichtsverlies, rugpijn, hoesten (maligniteit, hypothyreoïdie);
- beloop van de klachten (infectie, maligniteit, aspecifieke klachten van het bewegingsapparaat);
- gebruik van statines, spierzwakte (myopathie).
Lichamelijk onderzoek
Naar Volledige tekst ›- actief bewegingsonderzoek van nek, schouders, heupen: let op pijn en beperkingen. Overweeg myopathie bij de aanwezigheid van krachtverlies;
- gevoeligheid gewrichtskapsels van knie, pols en vinger- en handgewrichtjes, zwellingen ter plaatse gewrichten vinger/hand: overweeg RA;
- pijn of zwelling bij palpatie arteria temporalis, aanwezigheid pulsaties arteria temporalis.
Verricht afhankelijk van de bevindingen bij de anamnese en het lichamelijk onderzoek uitgebreider lichamelijk onderzoek, gericht op andere oorzaken.
Aanvullend onderzoek
Naar Volledige tekst ›Bepaal de bezinkingssnelheid erytrocyten (BSE) en verricht bij een verhoogde BSE verder aanvullend bloedonderzoek:
- bloedbeeld (infectieziekten, maligniteit);
- thyroïd stimulerend hormoon (TSH);
- totaal eiwit en eiwitspectrum (multipel myeloom);
- creatininekinase (CK) (myopathie door statines, poly-/dermatomyositis).
Anamnese en lichamelijk onderzoek kunnen een indicatie geven voor verder aanvullend onderzoek.
Evaluatie
Naar Volledige tekst ›Sluit veelvoorkomende aandoeningen uit die zich op vergelijkbare wijze kunnen presenteren als PMR:
- reumatoïde artritis (voor diagnostische kenmerken zie NHG-Standaard Artritis);
- hypothyreoïdie.
Overweeg daarnaast of andere aandoeningen het beeld kunnen verklaren: infectieziekte, maligniteit, tendino-artrogene nek en schouder- of heupklachten, myopathie, aspecifieke klachten van het bewegingsapparaat (zie tekst standaard).
Stel, wanneer de klachten redelijkerwijs niet door een andere oorzaak kunnen worden verklaard, de diagnose PMR bij patiënten ouder dan vijftig jaar met:
- bilaterale pijn in nek en schouder- en/of heupgordel met daardoor bewegingsbeperking, én
- klachten die gerekend van moment van eerste klachten langer dan vier weken bestaan, én
- ochtendstijfheid > 60 min, én
- BSE > 40 mm/uur.
Richtlijnen beleid
Naar Volledige tekst ›Voorlichting
Naar Volledige tekst ›- Aandoening met onbekende oorzaak, behandeling bestaat uit glucocorticoïden gedurende een tot twee jaar.
- Regelmatige controles zijn nodig, glucocorticoïden mogen nooit ineens worden gestaakt.
- Neem contact op bij koorts of bij verschijnselen van arteriitis temporalis: niet-bekende hoofdpijn, of acute visusdaling, blindheid (eenzijdig en soms kortdurend) of dubbelzien.
Medicamenteuze behandeling
Naar Volledige tekst ›Behandel PMR met prednis(ol)on, dosering volgens tabel 1.
Controles
Naar Volledige tekst ›Verricht één controle na 1 en na 4 weken en één tot 4 weken na iedere dosisverandering.
- Beoordeel ten opzichte van de vorige controle:
- de klachten: pijn, stijfheid en bewegingsbeperking;
- nieuwe klachten of symptomen, passend bij een alternatieve diagnose;
- gebruik medicatie: bijwerkingen, inname adequaat.
- Bepaal de BSE vier weken na de start van de behandeling en controleer dit steeds een tot vier weken na iedere dosisverandering. Heroverweeg de diagnose en stel het afbouwschema bij als de BSE oploopt.
- Bepaal de nuchtere glucose voorafgaand aan de start van de behandeling en na drie tot zeven dagen.
- Controleer in het begin van de behandeling de bloeddruk regelmatig.
Verwijzing of consultatie
Naar Volledige tekst ›Verwijs bij:
- acute visusdaling, (geheel of gedeeltelijk) gezichtsveldverlies of dubbelzien met spoed naar de oogarts;
- vermoeden van arteriitis temporalis naar een reumatoloog/internist binnen 24 uur;
- ernstige bijwerkingen van of contra-indicaties voor langdurig gebruik van glucocorticoïden naar de reumatoloog/internist voor een eventuele behandeling met methotrexaat.
Verwijs naar of consulteer een reumatoloog/internist:
- bij uitblijven van klinische verbetering na een week behandeling;
- als er na vier weken geen duidelijke klinische verbetering is én de BSE niet daalt;
- bij regelmatige terugval (meer dan twee maal per jaar);
- als het niet mogelijk is de glucocorticoïddosering te verminderen;
- bij twijfel aan de diagnose.
Kernboodschappen
Naar Samenvatting ›Polymyalgia rheumatica
Naar Samenvatting ›- Stel de diagnose polymyalgia rheumatica (PMR) bij patiënten > 50 jaar met:
- bilaterale pijn en stijfheid in de nek en schouderregio en/of heup/bekkenregio, met door de pijn veroorzaakte bewegingsbeperking, die gerekend vanaf het moment van de 1e klachten > 4 weken bestaan, én
- ochtendstijfheid > 60 minuten, én
- BSE > 40 mm/uur
- Wees bij de diagnostiek en de controles alert op aanwijzingen voor een andere diagnose.
- De diagnostiek richt zich daarom grotendeels op het uitsluiten van (soms ernstige) ziektebeelden die zich op vergelijkbare wijze kunnen presenteren als PMR.
- Bij de controles is vooral waakzaamheid geboden bij onvolledige of afwezige verbetering op prednis(ol)on.
- Start na het stellen van de diagnose met prednis(ol)on 15 mg/dag gedurende 1 maand. Verminder de dosis daarna geleidelijk in 1 tot 2 jaar.
Arteriitis temporalis
Naar Samenvatting ›- PMR kan gepaard gaan met arteriitis temporalis. Arteriitis temporalis is een potentieel ernstige aandoening vanwege complicaties, zoals blindheid.
- Bij aanwijzingen voor arteriitis temporalis is het noodzakelijk dat de patiënt binnen 24 uur na presentatie door de reumatoloog/internist wordt beoordeeld.
- Verwijs de patiënt met spoed naar de oogarts bij:
- (geheel of gedeeltelijk) gezichtsveldverlies
- acute visusdaling
- dubbelzien
Inleiding
Naar Samenvatting ›Scope
Naar Samenvatting ›- Richtlijnen voor de diagnostiek en behandeling van polymyalgia rheumatica (PMR). De standaard vervangt de Farmacotherapeutische richtlijn Polymyalgia rheumatica (2007) (zie Details).
- De standaard besteedt daarnaast aandacht aan arteriitis temporalis voor zover deze gepaard gaat met PMR. Bij arteriitis temporalis kan hoofdpijn op de voorgrond staan.
- Doelen van deze standaard zijn (zie Details):
- patiënten met symptomen die kunnen wijzen op PMR herkennen
- voldoende betrouwbaar andere aandoeningen uitsluiten
- aanbevelingen geven voor een adequate behandeling, rekening houdend met de frequent voorkomende comorbiditeit gezien de leeftijd waarop PMR voorkomt
- arteriitis temporalis herkennen en tijdig verwijzen
De huidige standaard vervangt de Farmacotherapeutische richtlijn Polymyalgia rheumatica uit 2006, die een meer beschrijvend karakter had. De standaard gaat met name uitgebreider in op de differentiaaldiagnose van polymyalgia rheumatica en geeft duidelijkere aanbevelingen. Daarnaast is de standaard voorzien van uitgebreide details.
Bahlas et al. voerden een retrospectief dossieronderzoek uit bij 123 door huisartsen naar een derdelijns reumatologische kliniek (Canada) verwezen patiënten bij wie uiteindelijk de diagnose PMR werd gesteld. Slechts bij 25% van de ingestuurde patiënten veronderstelde de huisarts in de verwijsbrief PMR.
Achtergronden
Naar Samenvatting ›Polymyalgia rheumatica
Naar Samenvatting ›Kenmerken
Naar Samenvatting ›- PMR is een syndroom dat wordt gekenmerkt door (zie Details):
- symmetrische pijn en stijfheid in de nek en schouderregio en/of heup/bekkenregio (zie figuur 1)
- ochtendstijfheid
- (meestal) een verhoogde BSE
- De diagnose kan pas worden gesteld als de klachten enige weken bestaan (zie Details).
Ondanks overeenstemming over het klinisch beeld zijn er geen standaard tests of algemeen geaccepteerde criteria voor PMR. Verschillende sets van diagnostische criteria worden in de literatuur beschreven (Bird, Jones/Hazleman, Hunder, Healey, Chuang). Vooral de criteria van Bird en van Jones/Hazleman, hoewel de laatste met name bedoeld waren als inclusiecriteria voor trials, worden in de literatuur veelvuldig gebruikt. Ook over de behandeling bestaat geen consensus. Verbetering door corticosteroïden werd in twee sets van diagnostische criteria als belangrijk kenmerk gezien (Jones-Hazleman, Healey). Anderen vonden juist dat met introductie van dit kenmerk de kans op diagnostische fouten toenam. Het gebrek aan overeenstemming rond de diagnostische criteria maakt ook onderzoeken rond PMR onderling moeilijker vergelijkbaar. Een internationale werkgroep is ingesteld om criteria voor PMR vast te stellen, onder auspiciën van de American College of Rheumatology en European League Against Rheumatism. De ontwikkeling van criteria heeft tot doel PMR te onderscheiden van andere ziekten met een vergelijkbare presentatie. In drie Delphi consensusrondes, aanvankelijk met experts en later met reumatologen en niet-reumatologen, is een set van zeven criteria vastgesteld, waarvan in prospectief onderzoek de bruikbaarheid moet worden vastgesteld: leeftijd > 50 jaar, duur klachten > 2 weken, bilaterale pijn aan schouder- en/of heupgordel, ochtendstijfheid > 45 min, verhoogde BSE, verhoogde CRP, snelle klinische en biochemische respons (> 75% globale respons < 1 week) op predniso(lo)n 15 tot 20 mg/dag.
Criteria van Bird
3 of meer van de volgende criteria, of ten minste 1 van de volgende criteria + positieve a.temporalis biopsie:
|
Criteria Jones en Hazleman
Alle volgende criteria:
|
Criteria van Chuang en Hunder
Alle onderstaande criteria:
|
Criteria van Healey
Alle onderstaande criteria:
|
De BSE kan, onafhankelijk van een ziekteproces, worden beïnvloed door geslacht, leeftijd en medicatiegebruik. Referentiewaarden van de bovengrens van de BSE zijn vastgesteld voor personen onder of boven de vijftig jaar. De LESA Rationeel aanvragen van laboratoriumdiagnostiek hanteert voor vrouwen onder en boven de vijftig jaar een bovengrens van 20 mm/uur respectievelijk 30 mm/uur en voor mannen onder en boven de vijftig jaar van 15 mm/uur respectievelijk 20 mm/uur (zie www.nhg.org).
De BSE en de CRP worden beide als parameter gebruikt bij de diagnostiek en de follow-up van PMR.
PMR kan voorkomen zonder verhoogde BSE. In verschillende (retrospectieve) patiëntenseries wordt bij 7 tot 22% een normale BSE gevonden. Het gebruikte afkappunt voor de BSE varieert tussen 30 tot 40 mm/uur. In een overzichtsartikel worden de volgende kenmerken van de groep PMR met lage BSE genoemd: relatief jongere leeftijd, langere duur van klachten voor het stellen van de diagnose, minder systemische verschijnselen, minder voorkomen van laboratoriumafwijkingen zoals anemie. Daarentegen was er geen verschil in aantal malen terugval of de prevalentie van reumatoïde artritis vergeleken met de groep met verhoogde BSE. Opmerkelijk was dat in de groep met PMR en een normale BSE niemand een arteriitis temporalis ontwikkelde. Het merendeel van de patiënten met PMR en een normale BSE blijkt wel een verhoogde CRP te hebben.
In een prospectief follow-uponderzoek in een tweedelijns centrum voor reumatologie (Italië) werd bij 177 opeenvolgende patiënten met PMR (criteria van Healey) bij de diagnostiek en gedurende de follow-up de BSE (Westergren methode) en CRP gemeten. Voor leeftijd en geslacht gematchte gezonde personen dienden als controles. Van de patiënten (voornamelijk mannen) had 8,5% een normale BSE (< 40 mm/uur) bij het stellen van de diagnose en 1,1% een normale CRP < 0,5 mg/dl). Patiënten met een hogere BSE hadden meer systemische verschijnselen. Voor de kans op terugval was de BSE bij diagnosestelling een betere voorspeller dan de CRP. De CRP daarentegen was een meer sensitieve indicator voor de huidige activiteit van de ziekte.
In een gecombineerd prospectief en retrospectief Noors onderzoek bij patiënten met PMR (n = 268) bleek dat de BSE (> 40 mm/uur) bij 97,7% van patiënten verhoogd was en CRP (≥ 10 mg/l) bij 94,8%. Bij 1,5% van de patiënten waren zowel BSE als CRP normaal. Daarnaast werden afwijkende leverenzymen gevonden: in 13,8% van de gevallen ging het om een verhoging van de ALAT, in 29,2% om een verhoging van de gGT en in 8,5% om een verhoging van de AF.
Conclusie
In verschillende onderzoeken betreffende PMR wordt de bepaling van de CRP, naast of in plaats van de BSE, aanbevolen. Ook wordt gesteld dat de CRP een meer sensitieve indicator van de activiteit van PMR is dan de BSE en bruikbaar kan zijn bij de diagnostiek en follow-up van de ziekte. De werkgroep kiest voor het gebruik van de BSE bij de diagnostiek en de follow-up van polymyalgia rheumatica om de volgende redenen: de CRP heeft geen meerwaarde boven de BSE, met het gebruik van de BSE bij PMR bestaat veel ervaring in de huisartsenpraktijk, de bepaling van de BSE is gemakkelijk (in de praktijk) uit te voeren en het gebruik van de BSE sluit aan bij reeds bestaande criteria.
In een gecombineerd prospectief (n = 287) en retrospectief onderzoek (n = 48) in Noorwegen werden patiënten met PMR en/of arteriitis temporalis (door reumatoloog vastgesteld op basis van criteria van Bird of Hamrin voor PMR of criteria van de ACR voor arteriitis temporalis) gevolgd tot het moment van stoppen van de therapie en complete remissie. In de prospectieve groep hadden 233 patiënten PMR (81,2%), 39 patiënten arteriitis temporalis zonder PMR (13,6%) en 15 patiënten PMR én arteriitis temporalis (5,2%). In de retrospectieve groep hadden 19 patiënten PMR, 10 patiënten arteriitis temporalis en 2 patiënten beide. De combinatie van arteriitis temporalis en PMR kwam bij vrouwen tweemaal zo vaak voor als bij mannen. De gemiddelde leeftijd bij het optreden van de ziekte was 71,7 jaar (spreiding 53 tot 89 jaar). Onderscheiden werden de eerste symptomen van de ziekte en de symptomen op het moment van presentatie bij de arts. Bij PMR was de meest voorkomende klacht pijn en stijfheid van de schouderregio (21% aanwezig bij eerste symptomen van de ziekte en 78% bij presentatie); voor pijn en stijfheid van de heupgordel was dit respectievelijk 16 en 65%. In minder dan een kwart van de gevallen waren er klachten van pijn en stijfheid van de nek, schouder, proximale armen, heupen en bovenbenen als eerste verschijnselen van de ziekte, terwijl bij presentatie het merendeel van de patiënten deze klachten had. Nachtzweten en gewichtsverlies werden weinig gemeld als eerste symptomen van de ziekte en werden in respectievelijk 42 en 29% van de gevallen bij de eerste presentatie gemeld.
Bij arteriitis temporalis was hoofdpijn bij 54% van de patiënten het eerste verschijnsel van de ziekte, terwijl dit bij presentatie 85% was. In een kwart van de gevallen ging het hierbij om temporale hoofdpijn. Bij presentatie was occipitale hoofdpijn bijna net zo vaak aanwezig als temporale hoofdpijn. Het onderzoek vermeldt niet of het om enkel of dubbelzijdige hoofdpijn ging. Bij PMR had ongeveer 25% van de patiënten klinisch aantoonbare ontsteking van de perifere gewrichten (60% knie, 36% pols, 38% hand en 9% enkel, 8% sternoclaviculair en 2% heup). 4% had polyartritis. Bij arteriitis temporalis was geen perifere artritis aanwezig. Eén patiënt met arteriitis temporalis had beiderzijds een compleet verlies van de visus en zeven patiënten met arteriitis temporalis meldden dat ze enig visusverlies hadden gehad. Er bleken geen significante verschillen in klinische presentatie tussen mannen en vrouwen.
In meer dan de helft van de patiënten met PMR was het begin van de klachten acuut (56,3%), bij arteriitis temporalis (of de combinatie van arteriitis temporalis en PMR) was dit 74,5%.
Conclusie
Bij presentatie bij de dokter had het merendeel van de patiënten met PMR klachten van de schouderregio en de heupgordel, maar ook van de nek, bovenarmen en bovenbenen. Bij arteriitis temporalis is hoofdpijn de meest frequente klacht bij presentatie.
Epidemiologie
Naar Samenvatting ›- PMR komt vrijwel uitsluitend boven het 50e levensjaar voor.
- De incidentie van PMR:
- ligt in de huisartsenpraktijk waarschijnlijk tussen 0,5 tot 1 per 1000 patiënten per jaar
- neemt toe met de leeftijd; de meeste gevallen doen zich voor na het 70e levensjaar
- De ratio vrouw-man ligt tussen 2-3:1 (zie Details).
- PMR wordt vaker gemeld in Noord-Europese landen.
- Van de patiënten met PMR heeft of ontwikkelt 5-15% eveneens arteriitis temporalis (zie Details).
Er is een grote variatie in de incidentie van PMR in verschillende onderzoeken. Verklaringen voor deze variatie kunnen zijn: een gebrek aan uniforme criteria voor de diagnose PMR, het meer of minder gespitst zijn op de diagnose of een daadwerkelijke geografische variatie.
In een review over de epidemiologie van PMR bleek dat in Scandinavische onderzoeken tienmaal hogere incidenties van PMR werden gevonden dan in onderzoeken uit Zuid-Europa (1,13/1.000 versus 0,12/1.000). Daarbij werd een positieve correlatie gevonden tussen de incidentie en de breedtegraad waarop het onderzoek werd uitgevoerd. Ook nam de incidentie in de loop van de tijd toe.
In de meeste patiëntenseries zijn voornamelijk patiënten met Europese voorouders vertegenwoordigd. Ook bij mensen van Afrikaanse afkomst komen PMR en arteriitis temporalis voor; presentatie, beloop en reactie op behandeling lijken gelijk te zijn tussen deze verschillende patiëntenpopulaties.
Bij analyse van EMD’s van huisartsenpraktijken in Groot-Brittannië (GPRD) over de periode 1990 tot 2001 bleek de incidentie van PMR 0,84 (95%-BI 0,83 tot 0,86) per 1.000. De ratio vrouw/man was 2,0. De incidentie nam toe van 0,69/1.000 in 1990 naar 0,93/1.000 in 2001. De incidentie steeg sterk met de leeftijd: van 0,98/1.000 bij 60- tot 69-jarigen naar 22,9/1.000 bij 70- tot 79-jarigen en 22,2/1.000 bij mensen boven de 80 jaar. De gemiddelde leeftijd waarop de diagnose werd gesteld was 72,7 jaar.
De incidentie van arteriitis temporalis bleef in de periode 1990 tot 2001 nagenoeg gelijk 0,22 (95%-BI 0,21 tot 0,23) Opmerkelijk is dat de incidentie in het zuiden van Groot-Brittannië hoger was dan in het noorden.
In de Nederlandse Continue Morbiditeitsregistratie (CMR) werden in zestien jaar tijd (1985 tot 2001) 95 gevallen van PMR geregistreerd met een incidentie van 0,2/1.000 bij mannen en 0,7/1.000 bij vrouwen. In ruim driekwart (76/95) van de gevallen ging het om patiënten ouder dan 65 jaar.
Uit dossieronderzoek in de eerste lijn in Groot-Brittannië over de periode 1990 tot 2001 werden 15.013 patiënten met de diagnose PMR en 3928 patiënten met de diagnose arteriitis temporalis geïdentificeerd. Bij 5,2% van de patiënten werd, voordat de diagnose PMR werd gesteld, de diagnose arteriitis temporalis gesteld. Bij 2,5% van de patiënten werd de diagnose arteriitis temporalis gesteld nadat de diagnose PMR was gesteld. Bij de 3928 patiënten met de diagnose arteriitis temporalis werd bij 14,9% voorafgaand de diagnose PMR vastgesteld en bij 14,2% achteraf.
Klachten en symptomen
Naar Samenvatting ›- De meest voorkomende klacht is continue, door beweging toenemende pijn en ochtendstijfheid in de nek en schouderregio en/of heup/bekkenregio. Deze klachten kunnen snel (in een periode van 1 tot 7 dagen) of geleidelijker ontstaan en ze beïnvloeden het uitoefenen van de dagelijkse bezigheden (zie Kenmerken). Meestal zijn de klachten beiderzijds aanwezig, maar ze kunnen asymmetrisch beginnen.
- Tot maximaal 50% van de patiënten heeft ook symptomen meer distaal (zie Details), zoals:
- artritis van de polsen
- pitting-oedeem van het distale gedeelte van de extremiteiten
- Bij presentatie heeft ruim 1/3 van de patiënten systemische verschijnselen, zoals:
- subfebriele temperatuur
- malaise
- vermoeidheid
- anorexie
- gewichtsverlies
- Daarnaast kunnen een lichte normocytaire anemie (anemie bij een chronische ziekte) of afwijkende leverfunctie waarden worden gevonden (zie Kenmerken).
- PMR heeft een uitgebreide differentiaaldiagnose (zie Details), waaronder:
- reumatoïde artritis
- myopathie door statines
- artrose
- hypothyreoïdie
- maligniteiten
- De periode vanaf het moment dat de 1e klachten zich manifesteren tot het moment dat de diagnose wordt gesteld, kan 1 tot enkele maanden duren (zie Details).
- Hoewel PMR en arteriitis temporalis samen kunnen vóórkomen, is de precieze relatie tussen beide niet bekend (zie Details). Arteriitis temporalis kan vanaf het begin aanwezig zijn, maar kan zich ook tijdens het beloop van PMR ontwikkelen.
- De pathogenese van PMR is onbekend. Bij beeldvormende diagnostiek zijn soms ontstekingsverschijnselen van synoviale structuren vast te stellen (zie Details).
In een prospectief follow-uponderzoek (twee reumatologische klinieken in Italië) van 177 opeenvolgende patiënten met PMR (Healey criteria) over een periode van vijf jaar hadden 45% van de patiënten distale articulaire en/of tenosynoviale symptomen bij de diagnose en gedurende de follow-up, 25% had een perifere artritis, 14% een CTS, 12% pitting oedeem van het distale deel van een extremiteit. In 31% van de gevallen waren distale manifestaties de enige uiting van een recidief. In een prospectief follow-uponderzoek in de tweede lijn (Italië) (n = 74) werd bij 51% een distale manifestatie van PMR (criteria Chuang) gevonden: 39% perifere synovitis (met name pols, MCP-gewrichten en knie), 5% pitting oedeem van de hand, 5% CTS en 1,3% distale tenosynovitis. In een tweedelijnsonderzoek (n = 287; Noorwegen) had ongeveer 25% van de patiënten met PMR een klinisch aantoonbare ontsteking van de perifere gewrichten.
Conclusie
Distale manifestaties van PMR, zoals artritis van perifere gewrichten, oedeem van hand of voet, carpaletunnelsyndroom en tenosynovitis, komen bij maximaal 50% van de patiënten voor. Deze kunnen aanwezig zijn vanaf het begin van de ziekte, maar ook (soms de enige) uiting zijn van een recidief.
Veel ziekten kunnen op PMR lijken, doordat ze gepaard gaan met myalgie. In een aantal overzichtsartikelen worden de volgende ziektebeelden genoemd in de differentiaaldiagnose van PMR: degeneratieve aandoeningen (zoals artrose, frozen shoulder), endocriene aandoeningen (hypothyreoïdie, hyperparathyreoïdie), infectieziekten ((prodromen van) virusziekten, tuberculose (TBC), endocarditis), inflammatoire systemische ziekten (RA, SLE, polymyositis), spierziekten (myopathie), maligniteit (hematopoietische maligniteiten, waaronder multipel myeloom en leukemie, longcarcinoom, carcinomen van urologische origine, ovariumcarcinoom, prostaatcarcinoom, coloncarcinoom, maagcarcinoom en pancreascarcinoom), neurologische aandoeningen (ziekte van Parkinson, myasthenie), psychiatrische zieken (depressie), bijwerkingen van medicatie (myositis door statines) en overige aandoeningen zoals fibromyalgie.
In een Noorse prospectief onderzoek van 287 door de huisarts verwezen patiënten met PMR en/of arteriitis temporalis bleek het gemiddelde diagnostische delay vanaf de eerste klachten tot de diagnose bij patiënten met PMR 2,9 maanden (spreiding 0,25 tot 18), bij de combinatie van PMR en arteriitis temporalis 1,9 maanden (0,5 tot 5) en bij arteriitis temporalis 1,5 maanden (0,25 tot 7).
Sommigen zien PMR en arteriitis temporalis als verschillende fases van dezelfde ziekte, anderen postuleren dat het om verschillende, maar vaak ook overlappende, ziektebeelden gaat. Hoewel het klinisch beeld anders is, gaan beide aandoeningen gepaard met een verhoogde BSE/CRP, systemische verschijnselen en snelle verbetering op glucocorticoïden.
In een review werd het bewijs rond de relatie tussen PMR en arteriitis temporalis beschreven. Geconcludeerd werd dat PMR en arteriitis temporalis met enige regelmaat samen voorkomen, maar dat de onderliggende oorzaak hiervan onduidelijk is.
Het is niet duidelijk of het pathofysiologisch mechanisme bij PMR een vasculitis, een synovitis of een combinatie van beide is. Uit beeldvormende diagnostiek blijkt dat het ontstekingsproces bij PMR zich afspeelt in extra-articulaire structuren, meestal de bursae bij gewrichten.
Prognose
Naar Samenvatting ›- De prognose van PMR is goed. Bij behandeling met glucocorticoïden treedt snel verbetering op; meestal zijn de klachten binnen enkele dagen tot 1 week grotendeels verdwenen.
- Onbehandeld is de duur van de aandoening soms > 5 jaar (zie Details). PMR kan recidiveren, maar heeft geen invloed op de levensverwachting (zie Details).
Het natuurlijk beloop van reumatoïde artritis zonder artritis, vanaf 1957 door Barber PMR genoemd, wordt in een aantal onderzoeken, voordat behandeling met glucocorticoïden gebruikelijk was, beschreven. Verondersteld wordt dat dit drie maanden tot 35 jaar kon duren, met een gemiddelde duur van 7,1 jaar.
Om vast te stellen of patiënten met PMR een vergroot risico hebben op perifere arteriële vaatziekten werden in een Amerikaans cohortonderzoek patiënten met PMR (n = 353) vergeleken met patiënten zonder PMR. Iedere patiënt met PMR werd vergeleken met twee patiënten zonder PMR. De 353 PMR-patiënten hadden een gemiddelde leeftijd van 73,3 jaar, 67% was vrouw. De 705 patiënten zonder PMR hadden een gemiddelde leeftijd van 73,2 jaar en 68% was vrouw. Meer dan 95% van de patiënten was 'wit' (het artikel spreekt over "US white population"). De gemiddelde follow-up was elf jaar. Na correctie voor risicofactoren voor hart- en vaatziekten bleek dat patiënten met PMR een significant verhoogd risico hadden op perifere arteriële vaatziekten (hazard ratio 2,50; 95%-BI 1,53 tot 4,08) ten opzichte van patiënten zonder PMR. Er was geen verschil in mortaliteit tussen patiënten met of zonder PMR, noch tussen de PMR-patiënten met of zonder perifere arteriële vaatziekten.
In een retrospectief cohortonderzoek (n = 364) werd het effect van behandeling van PMR met glucocorticoïden op het optreden van HVZ onderzocht. De gemiddelde leeftijd was 73 jaar, 67% was vrouw. 85% Van de patiënten kreeg glucocorticoïden. Behandeling met glucocorticoïden gaf geen verhoogd risico op cardiovasculaire ziekten. De hazard ratio voor myocardinfarct, hartfalen, perifere vaatziekten of CVA was respectievelijk 0,59 (95%-BI 0,27 tot 1,27), 0,81 (95%-BI 0,41 tot 1,60), 0,60 (95%-BI 0,23 tot 1,55) en 0,75 (95%-BI 0,37 tot 1,54).
Conclusie
In een observationeel onderzoek werd een verband gevonden tussen perifeer arterieel vaatlijden en PMR. Er was echter geen verband met mortaliteit. Er werd geen verband gevonden tussen de behandeling van PMR met glucocorticoïden en HVZ.
Arteriitis temporalis
Naar Samenvatting ›Kenmerken
Naar Samenvatting ›- Arteriitis temporalis, ook wel reuscelarteriitis genoemd, is een vasculitis. Deze kan zich, naast de meest voorkomende manifestatie in de arteria temporalis, nog op andere locaties voordoen. De grote en middelgrote arteriën die uit de aortaboog ontspringen, meestal de arteria carotis externa en de extracraniële takken van de arteria carotis interna, zijn daarbij aangetast (zie Details).
- Het aantonen van de kenmerkende granulomateuze ontsteking van de vaatwand is bewijzend voor de diagnose arteriitis temporalis, waarbij soms de typische reuscellen worden aangetroffen.
In 15% van de gevallen beperkt de vasculitis zich niet tot de arteria temporalis en zijn de arterietakken van de aortaboog betrokken, vooral de arteria subclavia en arteria axillaris. Dit kan leiden tot claudicatio van de arm. Voor het aantonen van een reuscelarteriitis op andere lokalisaties dan de arteria temporalis zijn andere diagnostische modaliteiten, zoals angiografie of MRA, dan de biopsie geschikt.
Epidemiologie
Naar Samenvatting ›- Arteriitis temporalis komt bijna uitsluitend voor boven het 50e levensjaar.
- De incidentie van arteriitis temporalis is naar schatting 0,2 per 1000 patiënten > 50 jaar (zie Details).
- Van de patiënten met arteriitis temporalis heeft of ontwikkelt 40-60% eveneens PMR.
De incidentie van arteriitis temporalis in Noord-Europa en bij de Angelsaksische bevolking in de VS wordt geschat op 0,2/1.000 bij personen boven de vijftig jaar en is bij vrouwen twee maal zo hoog als bij mannen. Net als PMR komt arteriitis temporalis in Europa vaker voor op hogere breedtegraden en is de prevalentie (zeer) laag in Japan, Azië en Arabische landen. Ongeveer de helft van patiënten met arteriitis temporalis heeft verschijnselen passend bij PMR.
Klachten en symptomen
Naar Samenvatting ›- De symptomen van arteriitis temporalis zijn gerelateerd aan:
- het systemische ontstekingsproces
- de vasculaire schade door dit ontstekingsproces of door de ischemie die veroorzaakt wordt door vernauwing of occlusie van het lumen van de arterie
- Het klinisch beeld kan soms vrij acuut beginnen, maar ontwikkelt zich meestal geleidelijk in enkele weken.
- Hoewel nieuw ontstane hoofdpijn de belangrijkste reden is voor klinisch vermoeden van arteriitis temporalis, is er geen specifiek type hoofdpijn; evenmin is er een andere klinische presentatie die specifiek is voor arteriitis temporalis.
- De meest voorkomende symptomen zijn:
- niet eerder bekende, heftige, uni- of bilaterale, stekende, soms bonzende hoofdpijn, meestal bij de slapen
- stekende gevoeligheid van de hoofdhuid
- pijn bij het kauwen
- uni- of bilaterale visusklachten en/of klachten passend bij PMR
- Visusklachten kunnen bestaan uit blindheid, die aanvankelijk eenzijdig en soms in korte tijd tweezijdig kan worden, maar ook uit tijdelijk (duur enkele seconden (amaurosis fugax) tot enkele uren), soms gedeeltelijk, soms totaal visusverlies van 1 oog, met uiteindelijk verlies van gezichtsscherpte of dubbelzien.
- De visusklachten kunnen voorbijgaand of blijvend zijn (zie Details).
- Eenmaal opgetreden blindheid is, ondanks behandeling met glucocorticoïden, bijna altijd irreversibel, tenzij in een zeer vroeg stadium met de behandeling wordt gestart.
- Arteriitis temporalis kan gepaard gaan met systemische verschijnselen, zoals:
- koorts
- verlies van eetlust
- gewichtsverlies
- Bevindingen bij lichamelijk onderzoek die bij arteriitis temporalis passen, zijn pijnlijke, verdikte, knobbelig aanvoelende takken van de arteria temporalis superficialis, waarvan de pulsaties niet meer voelbaar zijn en waarboven de huid rood verkleurd kan zijn. De BSE is in het algemeen verhoogd.
- Criteria voor arteriitis temporalis, oorspronkelijk bedoeld voor onderzoek, voldoen voor de diagnostiek niet goed (zie Richtlijnen diagnostiek). Om de diagnose arteriitis temporalis met meer zekerheid te kunnen stellen is een biopt van de arteria temporalis noodzakelijk (zie Details).
- Gezien de mogelijke betrokkenheid van andere arteriën kan de diagnostiek complex zijn. Mede door de ernst van de potentiële complicaties (blindheid, thoracale aorta-aneurysma/aortadissectie) worden patiënten met een vermoeden van arteriitis temporalis verwezen naar de reumatoloog/internist.
- Verwijs patiënten met spoed naar de oogarts in geval van visusklachten.
- De pathogenese van arteriitis temporalis is onbekend.
Arteriitis temporalis kan gepaard gaan met visusklachten. Ongeveer 20% van de patiënten met arteriitis temporalis presenteert zich met visusklachten zoals blindheid, die aanvankelijk eenzijdig en later tweezijdig kan worden, maar ook met tijdelijk (duur enkele seconden (amaurosis fugax) tot enkele uren), soms gedeeltelijk, soms totaal visusverlies van één oog, met verlies van gezichtscherpte of met dubbelzien. In patiëntenseries heeft ongeveer 15 tot 20% van de patiënten uiteindelijk blijvend visusverlies. In een retrospectief follow-up onderzoek gedurende vijf jaar (n = 245) bleek de kans op blijvend visusverlies na de start van de behandeling met glucocorticoïden afhankelijk te zijn van het moment van het ontstaan van de visusproblemen. De kans op blijvend visusverlies was 1% als deze ontstond na de start van de behandeling en 13% als deze reeds aanwezig was op het moment dat de behandeling werd gestart.
Oculaire beschadigingen treden op afhankelijk van de lokalisatie van de arterie en de mate waarin de arterie is aangetast. Er moet voldoende aantasting zijn om tot ischemie te leiden. Anterieure ischemische optische neuropathie is de meest voorkomende oculaire manifestatie van arteriitis temporalis. Daarnaast kan occlusie van de arteria centralis retinae of posterieure ischemische neuropathie van de nervus opticus optreden.
Conclusie
Door de ernst van de complicaties, de soms snelle progressie en de beperkte mogelijkheid om eenmaal opgetreden visusverlies te behandelen, vereisen nieuw opgetreden visusproblemen bij een vermoeden van arteriitis temporalis een spoedverwijzing.
Een biopsie van de arteria temporalis is de beste manier om arteriitis temporalis aan te tonen. De sensitiviteit van de biopsie ligt tussen 60 tot 80% wanneer de uiteindelijke klinische diagnose als gouden standaard wordt gezien. Ervaring in het nemen van een biopsie en het niet duidelijk aangetast zijn van de arteria temporalis in het kader van een reuscelarteritis hebben invloed op de uitslag van de biopsie.
Om het effect van reeds gestarte behandeling met glucocorticoïden op het biopsieresultaat bij vermoeden van arteriitis temporalis te meten, werd een cohort van 535 opeenvolgende patiënten die een temporalisbiopsie ondergingen (derdelijnscentrum in de VS) bekeken. Ongeveer de helft van de patiënten (n = 249) had tevoren een behandeling met een glucocorticoïd (> 15 mg/dag) gehad, van wie 107 patiënten korter dan één week en 32 patiënten langer dan twee weken. Alle patiënten hadden verschijnselen die op een arteriitis temporalis konden wijzen: 60% had een nieuw ontstane hoofdpijn, 73% had klachten conform de ACR-criteria, 35% had oculaire klachten of symptomen, 75% had een verhoogde BSE (> 40 mm/uur). De gemiddelde leeftijd van de patiënten was 71jaar (spreiding 31 tot 93). Een biopsie werd geclassificeerd als positief (met een onderscheid tussen typisch en atypisch) of negatief. De interbeoordelaarsbetrouwbaarheid van de histologische bevindingen was goed (kappa 0,87). Een biopsie van de contralaterale zijde werd genomen als de aangedane zijde een negatieve biopsie opleverde. 175 patiënten (33%) hadden een positieve biopsie, waarvan 49% typisch. Van de onbehandelde patiënten had 31% een positieve biopsie en van de behandelde patiënten 35%.
Conclusie
Een biopsie van de arteria temporalis kan tot meer dan veertien dagen na de start van de behandeling met corticosteroïden nog verschijnselen van arteriitis vertonen bij patiënten met aanwijzingen voor arteriitis temporalis.
Prognose
Naar Samenvatting ›De prognose wordt bepaald door:
- visusklachten
- ischemie door lumenvernauwing van betrokken vaten
- het optreden van thoracale aneurysmata/aortadissectie
- glucocorticoïdgerelateerde bijwerkingen
Richtlijnen diagnostiek
Naar Samenvatting ›- Enkele weken bestaande klachten van pijn en (ochtend)stijfheid in de nek en schouderregio en/of heup/bekkenregio bij patiënten > 50 jaar moeten een reden zijn om aan PMR te denken.
- Door het ontbreken van objectieve diagnostische criteria en van een eenduidig pathofysiologisch mechanisme, in combinatie met het beperkte onderscheidend vermogen van de huidige diagnostische criteria, is PMR lastig af te grenzen van aandoeningen met overeenkomstige verschijnselen (zie Details).
- Diagnostische accuratesse is mede geboden vanwege de vaak lange duur van de behandeling met glucocorticoïden en de daarmee gepaard gaande bijwerkingen.
- Voor de diagnostiek (en de behandeling) van PMR zijn slechts beperkte gegevens uit onderzoek beschikbaar.
- Criteria voor arteriitis temporalis, oorspronkelijk bedoeld voor onderzoek, voldoen voor de diagnostiek niet goed (zie Details).
In een retrospectief cohortonderzoek (1994 tot 2003) in drie grote huisartsenpraktijken in Engeland werd gekeken welke symptomen leidden tot de diagnose PMR. Daarnaast werden deze bevindingen vergeleken met bestaande sets van criteria voor de diagnose PMR (Bird, Jones/Hazleman, Hunder en Healey). Tot slot werd bekeken welke bevindingen bij de diagnosestelling van invloed waren op de uitkomst. Patiënten met verschijnselen van arteriitis temporalis werden geëxcludeerd. Er werden 183 patiënten met PMR geïdentificeerd. BSE > 30mm/uur en CRP > 6 mg/l werden gekenschetst als afwijkend. De gemiddelde leeftijd waarop de diagnose werd gesteld was 75 jaar. 75% van de patiënten was vrouw, 11% van de patiënten had een normale BSE en CRP. Bij 91% van de patiënten droeg een succesvolle proefbehandeling met corticosteroïden bij aan de diagnose. De diagnose werd verder ondersteund door verhoogde ontstekingsparameters (90%), spierpijn van het proximale deel van de extremiteit (82%) en normalisatie van de ontstekingsparameters (81%) tijdens behandeling. Bij 19% was ochtendstijfheid vastgelegd. De gemiddelde behandelduur was 1,4 jaar. De gemiddelde startdosering was 15 mg/dag prednisolon. Twee variabelen waren onafhankelijk geassocieerd met een langere behandelduur: vrouwelijk geslacht (OR 1,5) en verhoogde ontstekingsparameters (OR 2,0). 14% van de patiënten werd verwezen naar de tweede lijn. Slechts 25 van de 183 patiënten voldeden geheel aan één van de bestaande sets van criteria. Binnen twee jaar na de diagnose PMR hadden 22 patiënten (12%) een andere diagnose: negen patiënten RA, zeven een maligniteit en zes hypothyreoïdie. RA en hypothyreoïdie werden frequenter aangetroffen dan verwacht in de normale populatie.
In de helft van de gevallen werd de diagnose binnen twee weken na het begin van de klachten gesteld. Hiermee bestaat de kans dat self-limiting ziekten (postvirale klachten) te snel als PMR worden behandeld.
Het vastleggen van ochtendstijfheid kan belangrijk zijn om een onderscheid te kunnen maken tussen inflammatoire pijnklachten (PMR, RA) en niet-inflammatoire pijnklachten (cervicale artrose). Bij 25 patiënten werd een dosering gehanteerd die hoger was dan de gebruikelijke dosis van 20 mg of lager. Dit kan leiden tot maskeren van klachten die bij een alternatieve diagnose zou kunnen passen.
De relatief lage sensitiviteit van de biopsie (60 tot 80%) in combinatie met het risico op blijvend visusverlies heeft geleid tot het opstellen van diagnostische criteria voor arteriitis temporalis door de American College of Rheumatology (ACR): een leeftijd boven de vijftig jaar, recent ontstane nieuwe hoofdpijn, afwijkende bevindingen bij onderzoek van de arteria temporalis (pijn bij aanraken, afgenomen pulsatie, niet gerelateerd aan atherosclerose), een BSE > 50mm/uur en biopsie met kenmerkende afwijkingen.
In een prospectief cohortonderzoek in de tweede lijn werden 198 patiënten onderzocht vanwege vermoeden van vasculitis. De diagnose vasculitis volgens de ACR-criteria werd vergeleken met de uiteindelijke klinische diagnose, die als gouden standaard fungeerde. Vasculitis werd gediagnosticeerd bij 51 patiënten (26%). Bij een prevalentie van 4% was de positief voorspellende waarde van het toepassen van de ACR-criteria voor arteriitis temporalis 29% (95%-BI 19 tot 39).
Conclusie
De ACR-criteria voor arteriitis temporalis zijn in de eerste lijn niet goed bruikbaar vanwege de lage prevalentie van arteriitis temporalis. Daarnaast is er een overlap in klinische presentatie tussen de verschillende vasculitiden.
Anamnese
Naar Samenvatting ›- Vraag bij vermoeden van PMR naar:
- pijn: lokalisatie, eenzijdig of symmetrisch, houdings- of bewegingafhankelijk of continu aanwezig, ernst/invloed van de pijn op het dagelijks leven (overeind komen uit stoel of bed, invloed op de slaap, problemen met wassen en aankleden, invloed op betaalde of onbetaalde activiteiten)
- stijfheid: lokalisatie, tijdstip van de dag, duur, invloed van de stijfheid op het dagelijks leven
- duur van de klachten
- Vraag naar klachten die kunnen wijzen op arteriitis temporalis:
- hoofdpijn: bekende of onbekende hoofdpijn, lokalisatie, enkel- of dubbelzijdig (zie Details)
- pijn bij het kauwen, pijn bij haren kammen
- visusproblemen: gedeeltelijk of totaal gezichtsveldverlies, snel ontstane visusdaling, enkel- of dubbelzijdig, voorbijgaand of permanent, dubbelzien
- Besteed voor andere oorzaken van de klachten dan PMR of arteriitis temporalis aandacht aan:
- aanwezigheid van gezwollen gewrichten of peesscheden (reumatoïde artritis)
- temperatuur (infectie)
- malaise, verlies van eetlust, gewichtsverlies, rugpijn, hoesten (maligniteit, hypothyreoïdie)
- verloop van de klachten in de tijd: wanneer begonnen, waarmee begonnen, voorafgaande klachten, snel ontstaan of geleidelijker (infectie, maligniteit, aspecifieke klachten van het bewegingsapparaat)
- gebruik van statines, spierzwakte (myopathie) (zie Details)
In retrospectief dossieronderzoek bij patiënten met aangetoonde arteriitis temporalis bleek geen eenduidig patroon van hoofdpijn voor te komen. Bij ouderen met hoofdpijn, ongeacht soort, lokalisatie, ernst of patroon moet arteriitis temporalis worden overwogen.
In een review worden diverse aspecten rond myopathie door statines belicht. Het klinisch spectrum van klachten door gebruik van statines is breed: myalgie, myositis, rhabdomyolyse en asymptomatische toename van serum CK. De term myopathie wordt in het algemeen gebruikt om het gehele spectrum van klachten te beschrijven, zoals moeheid, spierpijn, gevoeligheid van de spieren, spierzwakte, nachtelijke krampen en pijn aan de pezen. De spierklachten betreffen meestal de proximale spiergroepen, zijn gegeneraliseerd en verergeren bij inspanning. Wanneer de CK lager blijft dan tien maal de bovengrens van de normaalwaarde spreekt men van myositis. Als de CK meer dan tien maal de bovengrens van de normaalwaarde overschrijdt, spreekt men van rhabdomyolyse. Een licht verhoogde CK komt in de algemene populatie overigens regelmatig voor.
Lichamelijk onderzoek
Naar Samenvatting ›- Het lichamelijk onderzoek richt zich vooral op aanwijzingen voor PMR en arteriitis temporalis. Afhankelijk van de bevindingen bij de anamnese en het lichamelijk onderzoek kan een uitgebreider lichamelijk onderzoek, gericht op andere oorzaken, noodzakelijk zijn.
Besteed beiderzijds aandacht aan:
- actief bewegingsonderzoek van de nek, schouders en heupen: let op pijn, beperkingen en de aanwezigheid van krachtverlies (myopathie)
- perifere artrogene en tendinomyogene afwijkingen: gevoeligheid gewrichtskapsels van de knie, pols, vinger- en handgewrichten, zwellingen ter plaatse van de gewrichten van vinger/hand (reumatoïde artritis), zwelling van de dorsale zijde van hand, pols, voeten en/of enkels, aanwijzingen voor carpaletunnelsyndroom
- gevoeligheid, pijn of zwelling bij palpatie arteria temporalis, aanwezigheid pulsaties arteria temporalis (zie Details)
- Meet de temperatuur.
In een review werd de waarde van anamnese, lichamelijk onderzoek en de BSE bij patiënten met klinisch vermoeden van arteriitis temporalis bekeken. Er werden 21 onderzoeken gevonden, waarvan 17 retrospectief, waarin patiënten met zowel positieve als negatieve temporalisbiopsie werden geïncludeerd.
Anamnese
Van de 2.680 patiënten hadden 1050 patiënten (39%) een positieve temporalisbiopsie. De diagnostische waarde van veertien anamnestische vragen werd onderzocht: anorexie, gewichtsverlies, artralgie, dubbelzien, moeheid, koorts, temporale hoofdpijn, alle hoofdpijnen, pijn bij het kauwen, spierpijn, PMR, eenzijdig visusverlies, alle visuele symptomen, duizeligheid. Alleen pijn bij het kauwen en dubbelzien waren duidelijk geassocieerd met arteriitis temporalis (positieve LR 4,2; 95%-BI 2,8 tot 6,2) respectievelijk 3,4; 95%-BI 1,3 tot 8,6). De sensitiviteit van pijn bij het kauwen bij patiënten met een positieve temporalisbiopsie was slechts 34% (95%-BI 29 tot 41%) en die van dubbelzien 9% (95%-BI 7 tot 13%). Alle overige anamnestische gegevens hadden een lage positieve LR (< 2). De negatieve LR was voor alle vragen niet onderscheidend.
Lichamelijk en aanvullend onderzoek
Bevindingen bij lichamelijk onderzoek hadden grotere invloed op de kans om een positieve temporalisbiopsie te vinden dan de anamnese. De diagnostische waarde van verschillende onderzoeksbevindingen werd onderzocht. Aanwezigheid van synovitis maakte de kans op een positieve temporalisbiopsie minder waarschijnlijk (positieve LR 0,41; 95%-BI 0,23 tot 0,72). Dit gold ook voor de afwezigheid van een afwijking aan de arteria temporalis (negatieve LR 0,53; 95%-BI 0,38 tot 0,75). Alle abnormale bevindingen bij palpatie van de arteria temporalis (kraalvormige structuur van de arteria temporalis, prominente of vergrote arteria temporalis, gevoelige arteria temporalis) maakten de kans op een positieve temporalisbiopsie groter (positieve LR in al deze gevallen > 4). Een normale BSE, hoewel niet altijd duidelijk gedefinieerd, maakte de kans op een positieve temporalisbiopsie klein (negatieve LR 0,2; 95%-BI 0,08 tot 0,51).
Er werd geen onderzoek gevonden waaruit bleek of de pulsaties van arteria temporalis bij gezonden altijd goed voelbaar zijn.
Conclusie
Het lijkt waarschijnlijk dat een aantal bevindingen bijdraagt aan de kans op arteriitis temporalis: anamnestisch pijn bij het kauwen, dubbelzien, en afwijkende bevindingen van de arteria temporalis. De kans op arteriitis temporalis is kleiner bij aanwezigheid van een synovitis of een normale BSE.
Aanvullend onderzoek
Naar Samenvatting ›- Bepaal de BSE en verricht bij een verhoogde BSE verder aanvullend bloedonderzoek (zie Kenmerken van polymyalgia rheumatica).
- Anamnese en lichamelijk onderzoek kunnen een indicatie geven voor verder aanvullend onderzoek (laboratoriumdiagnostiek, echografie of röntgenonderzoek).
- Overweeg het aanvragen van de volgende laboratoriumonderzoeken (zie Details):
- bloedbeeld (infectieziekten, maligniteit)
- TSH (hypothyreoïdie)
- totaal eiwit en eiwitspectrum (multipel myeloom)
- CK (myopathie door statines, poly-/dermatomyositis)
Hoewel de differentiaaldiagnose van PMR uitgebreid is (zie Klachten en symptomen), zal in zijn algemeenheid een gedegen anamnese en lichamelijk onderzoek richting geven aan de noodzaak van aanvullend onderzoek. Uit de literatuur blijken in de praktijk vooral hypothyreoïdie en RA, en ook (hematologische) maligniteiten schuil te gaan achter klachten die aanvankelijk als PMR werden geduid. De werkgroep adviseert daarom in ieder geval een bloedbeeld, TSH, totaal eiwit en een eiwitspectrum als aanvullend laboratoriumonderzoek te doen. Het aanvragen van een anti-CCP test (anti-cyclisch citrulline peptide) of reumafactortest wordt bij vermoeden van RA niet aanbevolen (zie NHG-Standaard Artritis).
Het multipel myeloom (ziekte van Kahler) kan gepaard gaan met een verhoogde BSE en botpijn, waardoor het zich kan presenteren als PMR. Het multipel myeloom is een maligne woekering van plasmacellen die uitgaat van het beenmerg. Bij de klinische presentatie staan botpijn (rug) of fracturen na gering trauma of spontaan op de voorgrond. Voorts kunnen er klachten zijn door anemie. Er is meestal een verhoogde infectieneiging. Bij een hoog M-Proteïnegehalte (paraproteïnegehalte) in het serum kan het hyperviscositeitssyndroom ontstaan met neurologische afwijkingen, diffuse slijmvliesbloedingen, visusstoornissen en hartfalen. Verder kunnen klachten ontstaan door een verhoogd calciumgehalte. De ziekte van Kahler is zeldzaam en wordt per jaar bij ongeveer 6 nieuwe patiënten per 100.000 inwoners in Nederland gezien. De helft van de patiënten is ouder dan 65 jaar; de ziekte komt even vaak bij vrouwen als bij mannen voor.
Evaluatie
Naar Samenvatting ›- Het is zaak om veelvoorkomende aandoeningen die zich op ongeveer dezelfde wijze kunnen presenteren als PMR uit te sluiten voordat de diagnose PMR wordt gesteld:
- (late-onset) reumatoïde artritis: 1 of meer gezwollen gewrichten, in combinatie met pijn, stijfheid, warmte, roodheid of bewegingsbeperking, tangentiële drukpijn van de MCP’s of MTP’s; ochtendstijfheid van 30 minuten of meer, duur van de klachten > 4 weken, ondanks behandeling met een NSAID. Soms is een langere follow-up nodig om de correcte diagnose te stellen (zie Details)
- hypothyreoïdie (TSH)
- Overweeg daarnaast of andere aandoeningen het beeld kunnen verklaren:
- infectieziekten zoals prodromen of restklachten van virusziekten of luchtweginfecties (koorts, afwijkend bloedbeeld, verloop van de klachten)
- maligniteit zoals multipel myeloom (anemie, verhoogd totaal eiwit/afwijkend eiwitspectrum)
- tendinoartrogene nek- en schouder- of heupklachten (meestal unilateraal, actieve bewegingsbeperking door pijn, normaal bloedbeeld)
- myopathie (spierzwakte staat meer op de voorgrond dan pijn, verhoogde CK, statinegebruik)
- aspecifieke klachten van het bewegingsapparaat (meestal leeftijd < 50 jaar, pijn niet beperkt tot de nek/schouder of heupregio, BSE normaal)
- Kunnen de klachten redelijkerwijs niet worden verklaard door een andere oorzaak, stel dan de diagnose PMR bij patiënten > 50 jaar en:
- duur van klachten > 4 weken, gerekend vanaf het moment van de 1e klachten (zie Kenmerken van polymyalgia rheumatica), én
- bilaterale pijn in de nek en schouderregio en/of heup/bekkenregio (door de pijn veroorzaakte actieve bewegingsbeperking van de schouders en/of beperkingen van actieve bewegingen van de heupen; vaak ’s nachts veel last en moeite met aankleden en overeind komen), én
- ochtendstijfheid > 60 min, én
- BSE > 40 mm/uur
- Zorg voor een goede verslaglegging van het klinisch beeld om de verbetering door medicatie te kunnen bepalen.
- Gebruik verbetering door orale glucocorticoïden niet als diagnostische test voor PMR. Ziektebeelden met dezelfde verschijnselen als PMR (bijvoorbeeld reumatoïde artritis) kunnen ook gunstig reageren op behandeling met glucocorticoïden.
- Atypische manifestaties van PMR komen voor, zoals asymmetrie van de klachten of het ontbreken van een verhoogde BSE (zie Details).
In een prospectief cohortonderzoek in de tweede lijn werden 116 opeenvolgende patiënten met bilaterale pijnklachten gedurende langer dan een maand en een verhoogde BSE gedurende twaalf maanden gevolgd; 19% van de patiënten bleek bij het eerste onderzoek RA te hebben en 81% PMR. Gedurende de follow-up ontwikkelden nog eens negentien patiënten RA. Aan het eind van het onderzoek werd bij 56% van de patiënten uiteindelijk de diagnose PMR bevestigd. BSE, reumafactoren, Hb, bloedbeeld, CD8-lymfocyten, ALAT, ASAT, AF en gGT noch het klinisch beeld konden in een vroeg stadium RA met PMR-achtige klachten onderscheiden van PMR. Alleen de aanwezigheid van perifere synovitis kon daarbij helpen, maar de positief voorspellende waarde hiervan was laag.
Atypische manifestaties van PMR komen voor: distale tendinomyogene klachten, zoals carpaletunnelsyndroom als enige symptoom van PMR of pijn aan het distale deel van arm of been, normale bezinking, spierzwakte, asymmetrische pijn en een leeftijd < 50 jaar. Uit een literatuurreview betreffende de associatie van carcinomen met reumatische syndromen bleek dat bij een atypische presentatie een grotere kans bestaat op een onderliggend carcinoom. Op basis van patiëntenseries en gevalsbeschrijvingen wordt verondersteld dat klachten en symptomen passend bij PMR op een leeftijd < 65 jaar de kans op een alternatieve diagnose groter maken.
Conclusie
Atypische manifestaties van PMR, zoals een niet-verhoogde BSE (zie Kenmerken van polymyalgia rheumatica), asymmetrische klachten en een leeftijd onder vijftig jaar, komen incidenteel voor. Bij deze atypische manifestaties bestaan de nodige valkuilen. Een grotere kans op een alternatieve diagnose lijkt aanwezig. Bij PMR met een normale BSE bestaat enerzijds het risico op overbehandeling van PMR als PMR niet de juiste diagnose blijkt, maar lopen patiënten anderzijds soms ook het risico op onnodig lang uitstel van behandeling als de diagnose PMR wel terecht blijkt.
Richtlijnen beleid
Naar Samenvatting ›Voorlichting en advies
Naar Samenvatting ›- Leg uit dat:
- PMR een aandoening is waarbij de nek en schouderregio en/of heup/bekkenregio stijf en pijnlijk zijn, vooral in de ochtend. De oorzaak is onbekend.
- bij de behandeling van PMR meestal glucocorticoïden noodzakelijk zijn. Doorgaans treedt daarmee snel verbetering op en geneest de ziekte uiteindelijk zonder restschade. Om te voorkomen dat de klachten van PMR terugkomen, moet de behandeling met glucocorticoïden in het algemeen 1 tot 2 jaar worden voortgezet. Regelmatige controle is noodzakelijk ter evaluatie van het effect van de medicatie op de klachten. Glucocorticoïden mogen niet ineens gestaakt worden.
- PMR gepaard kan gaan met arteriitis temporalis. Hierbij komt hoofdpijn voor, die anders wordt ervaren dan gewone hoofdpijn. Soms treedt deze hoofdpijn op bij kauwen en kunnen problemen met het gezichtsvermogen optreden, zoals snel ontstane visusdaling, dubbelzien of blindheid. Snelle behandeling met glucocorticoïden kan dan verdere schade voorkómen of de schade beperkt houden.
- Instrueer de patiënt direct contact op te nemen:
- bij koorts (door het gebruik van glucocorticoïden kunnen immunosuppressie, bijnierschorsinsufficiëntie en een verstoring van het klinisch beeld optreden)
- bij niet-bekende hoofdpijn
- bij acute visusdaling, (eenzijdig, soms kortdurend) visusverlies of dubbelzien
Thuisarts
Naar Samenvatting ›Verwijs naar de informatie over polymyalgia rheumatica en arteriitis temporalis op thuisarts.nl, die is gebaseerd op deze NHG-Standaard.
Niet-medicamenteuze behandeling
Naar Samenvatting ›De werkzaamheid van fysiotherapie bij PMR is niet onderzocht (zie Details).
Er is geen onderzoek gevonden naar de werkzaamheid van fysiotherapie bij de behandeling van PMR. De werkgroep ziet geen meerwaarde in de behandeling van PMR met fysiotherapie.
Medicamenteuze behandeling
Naar Samenvatting ›Polymyalgia rheumatica
Naar Samenvatting ›1e 3 maanden
Naar Samenvatting ›Behandel patiënten met PMR met orale glucocorticoïden (zie Details). Het doel van de behandeling is: afwezigheid van klachten. Het volgende behandelschema voor de 1e 3 maanden bevelen we aan (zie tabel 1) (zie Details).
- Start met prednis(ol)on, 1 dd 15 mg gedurende 1 maand. Na 1 maand dienen de pijn en stijfheid verdwenen te zijn en dient de bezinking gedaald te zijn tot < 40 mm/uur. Ook bij eerdere verbetering wordt de aanvangsdosering gecontinueerd tot minimaal 2 weken na het verdwijnen van de klachten.
- Verminder de dagdosering vervolgens elke 4 weken met 2,5 mg tot een dagdosering van 10 mg is bereikt.
| Moment vanaf start behandeling | Dosering prednis(ol)on |
|---|---|
| Week 0-4 | 15 mg per dag |
| Week 4-8 | 12,5 mg per dag |
| Week 8-12 | 10 mg per dag |
| Vanaf week 12 | Op geleide van de klachten zeer geleidelijke vermindering van de dosering. Zie Voorbeeldschema afbouw prednis(ol)on na 3 maanden. |
| Terugval | Bij het terugkeren van de klachten en symptomen of bij het oplopen van de BSE, zonder een verklaarbare andere oorzaak: verhoog de dagdosering naar het niveau waarop de klachten afwezig of acceptabel waren. Probeer na 4 weken de dosering opnieuw te verlagen. |
| Voor een houvast, zie Voorbeeldschema afbouw prednis(ol)on na 3 maanden. | |
Behandeling met glucocorticoïden is werkzaam bij de behandeling van PMR en arteriitis temporalis. Klinische ervaring en observationele onderzoeken hebben dit aangetoond. In de criteria van Jones en Hazleman en die van Healey is verbetering door glucocorticoïden een van de criteria voor de diagnose. Beide criteria hanteren een startdosis van ≤ 20 mg prednisolon.
Gecontroleerd onderzoek dat prednison of prednisolon met placebo vergelijkt werd niet gevonden. Bij orale toediening met glucocorticoïden heeft geen van deze beschikbare middelen de voorkeur. Prednison zelf is onwerkzaam en wordt in de lever omgezet in de werkzame stof prednisolon.
Uit ervaring lijkt een beperkte groep patiënten waarschijnlijk baat te hebben bij behandeling met een NSAID. Onderzoek naar de behandeling van PMR met NSAID’s werd evenwel niet gevonden.
Conclusie
Er is geen gecontroleerd onderzoek naar de medicamenteuze behandeling van PMR gevonden. Uit klinische ervaring en observationele onderzoeken blijkt dat glucocorticoïden bij PMR werkzaam zijn. Slechts bij een beperkt aantal patiënten kan met een NSAID worden volstaan; het is evenwel niet duidelijk welke patiënten hierbij baat kunnen hebben.
Er bestaan diverse schema’s voor de afbouw van predniso(lo)n die berusten op klinische ervaring en consensus. Een algemeen geaccepteerd behandelingsschema is er niet.
Voor het behandelingsschema baseert de werkgroep zich op een veelgebruikt schema, waarbij de volgende overwegingen een rol hebben gespeeld:
- het bereiken van symptoomverlichting met de laagst mogelijke dosering predniso(lo)n;
- een hoge startdosering en een snelle dosisvermindering leiden tot een grotere kans op terugval;
- hoge startdoseringen (> 20 mg/dag) geven grotere kans op maskering van andere ziektebeelden die zich op dezelfde wijze presenteren als PMR;
- afbouwen van glucocorticoïden moet geleidelijk gebeuren in verband met de kleine kans op een cortisoldeficiëntie ten gevolge van chronische suppressie van de hypothalame-hypofysaire-adrenale as;
- gezien de beperkte ervaring van huisartsen met PMR adviseert de werkgroep een vast doseringsschema gedurende de eerste drie maanden van de behandeling. Omdat na de eerste drie maanden het beloop wisselend is, worden voor de periode daarna randvoorwaarden genoemd, waaronder de afbouw adequaat kan geschieden.
Na 1e 3 maanden
Naar Samenvatting ›- Voor de vermindering van de dosering ná de 1e 3 maanden van behandeling zijn geen goede richtlijnen te geven, omdat het beloop kan verschillen. Baseer de vermindering van de dosering op de volgende overwegingen.
- Een zeer geleidelijke vermindering van de dagdosering geeft de minste kans op terugval.
- De fase waarbij de medicatie in nog zeer lage dosering wordt gegeven tot het moment van stoppen, kan langdurig zijn. Veel patiënten ervaren in die periode een terugval.
- Verhoog bij het terugkeren van de klachten of bij het oplopen van de BSE, zonder verklaarbare andere oorzaak, de dagdosering naar het niveau waarop de klachten afwezig of acceptabel waren. Probeer na 4 weken de dosering opnieuw te verlagen.
- De duur van de behandeling kan variëren van 1 tot 2 jaar. Een kleine groep patiënten heeft gedurende een langere periode een lage dosering nodig.
- Voor een houvast, zie Voorbeeldschema afbouw prednis(ol)on na 3 maanden.
Aandachtspunten bij behandeling met glucocorticoïden
Naar Samenvatting ›- Bij PMR treedt vaak een aanzienlijke verbetering op door behandeling met glucocorticoïden. Omdat een dergelijke verbetering ook kan optreden bij andere ziektebeelden met een vergelijkbare presentatie, blijft gedurende de behandeling waakzaamheid nodig.
- Glucocorticoïden zijn immunosuppressief. Wees daarom alert op aanwijzingen voor infecties of reactivering van latent aanwezige infecties zoals tuberculose TBC (zie Details). Instrueer de patiënt bij koorts (> 38,0 °C) contact op te nemen.
- Langdurig gebruik van glucocorticoïden kan suppressie van de bijnierschorsactiviteit geven (zie Details).
- Osteoporose. Geef bij de behandeling met glucocorticoïden bisfosfonaten volgens de richtlijnen in NHG-Standaard Fractuurpreventie. Staak de bisfosfonaten bij het beëindigen van de behandeling met glucocorticoïden. Overweeg, eveneens conform deze standaard, een aanvullende preventieve behandeling met calcium en vitamine D.
- Gastro-intestinale ulceraties. Wanneer alleen glucocorticoïden worden gebruikt, is er geen maagbescherming aangewezen. Bij een ulcus pepticum in de anamnese of bij aanwezigheid van een andere risicofactor (zoals het gebruik van NSAID’s, SSRI’s, salicylaten of anticoagulantia) is maagbescherming geïndiceerd (zie NHG-Standaard Maagklachten) (zie Details).
Een derde deel van de wereldbevolking heeft latente TBC. Een verhoogd risico op latente tuberculose bestaat bij personen met een nauw contact met besmette gevallen en reizen, verblijf of geboorte in gebieden waar TBC veel voorkomt. Verhoogde kans op reactivering van een latente tuberculose bestaat bij verminderde werking van het immuunsysteem door HIV, door jonge of hoge leeftijd, bij chronische ziekten of een slechte voedingstoestand zoals bij daklozen, drugsgebruik of alcoholisme, en bij gebruik van immunosuppressieve middelen.
Typische klachten van pulmonaire tuberculose zijn chronische hoest, gewichtsverlies, intermitterende koorts, nachtzweten en bloed ophoesten. Niet-pulmonale tuberculose manifesteert zich afhankelijk van de plek van voorkomen en kan gepaard gaan met gewichtsverlies en intermitterende koorts.
In een casecontroleonderzoek werden cases met TBC geïdentificeerd uit een eerstelijns database (2,7 miljoen patiënten) in Groot-Brittannië gedurende de periode 1990 tot 2001. Iedere case werd gematched met vier controles. Cases en controles met HIV of een hematologische maligniteit werden geëxcludeerd. Er werden 497 nieuwe gevallen van TBC geïdentificeerd. Gebruik van corticosteroïden voorafgaand aan de TBC werd onderscheiden in huidig gebruik (0 tot 120 dagen), recent gebruik (121 tot 180 dagen) en gebruik in het verleden (> 180 dagen geleden). De incidentie in de onderzoekpopulaties was 4,4 per 100.000 en was daarmee gelijk aan de incidentie van de Britse populatie zonder migratieachtergrond. Bij de cases en controles samen zaten onder andere twaalf patiënten met PMR. De OR voor het risico op TBC was bij huidig gebruik van een corticosteroïd 4,9 (95%-BI 2,9 tot 8,3), voor recent gebruik 4,3 (95%-BI 1,6 tot 11,1) en bij gebruik in het verleden 1,4 (95%-BI 0,9 tot 2,1). Er was een dosisresponsgradiënt: bij huidig gebruik was het verband groter bij een dagdosis > 7,5 mg (OR 7,0; 95%-BI 2,9 tot 16,8) dan bij een dosis < 7,5 mg (OR 2,3; 95%-BI 0,7 tot 7,5). Beperking van het onderzoek is het geringe aantal patiënten met PMR.
Conclusie
Patiënten die behandeld worden met corticosteroïden hebben een verhoogde kans om TBC te ontwikkelen onafhankelijk van het bestaan van andere risicofactoren. Kwantificering van dit risico hangt daarnaast samen met de prevalentie van TBC, omgevingsfactoren en risicofactoren van de patiënt.
Langdurig gebruik van glucocorticoïden kan leiden tot een verminderde functie van de bijnierschors. Dit wordt ook wel een tertiaire bijnierschorsinsufficiëntie genoemd.
In stresssituaties zoals een (koortsende) ziekte, ongeval of operatie, of ernstige psychische stress, waarbij aanmaak van meer bijnierschorshormoon cortisol dan normaal nodig is, kunnen de al falende bijnieren geen gehoor geven aan deze verhoogde behoefte en kan een acute bijnierschorsinsufficiëntie ontstaan. Ook het abrupt staken van glucocorticoïden, wanneer dit langer dan drie weken werd gebruikt, kan leiden tot een (acute) bijnierschorsinsufficiëntie. Een geleidelijke vermindering van de dosering geeft de bijnier de tijd om naar een normaal patroon van hormoonsecretie terug te keren. Vermindering van de dosering van glucocorticoïden kan echter ook met onthoudingsverschijnselen gepaard gaan, waarbij er klachten optreden gelijkend op die van bijnierschorsinsufficiëntie terwijl de cortisolspiegels acceptabel zijn. Dit kan behandeld worden met een tijdelijke verhoging van de dosering glucocorticoïden.
De meeste klinische verschijnselen van bijnierschorsinsufficiëntie zijn aspecifiek. Ze ontstaan vaak geleidelijk in de loop der maanden, soms kunnen ze echter snel ontstaan. Frequente verschijnselen van bijnierschorsinsufficiëntie zijn (ernstige) moeheid en (spier)zwakte, anorexia, gewichtsverlies, misselijkheid, braken, buikpijn, diarree, duizeligheid, (orthostatische) hypotensie, het optreden van spontane hypoglykemieën en psychische symptomen (onder andere depressie). Soms kan een levensbedreigende situatie ontstaan met hypotensie en shock (een hypocortisolistische crise). Het is niet bekend hoe lang en welke dosering glucocorticoïden gebruikt moet zijn om de kans op een acute bijnierinsufficiëntie te vergroten. De duur en de ernst van de suppressie van de hypofyse-bijnieras ten gevolge van gebruik van (farmacologische doseringen) glucocorticoïden zijn individueel zeer variabel. Als praktische richtlijn wordt vaak aangehouden dat wanneer langer dan drie weken farmacologische doseringen glucocorticoïden (> 7,5 mg prednis(ol)on per dag) gegeven zijn, een klinisch relevante suppressie van de hypofyse-bijnieras mogelijk is. Dit kan aanhouden tot een jaar na beëindiging van de glucocorticoïdtoediening.
In de literatuur bestaat geen eenduidigheid over de mate van dosisaanpassing bij ziekte. Klachten passend bij bijnierschorsinsufficiëntie kunnen in het algemeen worden voorkómen door bij (koortsende) ziekte de glucocorticoïddosering te verdubbelen (gedurende de hele periode van koorts). Niet duidelijk is of dit in de eerste lijn in alle gevallen van ziekte daadwerkelijk noodzakelijk is. Onderzoek naar de mate waarin dit probleem zich in de eerste lijn voordoet werd niet gevonden.
In een meta-analyse (n = 6.602) werd onderzocht of behandeling met glucocorticoïden, ongeacht de duur of dosering, in vergelijking met placebo een verhoogde kans gaf op complicaties zoals een peptisch ulcus, dermatologische effecten (onder andere acne, hirsutisme, Cushing uiterlijk), sepsis, diabetes, hypertensie, osteoporose en tuberculose en delier. Dermatologische effecten (OR 4,5; 95%-BI 3,5 tot 5,7), diabetes (OR 1,7; 95%-BI 1,1 tot 2,6) en hypertensie (OR 2,2; 95%-BI 1,4 tot 3,8) werden statistisch significant vaker aangetroffen in de behandelgroep met glucocorticoïden dan in de placebogroep. Een peptisch ulcus (OR 1,2; 95%-BI 0,8 tot 2,0), sepsis, osteoporose (OR 1,7; 95%-BI 0,7 tot 4,1), psychose (delier) en tuberculose kwamen vaker voor in de corticosteroïdgroep, maar de verschillen met de placebogroep waren statistisch niet significant. Geconcludeerd werd dat een ulcus geen contra-indicatie is voor een behandeling met corticosteroïden. In het HARM-onderzoek, een prospectieve multicenterstudie, werd de frequentie van geneesmiddelgerelateerde ziekenhuisopnames in Nederland onderzocht. Patiënten ouder dan 65 jaar hadden een tweemaal zo hoge frequentie van geneesmiddelgerelateerde opnames ten opzichte van patiënten jonger dan 65 jaar. Gastro-intestinale bloedingen, cardiovasculaire problemen, respiratoire aandoeningen, andere gastro-intestinale klachten en ontregelde diabetes mellitus waren de meest gevonden oorzaak van geneesmiddelgerelateerde opnames. De geneesmiddelen die de meeste problemen veroorzaakten waren trombocytenaggregatieremmers, coumarines, NSAID’s, psycholeptica, antidiabetica en glucocorticoïden. Therapieontrouw, verminderde cognitie, verminderde nierfunctie, het niet- zelfstandig wonen, meerdere aandoeningen in de medische voorgeschiedenis en polyfarmacie zijn geïdentificeerd als de belangrijkste onafhankelijke risicofactoren.
Conclusie
Dermatologische effecten, diabetes en hypertensie komen vaker voor bij behandeling met glucocorticoïden.
Arteriitis temporalis
Naar Samenvatting ›- Bij de behandeling van ongecompliceerde arteriitis temporalis volstaat een dosering van 40 tot 60 mg prednis(ol)on per dag. Hiermee treedt snelle verbetering van het klinisch beeld op.
- Geef hogere doseringen bij oogheelkundige complicaties (1 mg prednis(ol)on per kg lichaamgewicht).
- Voeg bij dreigende ischemische complicaties desgewenst een trombocytenaggregatieremmer aan de behandeling toe.
- De behandelingsduur is 1 tot 2 jaar. Tot op heden bestaan er geen nauwkeurige voorspellers voor de duur van de behandeling.
Controles
Naar Samenvatting ›- Controleer de patiënt regelmatig en gedurende lange tijd na het stellen van de diagnose PMR. Gebruik de aanwezigheid en de ernst van de klachten en de bezinking (BSE) om het ziekteproces te vervolgen (zie Details). Heroverweeg de diagnose:
- als het klachtenpatroon en/of de BSE niet naar verwachting afnemen
- bij toename van de klachten of bij stijging van de BSE ondanks behandeling
- Het is raadzaam de klachten en bevindingen goed vast te leggen om het beloop te kunnen volgen.
- Hanteer het volgende controleschema na de start van de behandeling:
- 1 week en 4 weken na de start van de behandeling – na 1 week mag al verbetering verwacht worden (zie Kenmerken van polymyalga rheumatica)
- 1 tot 4 weken na elke dosisverandering
- Beoordeel bij de controles de situatie ten opzichte van de vorige controle en bepaal of er verbetering, geen verandering of verslechtering is opgetreden. Hierbij komen aan de orde (zie Details):
- pijn en stijfheid in de nek en schouderregio en/of heupregio (vraag naar: overeind komen uit stoel of bed, invloed op de slaap, problemen met wassen en aankleden; onderzoek of de patiënt actief de armen of benen kan heffen)
- globale indruk door de huisarts; eventueel kan de patiënt met een score op de visueel analoge schaal (VAS) het beloop van de ziekte inzichtelijk maken
- ochtendstijfheid (in minuten)
- nieuwe klachten of symptomen, passend bij een alternatieve diagnose. Let vooral op klachten die bij arteriitis temporalis passen, zoals hoofdpijn, visusklachten en pijn bij kauwen, omdat arteriitis temporalis zich tijdens het beloop van PMR kan ontwikkelen. Instrueer de patiënt bij deze klachten direct contact op te nemen
- medicatie: bijwerkingen, zoals het optreden van maagklachten of problemen met het innameschema
- Bepaal:
- de BSE 4 weken na de start van de behandeling. Controleer daarna de BSE 1 tot 4 weken na elke dosisverandering. De BSE daalt onder invloed van prednis(ol)on naar een normale waarde. Voor een eventuele individuele referentiewaarde van de BSE kan een eerder bepaalde BSE behulpzaam zijn. Heroverweeg de diagnose of stel het afbouwschema bij als de (meermalen gemeten) BSE oploopt.
- de nuchtere glucose voorafgaand aan de start van de behandeling met prednis(ol)on en 3 tot 7 dagen daarna. Bepaal bij het ontstaan van hyperglykemie frequent de glucosespiegel en start behandeling en controles conform NHG-Standaard Diabetes mellitus type 2. Pas zo nodig de diabetesmedicatie aan bij de geleidelijke dosisvermindering van prednis(ol)on. Geef voorlichting over verschijnselen die passen bij hyperglykemie en wat patiënten dan kunnen doen. Vergelijkbare aanbevelingen gelden voor patiënten met bekende diabetes mellitus.
- In het begin van de behandeling is regelmatige controle van de bloeddruk gewenst.
- Tussentijdse overwegingen:
- Bij een deel van de patiënten zal gedurende de behandeling een terugval optreden. Hiervan is sprake wanneer de klachten een verhoging van de glucocorticoïddosering noodzakelijk maken (zie Details).
- Overweeg een alternatieve diagnose bij het uitblijven van verbetering op glucocorticoïden na de 1e weken van de behandeling en ook bij het ontstaan van verschijnselen gedurende de behandeling die niet passen bij PMR of arteriitis temporalis.
- Veel patiënten vertonen weliswaar een goede verbetering door behandeling, maar worden niet compleet klachtenvrij.
- Verhoog bij het terugkeren van de klachten en symptomen of bij het oplopen van de BSE, zonder aantoonbare andere oorzaak, de glucocorticoïddosering naar het laagste niveau waarbij de klachten nog afwezig waren. Probeer hierna bij verbetering van de klachten na 4 weken de dosering opnieuw te verlagen.
Voor het monitoren van PMR gebruikt men in het algemeen de klinische symptomen gecombineerd met de BSE en/of CRP. Bij de meeste patiënten is de BSE een goede maat voor de activiteit van de ziekte. De BSE kan echter normaal zijn bij ziekteactiviteit en afwijkend bij afwezigheid daarvan. De klachten en symptomen van patiënten zijn doorgaans een meer betrouwbare maat voor de ziekteactiviteit dan laboratoriumonderzoek.
Leeb en Bird hebben een scoresysteem ontwikkeld om de activiteit van PMR vast te kunnen stellen. Hiermee zou de corticosteroïddosering bij het afbouwen beter kunnen worden afgestemd op de behoefte van de patiënt. Dit scoresysteem bestaat uit vijf variabelen: ochtendstijfheid (in minuten), vermogen om arm te heffen (op een schaal 0 tot 3), globale inschatting van de ernst van de ziekte (visueel analoge schaal 0 tot 10), CRP en pijn (visueel analoge schaal 0 tot 10). In een vignettenonderzoek in de eerste lijn bleek dat het met dit scoresysteem niet goed mogelijk is om in te schatten of een patiënt met een lagere dosering zou kunnen volstaan.
In een prospectief observationeel onderzoek (n = 129) in de tweede lijn in Engeland werden patiënten met PMR (spierpijn schouder- en/of heupgordel, in afwezigheid van spierzwakte, ochtendstijf > 30 minuten, BSE > 30 mm/uur, afwezigheid van ziekte met eenzelfde presentatie) gevolgd. Uitkomstmaten waren: verbetering door corticosteroïden (startdosering 15 mg/dag) na drie weken, terugval, meting van de QoL middels de SF-36 (minimaal klinisch relevant verschil is vijf punten), de Health Assessment Questionnaire, en overeenstemming onder reumatologen over een eventuele herziening van de diagnose na één jaar. Complete respons was als volgt gedefinieerd: geen klachten of ten minste 50% reductie in pijn in schouder- en heupgordel op een VAS, ochtendstijfheid < 30min, BSE < 30 mm/uur en CRP < 10 mg/dl. De gemiddelde leeftijd was 70,9 jaar (52 tot 92 jaar), 60% was vrouw, 97,7% was Brits zonder migratieachtergrond. De gemiddelde duur van de klachten vóór presentatie was drie maanden. Een derde had perifere symptomen (hand/polspijn, oedeem of gewrichtsklachten). Na drie weken had ongeveer een derde nog een verhoogde BSE, 29% ochtendstijfheid > 30 min en een kwart proximale pijnklachten. Ruim de helft (55%) had geen complete respons in drie weken. 60% van de terugval trad op binnen twee weken na reductie van de dosis. Zowel de fysieke als mentale component van de SF-36 was met 12,6 (95%-BI 10,8 tot 14,4) respectievelijk 11,2 (95%-BI 8,5 tot 13,8) punten verbeterd na één jaar. Proximale pijn en ochtendstijfheid waren significant geassocieerd met een lagere fysieke kwaliteit van leven. Bijwerkingen van de behandeling waren: fracturen (5%), vollemaansgezicht (29%), enkeloedeem (21%), slechte glucoseregulatie (12%), bloeduitstortingen (20%), dyspepsie (39%), hypertensie (25%), kortademigheid (23%), gewichtstoename (> 5% toename gewicht in twaalf maanden) (44%).
Prednis(ol)on kan, vanwege zijn enigszins aldosteronachtige werking, resulteren in een daling van de kaliumconcentratie, meestal nog binnen het normale gebied, soms leidend tot een hypokaliëmie. De kans hierop is met name verhoogd als een diureticum wordt gebruikt.
Er is geen goed onderzoek gevonden naar verschillen in beloop tussen mannen en vrouwen bij behandeling en naar het verschil tussen mannen en vrouwen in het voorkomen van bijwerkingen.
Conclusie
De complete verbetering door glucocorticoïden kan soms enkele weken duren. Bij de follow-up is vooral de afname van de proximale pijn en ochtendstijfheid belangrijk, omdat patiënten deze als zeer hinderlijk ervaren. Langdurig gebruik van glucocorticoïden kan, zoals bekend, ernstige bijwerkingen hebben.
In een prospectief observationeel onderzoek (n = 74, follow-up zestig weken) werd het klinisch beloop van PMR (n = 39) (criteria volgens Jones en Hazleman) en arteriitis temporalis (n = 18) of een combinatie van beide (n = 17) gedurende de eerste twee maanden na het stellen van de diagnose en tijdens de behandeling onderzocht. Drie patiënten vielen uit, van wie één persoon door overlijden aan de gevolgen van arteriitis temporalis. Een terugval bij PMR werd gedefinieerd als klachten die een verhoging van de corticosteroïddosering noodzakelijk maakten, waarbij minstens pijn en stijfheid in de schouder- of heupgordel aanwezig waren. Een terugval werd bij arteriitis temporalis gedefinieerd als hoofdpijn met gevoeligheid van de arteria temporalis of aanwezigheid van visuele klachten. Patiënten met arteriitis temporalis kregen gedurende vijf dagen 40 mg prednisolon en werden daarna gerandomiseerd in een groep met een hoge dosis (vier weken 40 mg, twee weken 30 mg, twee weken 20 mg) en een groep met een lage dosis (vier weken 20 mg, twee weken 15 mg, twee weken 10 mg). Patiënten met PMR werden at random ingedeeld in een groep met hoge dosis regime (prednisolon vier weken 20 mg, twee weken 15 mg, twee weken 10 mg) of een groep met een lage dosis (vier weken 10 mg, twee weken 7,5 mg, twee weken 5 mg). De glucocorticoïden werden afgebouwd met 2,5 mg/maand in twee tot vier maanden, daarna met ongeveer 1 mg/maand in vier tot twaalf maanden en daarna met 1 mg iedere twee tot drie maanden. Zes patiënten met PMR ontwikkelden gedurende de eerste twee maanden van behandeling arteriitis temporalis en twee patiënten in de periode daarna. Vier patiënten met arteriitis temporalis ontwikkelden PMR 15 tot 75 weken na de start van de behandeling. In de eerste twee maanden van behandeling werd 77 keer een terugval door de arts geobserveerd, 24 keer bij PMR, acht keer bij arteriitis temporalis en elf keer bij patiënten met PMR/arteriitis temporalis. Er werd 41 keer een terugval gemeld door de patiënt. In slechts 27% van de gevallen werd geen terugval gezien of gemeld na twee maanden behandeling. Driekwart van de patiënten hadden één tot twee maal een terugval.
In een ander observationeel prospectief onderzoek bij 94 opeenvolgende patiënten met PMR in een tweedelijns setting werd het optreden van terugval gedurende 39 maanden bekeken wanneer patiënten werden behandeld met corticosteroïden. Klinische symptomen, BSE en CRP werden gemeten. De BSE was verhoogd bij 91,5% van de patiënten voor de start van de therapie; de CRP was verhoogd bij 98,9%. De helft van de patiënten had ten minste één terugval en een kwart ten minste twee terugvalperiodes. Na vier weken therapie was bij 13% van de patiënten de BSE nog verhoogd en de CRP bij 41%. In het eerste jaar van de follow-up bleef bij 9% van de patiënten de CRP verhoogd, terwijl geen enkele patiënt een verhoogde BSE had. Een persisterend verhoogde CRP gaf een verhoogd risico op een terugval.
Hogere startdosering en snelle dosisvermindering werd ook in een ander cohortonderzoek aangemerkt als risicofactor voor terugval.
Het beloop en de duur van de behandeling van PMR werd in vier huisartsenpraktijken in Nederland retrospectief onderzocht in de periode 1985 tot 1997. PMR werd bij 49 patiënten vastgesteld (40 vrouwen, 9 mannen). Patiënten werden gemiddeld 2,2 jaar (3 tot 89 maanden) met prednison behandeld; de initiële dosis bedroeg gemiddeld 20,5 mg. Bij 42 patiënten stelde de huisarts zelf de diagnose en startte de therapie. In twee gevallen kon worden volstaan met een NSAID. Een terugval deed zich bij 33 patiënten voor, waarbij het gemiddeld vier maanden duurde voor de eerste exacerbatie optrad. Bij zeven vrouwen en één man traden recidieven op. Gemiddeld waren deze patiënten 9,5 maanden gestopt met medicatie.
Conclusie
Een tijdelijk terugval bij de behandeling met glucocorticoïden komt bij ten minste de helft van de patiënten ten minste eenmaal voor. Een persisterend verhoogde CRP en snelle afbouw bij een hoge startdosering verhogen de kans op terugval.
Verwijzing of consultatie
Naar Samenvatting ›- Verwijs:
- bij vermoeden van arteriitis temporalis naar een reumatoloog/internist voor beoordeling binnen 24 uur na presentatie. De reden hiervoor is dat oogheelkundige complicaties zich snel kunnen ontwikkelen en bijna altijd irreversibel zijn. Huisartsen hebben daarnaast relatief weinig ervaring met het stellen van de diagnose op het klinisch beeld
- bij een acute visusdaling, (geheel of gedeeltelijk) gezichtsveldverlies of dubbelzien met spoed naar de oogarts
- bij ernstige bijwerkingen van of contra-indicaties voor langdurig gebruik van glucocorticoïden naar de reumatoloog/internist voor een eventuele behandeling met methotrexaat (zie Details en Aandachtspunten bij behandeling met glucocorticoïden en Controles)
- Verwijs naar of consulteer een reumatoloog/internist:
- bij uitblijven van klinische verbetering na 1 week behandeling of afwezigheid van duidelijke klinische én biochemische verbetering binnen 4 weken na start van de behandeling
- bij regelmatige terugval (> 2 keer per jaar)
- als het niet mogelijk is de glucocorticoïddosering te verminderen
- bij twijfel aan de diagnose
Behandeling met glucocorticoïden kan gepaard gaan met ernstige bijwerkingen. Soms zijn er contra-indicaties voor het langdurig gebruik van glucocorticoïden, zoals ernstige osteoporose.
Van der Veen et al. onderzochten in een dubbelblind placebogecontroleerd onderzoek (n = 40; van wie zes verschijnselen van arteriitis temporalis hadden) of toevoeging van methotrexaat (MTX) 7,5 mg/week aan prednison (startdosering 20 mg/dag) een steroïdsparend effect had bij de behandeling van PMR. De uitval was hoog (19/40) Na twee jaar follow-up bleek MTX geen steroïdsparend effect te hebben.
In een gerandomiseerde prospectief onderzoek werden patiënten (n = 42) gedurende één jaar gevolgd. Patiënten kregen óf MTX wekelijks in combinatie met prednison óf monotherapie met prednison. Na zes maanden werd getracht de prednison af te bouwen. Na twaalf maanden waren alle patiënten in remissie. Patiënten die behandeld waren volgens het MTX-regime hadden minder prednison nodig om in remissie te blijven. Daarnaast was de botdichtheid in de prednison-arm significant verlaagd.
In een dubbelblind placebogecontroleerd onderzoek bij 72 patiënten met PMR werd de effectiviteit en veiligheid van toevoeging van methotrexaat aan een behandeling met glucocorticoïden bekeken. Daaruit bleek dat bij een initiële behandeling met prednison 25 mg/dag plus methotrexaat 10 mg/week meer patiënten na 76 weken geen prednison meer gebruikten dan in de groep met prednison 25 mg/dag plus placebo (87% versus 53% patiënten). Een terugval of een recidief van de klachten na staken was lager in de methotrexaatgroep dan in de placebogroep (27 episodes versus 50 episodes). Het aantal patiënten dat bijwerkingen ontwikkelde was in beide groepen gelijk, het type bijwerking was verschillend. In de methotrexaatgroep kwamen meer gastro-intestinale bijwerkingen voor. Eén patiënt in de methotrexaatgroep ontwikkelde melaena. Er was geen verschil in corticosteroïdgerelateerde bijwerkingen in beide groepen.
In 2009 werd door een internationaal breed panel van reumatologen aanbevelingen gedaan voor gebruik van methotrexaat bij reumatische aandoeningen, met name bij reumatoïde artritis. Methotrexaat werd als steroïdsparend medicament bij PMR en arteriitis temporalis aanbevolen.
Overwegingen: gezien de potentieel ernstige bijwerkingen van methotrexaat en de intensievere follow-up is er een beperkte plaats voor dit middel, te meer omdat PMR voorkomt op een leeftijd waarop comorbiditeit vaak voorkomt. Bij ernstige bijwerkingen of contra-indicaties voor langdurig gebruik van glucocorticoïden is MTX te overwegen. Het gebruik van MTX is een veilig middel in de handen van artsen die hier ervaring mee hebben en de geldende richtlijn volgen. Behandeling met MTX dient daarom in de tweede lijn plaats te vinden.
Conclusie
Er is beperkt bewijs dat toevoeging van 10 mg methotrexaat per week aan een behandeling met prednisolon gedurende ten minste een jaar bij PMR kan resulteren in een kortere gebruiksperiode van prednisolon en minder terugval of recidief van de klachten.
Referenties
- Bahlas S, Ramos-Remus C, Davis P. Utilisation and costs of investigations, and accuracy of diagnosis of polymyalgia rheumatica by family physicians. Clin Rheumatol 2000;19: 278-80.
- Brooks RC, McGee SR. Diagnostic dilemmas in polymyalgia rheumatica. Arch Intern Med 1997;157:162-8.
- Dasgupta B, Salvarani C, Schirmer M, Crowson CS, Maradit-Kremers H, Hutchings A et al. Developing classification criteria for polymyalgia rheumatica: comparison of views from an expert panel and wider survey. J Rheumatol 2008;35: 270-7.
- Bird HA, Esselinckx W, Dixon AS, Mowat AG, Wood PH. An evaluation of criteria for polymyalgia rheumatica. Ann Rheum Dis 1979;38:434-9.
- Jones JG, Hazleman BL. Prognosis and management of polymyalgia rheumatica. Ann Rheum Dis 1981;40:1-5.
- Chuang TY, Hunder GG, Ilstrup DM, Kurland LT. Polymyalgia rheumatica: a 10-year epidemiologic and clinical study. Ann Intern Med 1982;97:672-80.
- Healey LA. Long-term follow-up of polymyalgia rheumatica: evidence for synovitis. Semin Arthritis Rheum 1984;13:322-8.
- Martinez-Taboada VM, Blanco R, Rodriguez-Valverde V. Polymyalgia rheumatica with normal erythrocyte sedimentation rate: clinical aspects. Clin Exp Rheumatol 2000;18: S34-S37.
- Cantini F, Salvarani C, Olivieri I. Erythrocyte sedimentation rate and C-reactive protein in the diagnosis of polymyalgia rheumatica. Ann Intern Med 1998;128:873-4.
- Cantini F, Salvarani C, Olivieri I, Macchioni L, Ranzi A, Niccoli L, et al. Erythrocyte sedimentation rate and C-reactive protein in the evaluation of disease activity and severity in polymyalgia rheumatica: a prospective follow-up study. Semin Arthritis Rheum 2000;30:17-24.
- Myklebust G, Gran JT. A prospective study of 287 patients with polymyalgia rheumatica and temporal arteritis: clinical and laboratory manifestations at onset of disease and at the time of diagnosis. Br J Rheumatol 1996;35:1161-8.
- Cimmino MA, Zaccaria A. Epidemiology of polymyalgia rheumatica. Clin Exp Rheumatol 2000;18:S9-11.
- Goodwin JS. The very low prevalence of polymyalgia rheumatica in blacks may be an artifact. J Am Geriatr Soc 1990;38:824-6.
- Smeeth L, Cook C, Hall AJ. Incidence of diagnosed polymyalgia rheumatica and temporal arteritis in the United Kingdom, 1990-2001. Ann Rheum Dis 2006;65:1093-8.
- Van de Lisdonk EH, Van den Bosch WJHM, Lagro-Janssen ALM. Ziekten in de huisartspraktijk. 5de editie. Maarssen: Elsevier Gezondheidszorg, 2008.
- Salvarani C, Cantini F, Macchioni P, Olivieri I, Niccoli L, Padula A, et al. Distal musculoskeletal manifestations in polymyalgia rheumatica: a prospective followup study. Arthritis Rheum 1998;41:1221-6.
- Ceccato F, Roverano SG, Papasidero S, Barrionuevo A, Rillo OL, Paira SO. Peripheral musculoskeletal manifestations in polymyalgia rheumatica. J Clin Rheumatol 2006;12:167-71.
- Bird HA, Leeb BF, Montecucco CM, Misiuniene N, Nesher G, Pai S, et al. A comparison of the sensitivity of diagnostic criteria for polymyalgia rheumatica. Ann Rheum Dis 2005;64:626-9.
- Gonzalez-Gay MA, Garcia-Porrua C, Salvarani C, Olivieri I, Hunder GG. The spectrum of conditions mimicking polymyalgia rheumatica in Northwestern Spain. J Rheumatol 2000;27:2179-84.
- Cantini F, Niccoli L, Storri L, Nannini C, Olivieri I, Padula A, et al. Are polymyalgia rheumatica and giant cell arteritis the same disease? Semin Arthritis Rheum 2004;33:294-301.
- Cantini F, Niccoli L, Nannini C, Bertoni M, Salvarani C. Diagnosis and treatment of giant cell arteritis. Drugs Aging 2008;25:281-97.
- Pavlica P, Barozzi L, Salvarani C, Cantini F, Olivieri I. Magnetic resonance imaging in the diagnosis of PMR. Clin Exp Rheumatol 2000;18:S38-S39.
- Bagratuni L. Anarthritic rheumatoid disease. Lancet 1956;271:694-7.
- Bagratuni L. Prognosis in the anarthritic rheumatoid syndrome. Br Med J 1963;1:513-8.
- Barber HS. Myalgic syndrome with constitutional effects; polymyalgia rheumatica. Ann Rheum Dis 1957;16:230-7.
- Warrington KJ, Jarpa EP, Crowson CS, Cooper LT, Hunder GG, Matteson EL, et al. Increased risk of peripheral arterial disease in polymyalgia rheumatica: a population-based cohort study. Arthritis Res Ther 2009;11:R50.
- Maradit Kremers H, Reinalda MS, Crowson CS, Davis JM, III, Hunder GG, Gabriel SE. Glucocorticoids and cardiovascular and cerebrovascular events in polymyalgia rheumatica. Arthritis Rheum 2007;57:279-86.
- Miller NR. Visual manifestations of temporal arteritis. Rheum Dis Clin North Am 2001;27:781-97, vi.
- Aiello PD, Trautmann JC, McPhee TJ, Kunselman AR, Hunder GG. Visual prognosis in giant cell arteritis. Ophthalmology 1993;100:550-5.
- Danesh-Meyer H, Savino PJ, Gamble GG. Poor prognosis of visual outcome after visual loss from giant cell arteritis. Ophthalmology 2005;112:1098-103.
- Liozon E, Herrmann F, Ly K, Robert PY, Loustaud V, Soria P, et al. Risk factors for visual loss in giant cell (temporal) arteritis: a prospective study of 174 patients. Am J Med 2001;111:211-7.
- Stone JH. Vasculitis: a collection of pearls and myths. Rheum Dis Clin North Am 2007;33:691-739, v.
- Hunder GG, Arend WP, Bloch DA, Calabrese LH, Fauci AS, Fries JF, et al. The American College of Rheumatology 1990 criteria for the classification of vasculitis. Introduction. Arthritis Rheum 1990;33:1065-7.
- Rao JK, Allen NB, Pincus T. Limitations of the 1990 American College of Rheumatology classification criteria in the diagnosis of vasculitis. Ann Intern Med 1998;129:345-52.
- Achkar AA, Lie JT, Hunder GG, O'Fallon WM, Gabriel SE. How does previous corticosteroid treatment affect the biopsy findings in giant cell (temporal) arteritis? Ann Intern Med 1994;120:987-92.
- Barraclough K, Liddell WG, Du Toit J, Foy C, Dasgupta B, Thomas M, et al. Polymyalgia rheumatica in primary care: a cohort study of the diagnostic criteria and outcome. Fam Pract 2008;25:328-33.
- Solomon S, Cappa KG. The headache of temporal arteritis. J Am Geriatr Soc 1987;35:163-5.
- Sathasivam S, Lecky B. Statin induced myopathy. BMJ 2008;337:a2286.
- Smetana GW, Shmerling RH. Does this patient have temporal arteritis? JAMA 2002;287:92-101.
- Van der Meer J, Stehouwer CDA. Interne geneeskunde. 13de editie. Houten: Bohn Stafleu van Loghum, 2005.
- Caporali R, Cimmino MA, Ferraccioli G, Gerli R, Klersy C, Salvarani C, et al. Prednisone plus methotrexate for polymyalgia rheumatica: a randomized, double-blind, placebo-controlled trial. Ann Intern Med 2004;141:493-500.
- Naschitz JE, Slobodin G, Yeshurun D, Rozenbaum M, Rosner I. Atypical polymyalgia rheumatica as a presentation of metastatic cancer. Arch Intern Med 1997;157:2381.
- Siebert S, Lawson TM, Wheeler MH, Martin JC, Williams BD. Polymyalgia rheumatica: pitfalls in diagnosis. J R Soc Med 2001;94:242-4.
- Li C, Dasgupta B. Corticosteroids in polymyalgia rheumatica -- a review of different treatment schedules. Clin Exp Rheumatol 2000;18:S56-S57.
- Vos PAJM, Bijlsma JWJ, Derksen RHWM. Polymyalgia rheumatica en arteriitis temporalis. Ned Tijdschr Geneeskd 2005;149:1932-7.
- Kyle V, Hazleman BL. Treatment of polymyalgia rheumatica and giant cell arteritis. I. Steroid regimens in the first two months. Ann Rheum Dis 1989;48:658-61.
- Carmona L. Quantifying risks: the case between glucocorticoids and tuberculosis. Arthritis Rheum 2006;55:1-2.
- NICE. Tuberculosis: clinical diagnosis and management of tuberculosis, and measures for its prevention and control (2006). Royal College of Physicians. Geraadpleegd mei 2009. Ga naar bron: NICE. Tuberculosis: clinical diagnosis and management of tuberculosis, and measures for its prevention and control (2006). Royal College of Physicians. Geraadpleegd mei 2009.
- Jick SS, Lieberman ES, Rahman MU, Choi HK. Glucocorticoid use, other associated factors, and the risk of tuberculosis. Arthritis Rheum 2006;55:19-26.
- Mulder AH, Nauta S, Pieters GF, Hermus AR. Addison-crisis bij patienten bekend wegens bijnierschorsinsufficientie: het belang van vroegtijdig ingrijpen. Ned Tijdschr Geneeskd 2008;152:1497-500.
- Hermus AR, Zelissen PM. Diagnostiek en therapie bij patienten met bijnierschorsinsufficientie. Ned Tijdschr Geneeskd 1998;142:944-9.
- Conn HO, Poynard T. Corticosteroids and peptic ulcer: meta-analysis of adverse events during steroid therapy. J Intern Med 1994;236:619-32.
- Leendertse AJ, Egberts AC, Stoker LJ, Van den Bemt PM. Frequency of and risk factors for preventable medication-related hospital admissions in the Netherlands. Arch Intern Med 2008;168:1890-6.
- Leeb BF, Bird HA. A disease activity score for polymyalgia rheumatica. Ann Rheum Dis 2004;63:1279-83.
- Binard A, De Bandt M, Berthelot JM, Saraux A. Usefulness of the disease activity scores for polymyalgia rheumatica for predicting glucocorticoid dose changes: a study of 243 scenarios. Arthritis Rheum 2007;57:481-6.
- Hutchings A, Hollywood J, Lamping DL, Pease CT, Chakravarty K, Silverman B, et al. Clinical outcomes, quality of life, and diagnostic uncertainty in the first year of polymyalgia rheumatica. Arthritis Rheum 2007;57:803-9.
- Kyle V, Hazleman BL. The clinical and laboratory course of polymyalgia rheumatica/giant cell arteritis after the first two months of treatment. Ann Rheum Dis 1993;52:847-50.
- Salvarani C, Cantini F, Niccoli L, Macchioni P, Consonni D, Bajocchi G, et al. Acute-phase reactants and the risk of relapse/recurrence in polymyalgia rheumatica: a prospective followup study. Arthritis Rheum 2005;53:33-8.
- Maradit Kremers H, Reinalda MS, Crowson CS, Zinsmeister AR, Hunder GG, Gabriel SE. Relapse in a population based cohort of patients with polymyalgia rheumatica. J Rheumatol 2005;32:65-73.
- Prickarts M, Lagro-Janssen T. Polymyalgia rheumatica in vier huisartspraktijken. Huisarts Wet 1999;42:597-601.
- Van der Veen MJ, Dinant HJ, Van Booma-Frankfort C, Van Albada-Kuipers GA, Bijlsma JW. Can methotrexate be used as a steroid sparing agent in the treatment of polymyalgia rheumatica and giant cell arteritis? Ann Rheum Dis 1996;55:218-23.
- Ferraccioli G, Salaffi F, De Vita S., Casatta L, Bartoli E. Methotrexate in polymyalgia rheumatica: preliminary results of an open, randomized study. J Rheumatol 1996;23:624-8.
- Caporali R, Montecucco C, Epis O, Bobbio-Pallavicini F, Maio T, Cimmino MA. Presenting features of polymyalgia rheumatica (PMR) and rheumatoid arthritis with PMR-like onset: a prospective study. Ann Rheum Dis 2001;60:1021-4.
- Visser K, Katchamart W, Loza E, Martinez-Lopez JA, Salliot C, Trudeau J, et al. Multinational evidence-based recommendations for the use of methotrexate in rheumatic disorders with a focus on rheumatoid arthritis: integrating systematic literature research and expert opinion of a broad international panel of rheumatologists in the 3E Initiative. Ann Rheum Dis 2009;68:1086-93.
- Verduijn MM, Van den Bemt BJF, Dijkmans BAC, Van der Waal RIF, Horikx A. Methotrexaat veilig, mits juist voorgeschreven. Ned Tijdschr Geneesk 2009;153:A695.