Ziekte van Parkinson
Richtlijnen diagnostiek
Naar Volledige tekst ›Anamnese
Naar Volledige tekst ›Vraag naar:
- aard van de klachten:
- aanwezigheid van tremor, gevoel van verminderde kracht, onhandigheid, stijfheid, pijn
- verandering in mimiek, spraak
- duur en beloop van klachten; eenzijdig of symmetrisch begin
- ernst van de klachten en gevolgen voor het dagelijks leven
- gerelateerde klachten en symptomen, zoals depressieve klachten, cognitieve stoornissen, autonome stoornissen
- gebruik van geneesmiddelen die reversibel parkinsonisme kunnen veroorzaken (antipsychotica, anti-emetica, SSRI’s, venlafaxine, bupropion, valproïnezuur)
Lichamelijk onderzoek
Naar Volledige tekst ›- Tremor:
- beoordeel handen en armen in ontspannen houding op tafel of in de schoot
- laat een beweging uitvoeren (bijvoorbeeld een glas water drinken of overschenken)
- laat de armen uitstrekken en uitgestrekt vooruit houden
- beoordeel of de tremor verandert bij een cognitieve taak, zoals rekenen of terugtellen
- Looppatroon: snelheid, gangspoor, paslengte, armzwaai
- Evenwicht: houdingsinstabiliteit bij opstaan, stilstaan, vooroverbuigen, lopen, draaien
- Motoriek
- Tonus en kracht van arm- en beenspieren bij passieve en actieve bewegingen: rigiditeit en tandradfenomeen
- Houding en gezichtsuitdrukking
- Spraak
Evaluatie
Naar Volledige tekst ›Symptomen die wijzen op een hypokinetisch-rigide syndroom
Naar Volledige tekst ›Traag bewegen (bradykinesie) plus ≥ 1 van de volgende symptomen:
- rigiditeit
- rusttremor
Symptomen die de diagnose ‘ziekte van Parkinson’ ondersteunen
Naar Volledige tekst ›- Houdingsinstabiliteit
- Unilateraal begin en blijvend asymmetrisch beeld
- Langzaam progressief beloop
- Afname van het reukvermogen die niet anderszins te verklaren is
- Traag looppatroon met verminderde armzwaai
- Voorovergebogen houding van de romp
- Zachte, monotone spraak
Zie ook tabel 1
Differentiaaldiagnose
Naar Volledige tekst ›Hypokinetisch-rigide syndroom
Naar Volledige tekst ›- Atypisch parkinsonisme
- Secundair parkinsonisme (medicamenteus (anti-emetica, antipsychotica), metabool, vasculair, overig)
Tremor
Naar Volledige tekst ›Kenmerkend voor de ziekte van Parkinson is een rusttremor die toeneemt bij het uitvoeren van een cognitieve taak. Voor de differentiaaldiagnose bij andere typen tremoren, zie NHG-Behandelrichtlijn Essentiële tremor.
Richtlijnen beleid bij vermoeden van hypokinetisch-rigide syndroom
Naar Volledige tekst ›- Stop of verander indien mogelijk de medicatie bij een vermoeden dat het syndroom veroorzaakt wordt door medicatie (antipsychotica, anti-emetica). Overleg zo nodig met de neuroloog of behandelend specialist.
- Verwijs patiënten die deze medicatie niet gebruiken binnen 6 weken naar een neuroloog.
Richtlijnen beleid bij ziekte van Parkinson
Naar Volledige tekst ›Algemeen
Naar Volledige tekst ›- De behandeling gebeurt bij voorkeur door een samenwerkingsverband van neuroloog, huisarts, paramedici en parkinsonverpleegkundige of verpleegkundig specialist (zie Organisatie van zorg).
- In eerste instantie berusten coördinatie en zorgverlening vooral bij de neuroloog en de parkinsonverpleegkundige, in het eindstadium verschuift dit naar de huisarts.
Rol van de huisarts
Naar Volledige tekst ›- Signaleren van bijwerkingen en veranderingen in effectiviteit of gebruik van de medicatie
- Signaleren en eventueel diagnosticeren en behandelen van nieuw ontstane (niet-motorische) symptomen of gerelateerde aandoeningen
- Intensiveren en coördineren van zorg in de terminale fase
- Signaleren van psychosociale problemen bij patiënt of partner/mantelzorger
Voorlichting en advies
Naar Volledige tekst ›- De rol van de huisarts wordt groter naarmate de ziekte vordert.
- Aandachtspunten:
- bewegen
- gewichtsverlies
- valrisico
- maatschappelijk functioneren, waaronder arbeidsparticipatie
- mantelzorg
- proactieve zorgplanning
Medicamenteuze behandeling
Naar Volledige tekst ›- De neuroloog start en controleert de medicamenteuze behandeling.
- Consulteer of verwijs naar de neuroloog bij veranderingen in werkzaamheid (bijvoorbeeld responsfluctuaties).
- Wees alert op een impulscontrolestoornis, bijvoorbeeld bij een verslaving (gokken, seksualiteit, winkelen en eten).
- Wees alert op dopaminedysregulatiesyndroom bij snelle dosisverhoging van dopaminerge medicatie of wanneer de patiënt om extra medicatie vraagt.
- Zorg dat dopaminerge medicatie indien mogelijk wordt gecontinueerd, ook rondom operaties en in de terminale fase (ter voorkoming van ernstige rigiditeit, tremoren en het maligne-levodopa onttrekkingssyndroom).
Niet-motorische symptomen en aandoeningen
Naar Volledige tekst ›- Niet-motorische klachten komen veel voor en hun intensiteit neemt toe met het vorderen van de ziekte.
- De huisarts heeft een rol in het signaleren van deze klachten, zeker als de patiënt zelf de relatie met de ziekte van Parkinson nog niet heeft gelegd.
- Niet-motorische klachten zijn onder andere: apathie, depressie, dementie, angst, hallucinaties, wanen, slaapstoornissen, pijn, vermoeidheid en autonome stoornissen zoals slikproblemen, speekselvloed, obstipatie, mictieklachten, seksuele problemen, orthostatische hypotensie en overmatig transpireren). Zie de volledige tekst voor diagnostiek en beleid bij deze symptomen en aandoeningen.
- Behandeling gebeurt meestal door of in overleg met de neuroloog.
Terminale fase
Naar Volledige tekst ›- Continueer bij voorkeur de dopaminerge medicatie, eventueel via een neus-maagsonde.
- Vermijd antidopaminerge medicatie (metoclopramide, haloperidol) en anticholinerge medicatie (atropine).
- Voor de medicamenteuze behandeling, zie tabel 2.
Consultatie en verwijzing
Naar Volledige tekst ›- Overweeg verwijzing bij parkinsongerelateerde klachten of problemen (zie tabel 3). Verwijs bij voorkeur naar een hulpverlener met parkinsonspecifieke kennis (zie Parkinsonzorgzoeker of ParkinsonNet.
- Verwijs direct naar neuroloog bij vermoeden van:
- maligne levodopa-onttrekkingssyndroom
- serotoninesyndroom
Belangrijkste wijzigingen
Naar Samenvatting ›- Het beleid bij niet-motorische symptomen is geactualiseerd en uitgebreid
- Er is informatie toegevoegd over spoedeisende complicaties, waaronder het maligne levodopa-onttrekkingssyndroom
- De informatie over het beleid bij patiënten met de ziekte van Parkinson in de terminale fase is uitgebreid
Kernboodschappen
Naar Samenvatting ›- Kenmerkend voor de ziekte van Parkinson is bradykinesie in combinatie met rigiditeit en/of rusttremor
- De behandeling is symptomatisch. Er zijn geen behandelingen die de progressie van de ziekte afremmen
- Niet-motorische symptomen of aandoeningen, zoals depressie, dementie en autonome stoornissen, komen veel voor. De intensiteit neemt meestal toe met het vorderen van de ziekte. In een latere fase kunnen deze symptomen op de voorgrond komen te staan
- Continueer indien mogelijk dopaminerge medicatie, ook in de terminale fase
- De behandeling vindt plaats in een samenwerkingsverband van huisarts, neuroloog en parkinsonverpleegkundige of verpleegkundig specialist. In het algemeen is de neuroloog hoofdbehandelaar van de gezondheidsproblemen die gerelateerd zijn aan de ziekte van Parkinson.
- De huisarts kan een rol hebben bij:
- vroege herkenning van symptomen die op de ziekte van Parkinson kunnen wijzen
- herkenning en eventuele behandeling van niet-motorische symptomen en aandoeningen die gerelateerd zijn aan de ziekte van Parkinson
- signalering van bijwerkingen of veranderingen in effectiviteit van medicatie
- signaleren van psychosociale problemen bij de patiënt en/of diens partner of mantelzorger
- het intensiveren en coördineren van zorg in de terminale fase
Inleiding
Naar Samenvatting ›Scope
Naar Samenvatting ›Richtlijnen voor diagnostiek en beleid bij:
- ziekte van Parkinson
- gerelateerde symptomen en aandoeningen
Buiten de scope
Naar Samenvatting ›- Andere vormen van tremor:
- versterkte fysiologische tremor
- essentiële tremor
- tremor bij cerebellaire pathologie (bijvoorbeeld cerebellair infarct of een erfelijke ataxie)
- tremor bij dystonie
- functionele tremor
- Andere oorzaken van parkinsonisme:
- vasculair parkinsonisme
- multipele systeematrofie
- corticobasale degeneratie
- progressieve supranucleaire paralyse
- Lewy body-dementie
- secundair parkinsonisme, bijvoorbeeld medicamenteus (o.a. neuroleptica) of metabool (o.a. ziekte van Wilson)
Samenwerking en afstemming
Naar Samenvatting ›Deze standaard sluit waar mogelijk aan bij de volgende richtlijnen:
- Deze NHG-Standaard is gebaseerd op de Multidisciplinaire richtlijn Ziekte van Parkinson. Deze multidisciplinaire richtlijn (MDR) kwam tot stand op initiatief van de Nederlandse Vereniging voor Neurologie (NVN) en de Nederlandse Vereniging van Revalidatieartsen (VRA), met medewerking van het NHG.
- De adviezen met betrekking tot de laatste levensfase zijn afgestemd op de Richtlijn Ziekte van Parkinson: de palliatieve fase van Integraal Kankercentrum Nederland (IKNL).
Achtergronden
Naar Samenvatting ›Begrippen
Naar Samenvatting ›Bradykinesie
Traagheid in bewegen
Hypokinesie
Afnemende amplitude van bewegingen
Dopaminedysregulatiesyndroom
Toegenomen behoefte aan en overmatig gebruik van dopaminerge medicatie. Dit syndroom kan gepaard gaan met motorische klachten (vooral ernstige dyskinesieën), dwangmatig gebruik van de medicatie, opwinding, (hypo)manie, agressie en/of hallucinaties
Dyskinesieën
Onwillekeurige, doelloze bewegingen, meestal van hoofd en/of ledematen, meestal als gevolg van dopaminerge medicatie
Freezing
Bewegingsblokkade, bijvoorbeeld tijdens het lopen, waardoor het lijkt alsof de voeten aan de vloer blijven kleven of eraan vastgevroren zitten
Hypokinetisch-rigide syndroom
Verzamelnaam voor ziektebeelden gekenmerkt door bradykinesie in combinatie met minstens 1 van de volgende symptomen:
- rigiditeit
- rusttremor
De ziekte van Parkinson is de meest voorkomende oorzaak van het hypokinetisch-rigide syndroom
Impulscontrolestoornis
Pathologisch gokken, hyperseksualiteit, dwangmatige vormen van kopen, eten en internetgebruik als bijwerking van dopaminerge medicatie of het overmatig gebruik hiervan.
Maligne levodopa-onttrekkingssyndroom
Gedaald bewustzijn, extreme rigiditeit (met verhoogde spierenzymen), hoge koorts en autonome stoornissen (bijvoorbeeld tachycardie), meestal veroorzaakt door acute onthouding (≥ 24 uur) van dopaminerge medicatie (vooral levodopa), bijvoorbeeld postoperatief
Rigiditeit
Stijfheid, voelbaar door een verhoogde spiertonus bij passief bewegen
Responsfluctuaties
Schommelingen in de klinische reactie op dopaminerge medicatie, meestal na een ziekteduur van een aantal jaren. In het begin van de behandeling zijn deze fluctuaties vaak voorspelbaar, later kunnen ze onvoorspelbaar worden
- On-fase: de fase waarin de medicatie goed werkt.
- Off-fase: de medicatie is uitgewerkt, gekenmerkt door stijfheid, traagheid en/of tremor.
- Peak-dose dyskinesieën: onwillekeurige bewegingen als gevolg van een plotselinge stijging van de dopamine concentratie na inname van de medicatie.
Rusttremor
Tremor die aanwezig is als het lichaamsdeel ondersteund en ontspannen is, bijvoorbeeld als een arm op tafel ligt.
Tandradfenomeen
Schokkende beweging die voelbaar is bij passieve beweging van een gewricht
Tremor
Onwillekeurige, ritmische, trillende beweging die unilateraal of symmetrisch aanwezig kan zijn. Voor de indeling van tremoren, zie NHG-Behandelrichtlijn Essentiële tremor
Dopaminedysregulatiesyndroom (DDS)
Van de patiënten met de ziekte van Parkinson ontwikkelt 3-4% een DDS. Waar sommige experts de DDS zien als een complicatie van een niet (h)erkende en niet behandelde niet-motorische anticipatieangst, spanning of paniek die ontstaat bij wearing-off, zien andere experts het meer als een aan verslaving-gerelateerde impulscontrolestoornis. De klinische kenmerken zijn:
- behoefte aan hogere dosering dopaminerge medicatie dan nodig om symptomen en klachten te verlichten
- pathologisch gebruikspatroon: behoefte aan hogere doseringen dopaminerge medicatie in aanwezigheid van significante dyskinesieën, hamsteren van of op zoek gaan naar medicatie, onwil of onvermogen om de dosering te verlagen, afwezigheid van pijnlijke dystonieën
- stoornissen in gedrag en in sociaal en/of beroepsmatig functioneren (agressief gedrag, verlies van vrienden, werkverzuim, baanverlies, juridische problemen, ruzies of problemen met familie)
- ontwikkeling van een hypomaan/manisch of cyclothymisch affectief beeld in relatie tot hoge dosering dopaminerge medicatie
- ontwikkeling van onttrekkingsverschijnselen, zoals dysforie, depressie, prikkelbaarheid en angst, bij dosisverlaging of -normalisering
- duur van de verstoring ≥ 6 maanden
Dyskinesieën
In het beloop van de ziekte kunnen perioden van overbeweeglijkheid optreden. Het betreft hier geen tremoren of ritmische bewegingen maar een meer choreatiforme overbeweeglijkheid die soms gepaard gaat met dystonie (langdurige verkramping). Meestal gaat het om peak-dose-dyskinesieën doordat de hersenen niet meer goed kunnen omgaan met de plotselinge stijging van de dopamineconcentratie na de inname van medicatie.
Impulscontrolestoornis
Impulscontrolestoornissen komen voor bij 14-30% van de patiënten met de ziekte van Parkinson. Het betreft vooral gedragsverslavingen op het gebied van gokken, seksualiteit, kopen en eten. De stoornis uit zich vaak al in een vroege fase als reactie op de dopaminerge medicatie. Dopamineagonisten geven een relatief groter risico op een impulscontrolestoornis dan levodopapreparaten. Hyperseksualiteit kan zich op verschillende manieren uiten, zoals toegenomen seksuele behoefte, overmatig masturberen en in zeer zeldzame gevallen parafilieën.
Impulscontrolestoornissen hebben over het algemeen grote impact op de patiënt en diens omgeving, en vaak ook financiële gevolgen. Daarom is voorafgaand aan start van de dopaminerge medicatie uitleg over het risico en de kenmerken van een impulscontrolestoornis van belang. Zo zullen patiënt en naasten een verandering in het gedrag sneller herkennen en in verband brengen met de medicatie.
Maligne levodopa-onttrekkingssyndroom
Dit beeld is vergelijkbaar met het maligne neurolepticasyndroom, maar heeft andere oorzaken. Mogelijke oorzaken zijn een plotselinge verandering in dopaminerge medicatie (dosisreductie), verminderde absorptie (bijvoorbeeld door ernstige obstipatie), infecties, trauma en stress.
De behandeling bestaat uit opname op de intensive care, behandeling met dopaminerge medicatie en ondersteunende maatregelen zoals intraveneuze vochttoediening en koelen. De incidentie bedraagt 3 per 1000 patiënten per jaar. Bij ouderen met sarcopenie is het beloop minder ernstig doordat bij hen minder rabdomyolyse optreedt.
Responsfluctuaties
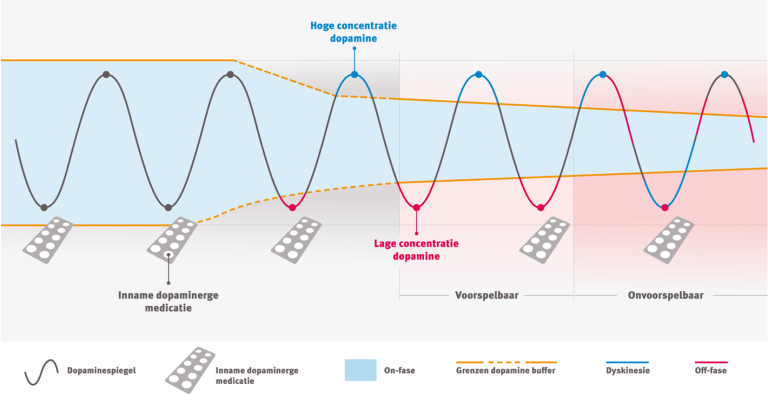
Van de patiënten die met levodopa behandeld worden, ontwikkelt 40-50% na ongeveer 5 jaar zogeheten responsfluctuaties, ook wel on-off-fluctuaties genoemd. Tijdens de on-fase is er een goede motorische respons op de dopaminerge medicatie, maar tijdens de off-fase, als de medicatie uitgewerkt raakt, keren motorische klachten zoals een tremor terug.
Wanneer de on- en de off-fases een patroon volgen dat gerelateerd kan worden aan de inname van de medicatie, spreken we van voorspelbare responsfluctuaties. Wanneer er geen duidelijke relatie is met het tijdstip van inname, spreekt men van onvoorspelbare responsfluctuaties (zie figuur d1). Onvoorspelbare responsfluctuaties kunnen gerelateerd zijn aan gastro-intestinale problematiek.
Geavanceerde behandelingen om deze responsfluctuaties tegen te gaan zijn apomorfine subcutaan of intraduodenale levodopa/carbidopa. Deze middelen zorgen voor een continue dopaminerge afgifte.
Epidemiologie
Naar Samenvatting ›- Na de ziekte van Alzheimer is de ziekte van Parkinson de meest voorkomende chronische neurodegeneratieve aandoening
- Incidentie in de huisartsenpraktijk: 0,2-0,4 per 1000 patiënten per jaar
- Prevalentie in de huisartsenpraktijk: 3,7 per 1000 mannen en 2,4 per 1000 vrouwen. De prevalentie stijgt
- Van de patiënten met de ziekte van Parkinson is ca. 80% bij diagnose > 65 jaar en 3-5% bij diagnose < 50 jaar
De ziekte van Parkinson in de huisartsenpraktijk
In 2022 was de incidentie van parkinsonisme, waarvan de ziekte van Parkinson de voornaamste groep uitmaakt (ICPC-code N87) in de huisartsenpraktijk 0,4 per 1000 mannen per jaar en 0,2 per 1000 vrouwen per jaar. De prevalentie bedroeg 3,7 per 1000 mannen per jaar en 2,4 per 1000 vrouwen per jaar. Dit is een onderschatting van het werkelijke aantal mensen met de ziekte van Parkinson, want personen die zijn opgenomen in een verpleeghuis worden niet meegerekend en de diagnose wordt vaak pas laat in het leven gesteld. In bevolkingsonderzoek wordt de prevalentie van de ziekte van Parkinson en andere vormen van parkinsonisme een factor 2-2,5 hoger geschat dan in huisartsenregistraties [VZinfo.nl]. Het aantal personen met een vorm van parkinsonisme neemt toe met de leeftijd. Bij een begin op de leeftijd van 21-40 jaar spreken we van Young Onset Parkinson’s disease (YOPD). Bij 3-5% van de patiënten starten de symptomen vóór de leeftijd van 40-50 jaar. Alleen al door vergrijzing van de bevolking zal de jaarprevalentie van de ziekte van Parkinson in 2040 naar verwachting 56% hoger zijn dan in 2018 [VZinfo.nl].
Gender
De incidentie en prevalentie van de ziekte van Parkinson zijn bij mannen hoger dan bij vrouwen, en bij mannen openbaart de ziekte zich op gemiddeld jongere leeftijd dan bij vrouwen. In de Vektis-database worden alle patiënten met de ziekte van Parkinson in Nederland geregistreerd. Onderzoek in deze database wees uit dat de diagnose ‘ziekte van Parkinson’ in 2012-2016 gesteld werd bij 22.293 patiënten. De gemiddelde leeftijd bij diagnose was bij mannen (n= 13.518) 71,6 jaar en bij vrouwen (n= 8775) 72,5 jaar. Mogelijk is dit verschil toe te schrijven aan oestrogenen, maar het werkingsmechanisme is onbekend.
Waarschijnlijk is de ziekte bij mannen sneller progressief dan bij vrouwen. In het genoemde databaseonderzoek deden vrouwen echter eerder en vaker een beroep op verschillende zorgverleners (huisarts, fysiotherapeut, ergotherapeut, logopedist).
Etniciteit
Of er verschillen zijn tussen de incidentie en het beloop van de ziekte van Parkinson in verschillende etnische groeperingen is niet bekend.
Mortaliteit
De sterfte aan de ziekte van Parkinson als primaire doodsoorzaak was in 2021 13,1 per 100.000 mannen en 8,2 per 100.000 vrouwen [VZinfo.nl].
Etiologie en pathofysiologie
Naar Samenvatting ›- Bij de ziekte van Parkinson is het aantal dopamineproducerende neuronen in de substantia nigra afgenomen
- De oorzaak en de exacte pathofysiologie van dit proces zijn niet bekend, vermoedelijk spelen zowel genetische als omgevingsfactoren een rol:
- genetische factoren spelen vooral bij patiënten < 40 jaar; bij naar schatting 5-10% van de patiënten heeft de ziekte van Parkinson een erfelijke oorzaak
- omgevingsfactoren: mogelijke risicofactoren zijn blootstelling aan pesticiden, wonen in een industriegebied, luchtverontreiniging, wonen op het platteland en werken in de agrarische sector
Pathofysiologie
De exacte pathofysiologie is niet bekend. Kenmerkend is de degeneratie van neuronen in specifieke regio’s van de hersenen, waaronder de dopaminerge neuronen in de pars compacta van de substantia nigra, waardoor een tekort aan de neurotransmitter dopamine ontstaat. Daarnaast ziet men intraneuronale ophopingen van lewylichaampjes en lewyneurieten. Eén van de belangrijkste proteïnen in deze ophopingen is alfasynucleïne. Op moleculair niveau dragen disfunctie van mitochondriën, oxidatieve stress, verstoorde afbraak van proteïnen en reactieve microgliose bij aan de neurodegeneratie. Het hypokinetisch-rigide syndroom treedt op als de dopaminerge activiteit met 50-60% is afgenomen.
Etiologie
Gevorderde leeftijd en mannelijk geslacht worden als belangrijkste risicofactoren voor de ziekte van Parkinson beschouwd. Mogelijk zijn hoofd-hersentrauma’s en ontstekingen in de hersenen predisponerende factoren. Ook genetische factoren en omgevingsfactoren(toxische stoffen) spelen een rol.
Genetische factoren
Bij naar schatting 5-10% van de patiënten heeft de ziekte van Parkinson een erfelijke oorzaak. Bij de erfelijke vorm van de ziekte ontstaan de eerste symptomen meestal voor het 40e jaar. Het aantal bekende etiologische genmutaties neemt nog steeds toe. Daarnaast worden steeds meer genetische risicofactoren ontdekt die zijn geassocieerd met een iets grotere kans op het ontstaan van de ziekte van Parkinson, ook bij de vormen van de ziekte die op latere leeftijd ontstaan. De meest voorkomende genen die betrokken zijn bij een autosomaal dominante overerving zijn SNCA, LRRK2, GBA en VPS35, de meest voorkomende genen die betrokken zijn bij een autosomaal recessieve overerving zijn PARKIN, PINK1 en DJ-1.
Omgevingsfactoren
Mogelijke risicofactoren voor de ziekte van Parkinson zijn wonen in een industriegebied, wonen op het platteland, drinken van bronwater en zuivel, en werken in de agrarische sector. Structureel bewijs hiervoor is nog niet gevonden. Pesticiden zijn geassocieerd met een verhoogd risico op de ziekte van Parkinson. Specifieke pesticiden die tot een verhoogd risico leiden, zijn echter niet geïdentificeerd. Er is vooral onderzoek gedaan naar de rol van de onkruidbestrijder paraquat (1,1’-dimethyl-4,4’bipyridine). Uit een systematische review van 9 patiënt-controleonderzoeken (n = 6270) bleek dat de prevalentie van de ziekte van Parkinson 25% hoger was bij mensen die waren blootgesteld aan paraquat (OR 1,25; 95%-BI 1,01 tot 1,55). In 1 geïncludeerd cohortonderzoek (n = 56.009) werd een risicoverschil gevonden tussen mensen die waren blootgesteld aan paraquat en mensen die dat niet waren, maar dit verschil was niet significant (OR 1,08; 95%-BI 0,57 tot 2,04). Door beperkingen in de onderzoeksopzet (vaak onduidelijkheid over de mate en duur van de blootstelling aan paraquat) kon een oorzakelijke relatie niet ondubbelzinnig worden aangetoond.
Beschermende factoren
Roken en cafeïne lijken het risico op de ziekte van Parkinson te verkleinen. Daarnaast zijn er aanwijzingen dat voldoende lichaamsbeweging een beschermend effect heeft.
Klinisch beeld
Naar Samenvatting ›Bij ongeveer 2/3 van de patiënten met de ziekte van Parkinson openbaart de ziekte zich met klachten van een (rust)tremor. Daarnaast kan de patiënt zich presenteren met:
- een zwak, onhandig, pijnlijk of stijf gevoel in arm of been
- een traag looppatroon met verminderde armzwaai
Prodromale symptomen
Naar Samenvatting ›Verschillende verschijnselen kunnen al jaren aanwezig zijn voordat de klassieke motorische klachten (bradykinesie, rigiditeit en/of tremor) tot uiting komen. Voorbeelden:
- verslechtering van slaapkwaliteit en slaapduur
- REM-slaapgedragsstoornis (onvoldoende verslapping van de spieren tijdens de REM-slaap, zich uitend in complex motorisch en vocaal gedrag (het fysiek uitleven van een droom))
- vermindering van het reukvermogen
- autonome stoornissen (geringe hypotensie, urge-incontinentie, erectiele disfunctie, obstipatie, overmatig transpireren)
- balansstoornis
- vermoeidheid
- Schrag 2015. In een patiënt-controleonderzoek uitgevoerd in het Verenigd Koninkrijk werden 8166 personen met de ziekte van Parkinson en 46.755 personen zonder de ziekte geïncludeerd. In het huisartseninformatiesysteem werd de incidentie van klachten in de groep bij wie later de diagnose van Parkinson werd gesteld vergeleken met die in de controlegroep. In de 2 jaar voorafgaand aan de diagnose had de parkinsongroep een hogere incidentie van tremor (RR 32,54; 95%-BI 24,94 tot 42,90), obstipatie (RR 2,44; 95%-BI 2,29 tot 2,59), vermoeidheid RR 1,79 (95%-BI 1,55 tot 2,06), duizeligheid (RR 1,80 95%-BI 1,58 tot 2,05), depressie (RR 2,15; 95%-BI 1,85 tot 2,49), schouderpijn of -stijfheid (RR 1,35; 95%-BI 1,17 tot 1,56); angst (RR 1,89; 95%-BI 1,58 tot 2,25), mictieklachten (RR 2,27; 95%-BI 1,80 tot 2,85), erectiele disfunctie (RR 1,30; 95%-BI 1,06 tot 1,57), slaapstoornissen (RR 1,38; 95%-BI 1,11 tot 1,70), hypotensie (RR 3,03; 95%-BI 2,18 tot 4,18), balansstoornissen (RR 2,43; 95%-BI 1,69 tot 3,44), geheugenproblemen (RR 2,13; 95%-BI 1,44 tot 3,11) en rigiditeit (RR 2,63; 95%-BI 1,11 tot 5,79). Ook 2-5 jaar voor de diagnose was de incidentie van tremor, balansstoornissen, obstipatie, hypotensie, erectiele disfunctie, mictieklachten, duizeligheid, vermoeidheid, depressie en angst significant hoger in de parkinsongroep. En 10 jaar voordat de diagnose gesteld werd, was de incidentie van tremor en obstipatie in de parkinsongroep significant hoger.
- Plouvier 2014. In een Nederlands patiënt-controleonderzoek (86 patiënten met de diagnose ‘ziekte van Parkinson’ en 78 controlepatiënten) werd van verschillende symptomen bekeken hoe vaak ze in het huisartseninformatiesysteem werden gerapporteerd in de 2 jaar voorafgaand aan de diagnose. Functionele somatische symptomen (gedefinieerd als fysieke klachten bij patiënten met veronderstelde psychosociale problemen of psychische stress, waarvoor bij adequaat onderzoek geen medische verklaring wordt gevonden) kwamen significant vaker voor in de parkinsongroep (38,4 vs. 21,8%; OR 2,45; 95%-BI 1,2 tot 5,1). Dit gold ook voor slaapstoornissen (25,6 vs. 3,9%; OR 6,98; 95%-BI 2,0 tot 24,3) en overmatig transpireren (dit werd alleen in de parkinsongroep gerapporteerd: 9,3 vs. 0%).
- Een REM-slaapgedragsstoornis is de sterkste prodromale niet-motorische marker voor het ontwikkelen van een alfasynucleïnopathie. Dit is een groep neurodegeneratieve ziekten die bestaat uit de ziekte van Parkinson, multipele systeematrofie en Lewy body-dementie. Wanneer de De voorspellende waarde van een REM-slaapgedragsstoornis die bewezen is met een polysomnografie is zeer hoog. In prospectieve onderzoeken met een lange follow-up kreeg > 75% van de patiënten met een REM-slaapgedragsstoornis uiteindelijk een alfasynucleïnopathie.
Motorische symptomen
Naar Samenvatting ›- Kenmerkend voor de ziekte van Parkinson is bradykinesie in combinatie met rigiditeit en/of rusttremor.
- Andere kenmerken zijn onder andere: maskergelaat, micrografie, voorovergebogen houding van de romp (zie tabel 1).
- Er is een grote variatie in aard en ernst van de symptomen. Bij sommige patiënten staan bradykinesie en rigiditeit op de voorgrond, bij anderen rusttremor. In de eerste groep is de progressie van de ziekte doorgaans sneller dan in de tweede groep.
- De klachten beginnen unilateraal, maar kunnen later ook aan de andere zijde optreden. In dat geval blijven de klachten asymmetrisch: ze blijven erger aan de kant waar ze begonnen
Niet-motorische symptomen
Naar Samenvatting ›- Niet-motorische stoornissen komen veel voor, soms al vóórdat motorische symptomen tot uiting komen.
- Enkele veelvoorkomende niet-motorische symptomen (zie ook tabel 1):
- verminderd reukvermogen (hyposmie) komt voor bij ongeveer 80% van de patiënten.
- cognitieve stoornissen (meestal aandacht, tempo en executieve functies, maar ook geheugen en visueel-ruimtelijke oriëntatie); 48-80% van de patiënten ontwikkelt na verloop van tijd parkinsondementie.
- depressieve symptomen komen voor bij ongeveer 30% van de patiënten, vaak in combinatie met cognitieve stoornissen.
- wanen en hallucinaties zijn veelvoorkomende bijwerkingen van parkinsonmedicatie, maar kunnen ook zonder medicatie ontstaan; deze psychotische symptomen kunnen op elk moment in het beloop ontstaan; bij 30% van de patiënten ontstaan ze in de eerste 5 jaar na de diagnose.
- impulscontrolestoornissen als gevolg van dopaminerge medicatie komen voor bij 14-30% van de patiënten (vooral patiënten < 45 jaar), meestal in de vorm van een verslaving (gokken, seksualiteit, winkelen, eten) of dwangmatig gebruik van dopaminerge medicatie (dopaminedysregulatiesyndroom).
- De intensiteit van niet-motorische symptomen neemt meestal toe met het vorderen van de ziekte.
Diagnose
Naar Samenvatting ›- De ziekte van Parkinson is een diagnose die door de neuroloog wordt gesteld op grond van het klinische beeld.
- Het differentiëren tussen de ziekte van Parkinson, atypisch parkinsonisme en secundair parkinsonisme is van belang, zowel voor het beloop als de behandeling (zie Evaluatie)
Klinische diagnose
- Goed opgezet onderzoek naar de diagnostische waarde van anamnese en lichamelijk onderzoek in de huisartsenpraktijk is niet voorhanden.
- De diagnose ‘ziekte van Parkinson’ is een klinische diagnose, waarbij de neuroloog gebruik maakt van de Movement Disorder Society clinical diagnostic criteria for Parkinson’s disease.
- Zekerheid over de diagnose kan alleen worden verkregen door neuropathologisch onderzoek post mortem, waarbij lewylichaampjes en gedegenereerde dopaminerge neuronen worden aangetroffen.
Differentiaaldiagnose
- De Multidisciplinaire richtlijn Ziekte van Parkinson maakt onderscheid tussen de ziekte van Parkinson en atypisch parkinsonisme. Als groep hebben atypische parkinsonismen klinische overeenkomsten met de ziekte van Parkinson, maar ook een aantal belangrijke verschillen. Deze verschillen zijn onder andere een (gemiddeld) snellere progressie, een beperktere tot afwezige reactie op parkinsonmedicatie en een kortere levensverwachting.
- Symptomen die kunnen wijzen op atypisch parkinsonisme:
- snel progressief beloop
- cerebellaire verschijnselen zoals ataxie
- verticale blikparese
- bilaterale, symmetrische verschijnselen
- ernstige dysfonie, dysartrie, dysfagie vroeg in het beloop
- ernstige autonome verschijnselen vroeg in het beloop
- ernstige dementie vroeg in het beloop (kan wijzen op Lewy body-dementie)
- Zie tabel d1 voor de differentiaaldiagnose van het hypokinetisch-rigide syndroom.
|
Ziekte van Parkinson |
Atypisch parkinsonisme |
Secundair parkinsonisme |
|
Infectieus/inflammatoir:
|
|
|
|
Toxisch:
|
|
|
Medicatie:
|
||
|
Metabool:
|
||
|
Overig:
|
||
|
Psychogeen |
||
|
Vasculair |
||
|
SCA = spinocerebellaire ataxie. |
||
Aanvullend onderzoek
Als de patiënt een kenmerkende vorm van de ziekte heeft en bij de eerste verschijnselen > 50 jaar is, wordt geen aanvullend onderzoek gedaan. De neuroloog zal in de volgende gevallen aanvullend onderzoek overwegen :
- beeldvormend onderzoek (123I-FP-CIT SPECT of 18F-DOPA PET en/of MRI-hersenen) bij atypische kenmerken en/of een beloop dat niet past bij de ziekte van Parkinson
- onderzoek naar de ziekte van Wilson bij debuutleeftijd < 50 jaar (normale waarden van koper en ceruloplasmine in bloedonderzoek, normale 24-uurs koperexcretie in urineonderzoek en afwezigheid van kayser-fleischerringen in de cornea maken de ziekte van Wilson zeer onwaarschijnlijk)
- counseling over genetische diagnostiek bij patiënten met:
- debuutleeftijd < 40 jaar óf
- eerstegraads familielid met de ziekte van Parkinson
Genetische diagnostiek
De waarschijnlijkheid dat een patiënt een in aanleg genetische variant van de ziekte van Parkinson heeft, is groter bij een lage debuutleeftijd (< 40 jaar) en een positieve familieanamnese. Genetisch testen bij de ziekte van Parkinson is alleen zinvol onder specifieke condities :
- genetisch onderzoek kan worden overwogen bij alle patiënten met een kenmerkende vorm van de ziekte en een debuutleeftijd < 40 jaar
- onderzoek naar de genen LRRK2 en SNCA kan worden overwogen bij patiënten met een kenmerkende vorm van de ziekte en een duidelijke dominante overerving
- onderzoek naar de genen PARKIN, PINK1 en DJ-1 kan worden overwogen bij patiënten met een kenmerkende vorm van de ziekte, een debuutleeftijd < 50 jaar en een familieanamnese die kan passen bij autosomaal recessieve overerving (broer of zus aangedaan, ouders niet).
Beloop
Naar Samenvatting ›- De ziekte van Parkinson is een progressieve aandoening, waarbij meestal een aanvankelijk asymmetrisch hypokinetisch-rigide syndroom zonder evenwichtsstoornissen gevolgd wordt door evenwichtsstoornissen en functiebeperkingen aan beide zijden.
- Veel patiënten raken uiteindelijk dermate beperkt dat ze alleen met hulp kunnen lopen en rolstoelafhankelijk worden.
- Niet-motorische symptomen kunnen al in het begin van de ziekte aanwezig zijn, maar ook in het beloop van de ziekte ontstaan.
- Wanneer bradykinesie en rigiditeit op de voorgrond staan, is de progressie van de ziekte doorgaans sneller dan wanneer de tremor op de voorgrond staat.
- Patiënten hebben een kortere levensverwachting dan leeftijdsgenoten zonder de ziekte van Parkinson (ongeveer 2 × zo hoog risico om binnen 10 jaar te overlijden). Bij dementie daalt de levensverwachting nog verder.
- De meeste patiënten overlijden niet aan de ziekte van Parkinson zelf, maar aan een comorbide aandoening.
Stadia
De literatuur onderscheidt 3 stadia in de ziekte van Parkinson:
- in de preklinische fase is het neurodegeneratieve proces al begonnen, maar zijn er nog geen symptomen en/of verschijnselen
- in de prodromale fase zijn er al wel symptomen en verschijnselen, maar zijn deze nog onvoldoende om de diagnose met zekerheid te kunnen stellen
- in de klinische fase zijn er symptomen en verschijnselen, en kan de diagnose ‘ziekte van Parkinson’ worden gesteld op basis van de klassieke motorische symptomen (bradykinesie, rigiditeit en/of tremor).
Ernst en progressie
- De ernst en progressie van functiestoornissen, beperkingen in activiteiten en participatieproblemen variëren van persoon tot persoon en laten zich niet voorspellen.
- De aangepaste schaal van Hoehn en Yahr kan worden gebruikt om de ernst van de ziekteverschijnselen vast te stellen (zie tabel d2).
|
Stadium |
Symptomen |
|
1 |
Alleen unilaterale motorische symptomen |
|
1,5 |
Unilaterale en axiale motorische symptomen |
|
2 |
Bilaterale motorische symptomen zonder lichaamsinstabiliteit/onbalans |
|
2,5 |
Geringe bilaterale motorische symptomen met intacte reflexen op onverwachte wijziging van de lichaamshouding |
|
3 |
Geringe tot matige bilaterale motorische symptomen; geringe lichaamsinstabiliteit/onbalans; fysiek zelfstandig |
|
4 |
Ernstige functiebeperkingen; zelfstandig lopen en staan lukt nog |
|
5 |
Zorgafhankelijk; aan bed of rolstoel gebonden als geen hulp wordt geboden |
Levensverwachting
De levensverwachting van patiënten met de ziekte van Parkinson is minder dan die van leeftijdgenoten in de algemene bevolking.
- De Lau 2005. In een cohortonderzoek met een follow-up van 9 jaar onder 6969 mensen ≥ 55 jaar in de algemene bevolking van Rotterdam was in de groep met de ziekte van Parkinson 54% overleden, versus 24% in de groep zonder de ziekte van Parkinson (HR 1,83; 95%-BI 1,47 tot 2,26). Bij parkinsonpatiënten met dementie was het risico op overlijden groter dan bij patiënten zonder dementie (HR 2,85; 95%-BI 1,77 tot 4.62).
- Dommershuijsen 2020. In ditzelfde Rotterdamse cohortonderzoek, nu met een follow-up van 12 jaar, was de gemiddelde leeftijd bij diagnose 78,6 jaar (SD 8,1). Was de diagnose gesteld op een leeftijd < 55 jaar dan was de levensverwachting 10,1 jaar korter (95%-BI 5,6 tot 14,3) dan die van gematchte controlepatiënten; bij diagnose < 65 jaar was de levensverwachting 6,7 jaar korter (95%-BI 2,4 tot 10,7) en bij diagnose < 75 jaar was de levensverwachting 3,5 jaar korter (95%-BI –0,4 tot 7,2). Patiënten van 85 jaar hadden een 1,2 jaar kortere levensverwachting dan gematchte controlepatiënten (95%-BI –2,2 tot 4,5).
- De Lau 2014. In een ander Nederlands cohortonderzoek onder 414 parkinsonpatiënten was na een follow-up van gemiddeld 4,3 jaar 11,8% van de patiënten overleden. Onafhankelijke voorspellende factoren waren mannelijk geslacht, cognitieve stoornissen, houdingsinstabiliteit en psychotische symptomen.
Complicaties
Naar Samenvatting ›Veelvoorkomende complicaties zijn:
- vallen (bijvoorbeeld ten gevolge van orthostatische hypotensie, balansstoornissen of ondervoeding)
- aspiratiepneumonie (ten gevolge van slikproblemen)
Spoedeisende complicaties
Naar Samenvatting ›Koorts bij een patiënt met de ziekte van Parkinson kan een symptoom zijn van het maligne levodopa-onttrekkingssyndroom of het serotoninesyndroom. Beide zijn zeldzame, maar ernstige complicaties.
Maligne levodopa-onttrekkingssyndroom
- Dit syndroom wordt meestal veroorzaakt door acute onthouding (≥ 24 uur) van dopaminerge medicatie, vooral levodopa, bijvoorbeeld postoperatief.
- Andere oorzaken:
- plotselinge verandering in dopaminerge medicatie (dosisreductie)
- verminderde absorptie (bijvoorbeeld door ernstige obstipatie)
- infecties
- trauma
- stress
- Symptomen:
- gedaald bewustzijn
- extreme rigiditeit (met verhoogde spierenzymen)
- hoge koorts
- autonome stoornissen (bijvoorbeeld tachycardie)
- Zonder behandeling is het beloop ernstig met mogelijk ontstaan van aspiratiepneumonie, acuut nierfalen als gevolg van rabdomyolyse en dehydratie, en trombo-embolische complicaties. De mortaliteit bedraagt 4%.
Serotoninesyndroom
- Dit syndroom wordt meestal veroorzaakt door de combinatie van MAO-B-remmers met andere sterk serotonerg werkende medicatie, zoals SSRI’s, TCA’s en tramadol. Dit zorgt voor verhoogde serotonineconcentraties in het centrale en perifere zenuwstelsel (zie NHG-Standaard Angst en NHG-Standaard Depressie).
- Symptomen lijken op die van het maligne levodopa-onttrekkingssyndroom (gedaald bewustzijn, extreme rigiditeit, hoge koorts, autonome stoornissen), met mogelijk ook:
- verwijde pupillen
- overactieve reflexen
- diarree
- acathisie (innerlijke onrust en karakteristieke bewegingen van de benen)
Paralytische ileus
- De oorzaak is vertraagde darmmotiliteit als gevolg van autonome disfunctie. Paralytische ileus wordt vaak voorafgegaan door ernstige obstipatie
- Mogelijke symptomen zijn zwelling van het abdomen, pijn, misselijkheid en braken.
- Preventie van obstipatie is belangrijk (zie NHG-Standaard Obstipatie).
Neuropsychiatrische complicaties
Onder andere psychose, depressie, impulscontrolestoornissen en het dopaminedysregulatiesyndroom (zie Niet-motorische symptomen).
De informatie in dit detail is gebaseerd op overzichtsartikelen van Ghosh, Simonet en Van der Kolk.
Serotoninesyndroom
De behandeling bestaat uit het staken van de serotonerge medicatie en zo nodig opname (zie ook NHG-Standaard Angst en NHG-Standaard Depressie).
Paralytische ileus (of pseudo-obstructieve ileus)
De incidentie bedraagt ca. 2,4%. Een mogelijke complicatie is een darmperforatie.
Dyskinesie-hyperpyrexiesyndroom
Dyskinesieën als gevolg van de behandeling met levodopa kunnen in zeldzame gevallen dermate ernstig worden dat ze zich continu en over het hele lichaam voordoen. Mogelijke gevolgen zijn dehydratie en rabdomyolyse. De behandeling bestaat uit geleidelijk verminderen van de dopaminerge medicatie. Diepe hersenstimulatie kan overwogen worden.
Complicaties van levodopa-carbidopa intestinale gel
Bij deze behandeling wordt levodopa continu afgegeven in het jejunum via een percutane endoscopische gastrostomie. Complicaties komen frequent voor en kunnen gerelateerd zijn aan de procedure (gastrostomie), het infusiesysteem en de medicatie zelf. Voorbeelden zijn dislocatie van de katheter of bezoarvorming rondom de katheter en daardoor darmobstructie. Buikpijn, flatulentie en obstipatie zijn de voornaamste symptomen.
Richtlijnen diagnostiek
Naar Samenvatting ›Anamnese
Naar Samenvatting ›Vraag naar:
- Aard van de klachten:
- tremor, verminderde kracht, onhandigheid, stijfheid, pijn
- verandering in mimiek en/of spraak
- Duur en beloop van tremor, stijfheid en loopproblemen; eenzijdig of symmetrisch begin
- Ernst van de klachten en gevolgen voor het dagelijks leven:
- verstoorde fijne motoriek (problemen met schrijven, vastmaken van knoopjes of tandenpoetsen)
- verhoogde valneiging
- gevolgen voor het werk
- Gerelateerde klachten en symptomen (zie Klinisch beeld):
- verminderd reukvermogen
- vermoeidheid
- depressieve klachten
- cognitieve stoornissen
- autonome stoornissen
- Gebruik van geneesmiddelen die reversibel parkinsonisme kunnen veroorzaken (antipsychotica, anti-emetica, SSRI’s, venlafaxine, bupropion, valproïnezuur)
- Familieanamnese
Lichamelijk onderzoek
Naar Samenvatting ›- Tremor:
- laat de patiënt de handen en armen ontspannen neerleggen op tafel of in de schoot
- laat de patiënt een beweging uitvoeren (bijvoorbeeld een glas water drinken of overschenken)
- laat de patiënt de armen vervolgens uitstrekken tegen de zwaartekracht in en uitgestrekt voor zich uit houden
- beoordeel of de tremor verandert bij een cognitieve taak, zoals rekenen of terugtellen
- Looppatroon: laat de patiënt een stukje lopen, let op snelheid, gangspoor, paslengte, armzwaai
- Evenwicht: let op houdingsinstabiliteit bij opstaan, stilstaan, vooroverbuigen, lopen, draaien
- Motoriek:
- vraag patiënt een zin te schrijven, let op micrografie (onregelmatig patroon tijdens het schrijven)
- Tonus en kracht van arm- en beenspieren bij passieve en actieve bewegingen, let op rigiditeit en tandradfenomeen (schokkende beweging bij passieve beweging van een gewricht)
- Houding en gezichtsuitdrukking, mimiek
- Spraak
Op indicatie
Verricht overig neurologisch onderzoek bij aanwijzingen voor andere neurologische aandoeningen.
Looppatroon bij de ziekte van Parkinson
De beschrijving van het begrip gangspoor en het looppatroon bij de ziekte van Parkinson zijn ontleend aan een leerboek en een overzichtsartikel waarin de verschillende looppatronen en de onderliggende aandoeningen worden besproken.
Houdingsinstabiliteit
Ter beoordeling van de houdingsstabiliteit (en het risico van vallen) bij patiënten met de ziekte van Parkinson worden verschillende diagnostische onderzoeken beschreven. Een hiervan is de retropulsietest, waarbij de patiënt met een onverwachte, snelle ruk aan de schouders achterwaarts wordt getrokken. De uitslag is afwijkend als de patiënt > 2 stappen achteruit zet of ondersteund moet worden om het evenwicht te bewaren. Er zijn geen onderzoeken gevonden naar de diagnostische waarde in de eerste lijn van de retropulsietest voor de ziekte van Parkinson.
Evaluatie
Naar Samenvatting ›Symptomen die wijzen op een hypokinetisch-rigide syndroom
Traag bewegen (bradykinesie) plus ≥ 1 van de volgende symptomen:
- rigiditeit
- rusttremor
Symptomen die de diagnose ‘ziekte van Parkinson’ ondersteunen (zie ook tabel 1)
- Houdingsinstabiliteit zonder aanwijzingen voor visuele, vestibulaire, cerebellaire of proprioceptieve stoornis
- Unilateraal begin en blijvend asymmetrisch beeld ten nadele van de kant waar de ziekte begon
- Langzaam progressief beloop
- Afname van het reukvermogen die niet anderszins te verklaren is
- Traag looppatroon met verminderde armzwaai
- Voorovergebogen houding van de romp
- Zachte, monotone spraak
Differentiaaldiagnose
Hypokinetisch-rigide syndroom
De ziekte van Parkinson is de meest voorkomende oorzaak van een hypokinetisch-rigide syndroom, maar dit syndroom kan ook, zij het veel minder vaak, worden veroorzaakt door andere aandoeningen:
- atypisch parkinsonisme
- secundair parkinsonisme (onder andere medicamenteus (anti-emetica, antipsychotica) en vasculair, zie tabel d1)
Tremor
- Kenmerkend voor de ziekte van Parkinson is een rusttremor die toeneemt bij het uitvoeren van een cognitieve taak.
- Voor de differentiaaldiagnose bij andere typen tremoren, bijvoorbeeld een bewegingstremor, zie NHG-Behandelrichtlijn Essentiële tremor.
Richtlijnen beleid bij vermoeden van hypokinetisch-rigide syndroom
Naar Samenvatting ›Voorlichting en advies bij hypokinetisch-rigide syndroom
Naar Samenvatting ›- Stop of verander indien mogelijk de medicatie bij een vermoeden dat het syndroom veroorzaakt wordt door medicatie (antipsychotica, anti-emetica). Overleg zo nodig met de neuroloog of behandelend specialist.
- Leg in dat geval aan de patiënt uit dat medicamenteus‐geïnduceerd parkinsonisme weken tot maanden na het staken van het middel kan blijven bestaan.
Consultatie en verwijzing bij hypokinetisch-rigide syndroom
Naar Samenvatting ›Verwijs de overige patiënten binnen 6 weken naar een (bij voorkeur in bewegingsstoornissen gespecialiseerde) neuroloog voor diagnostiek en behandeling.
De diagnose ‘ziekte van Parkinson’ of ‘parkinsonisme' kan in de beginfase lastig te stellen zijn. Er zijn geen behandelingen die de aandoening kunnen genezen of het beloop kunnen vertragen, maar toch hebben patiënten vaak behoefte aan duidelijkheid over diagnose, beleid en prognose, en over aandoeningen en functiebeperkingen die met de ziekte gerelateerd zijn. De diagnose ‘ziekte van Parkinson’ of ‘parkinsonisme' wordt door de neuroloog gesteld.
Richtlijnen beleid bij ziekte van Parkinson
Naar Samenvatting ›Algemeen
Naar Samenvatting ›- De ziekte van Parkinson heeft grote invloed op de ervaren kwaliteit van leven
- De behandeling gebeurt bij voorkeur door een samenwerkingsverband van neuroloog, huisarts, paramedici en parkinsonverpleegkundige of verpleegkundig specialist (zie Organisatie van zorg).
- In eerste instantie berusten de coördinatie en de zorgverlening vooral bij de neuroloog en de parkinsonverpleegkundige of verpleegkundig specialist; in het eindstadium zal dit naar de huisarts verschuiven.
Rol van de huisarts
Naar Samenvatting ›- Stem de contactfrequentie af op de behoefte van de patiënt en diens naasten, op de fase en ernst van de ziekte en op bijkomende problemen of aandoeningen.
- De neuroloog is hoofdbehandelaar. Het moet duidelijk zijn wie verantwoordelijk is voor welk deel van de zorg en voor de patiënt moet duidelijk zijn wie het aanspreekpunt is bij problemen (zie Organisatie van zorg).
- De huisarts kan een rol hebben bij:
- signaleren van bijwerkingen en van veranderingen in effect of gebruik van de medicatie. Dit kan aanleiding zijn om (vervroegd) de neuroloog te consulteren (zie Medicamenteuze behandeling).
- signaleren en eventueel diagnosticeren en behandelen van (niet-motorische) symptomen (of de huisarts verwijst hiervoor naar de neuroloog of overige zorgverleners) (zie Beleid bij niet-motorische symptomen en aandoeningen)
- intensiveren en coördineren van zorg in de terminale fase (zie Terminale fase)
- signaleren van psychosociale problemen bij de patiënt en/of diens partner of mantelzorger (zie Psychosociale problematiek)
- De ziekte van Parkinson gaat vaak gepaard met polyfarmacie en comorbiditeit, en in het beloop van de ziekte ontstaan vaak ook niet-motorische symptomen of aandoeningen. Het bevordert de kwaliteit en continuïteit van de zorg als de huisarts aandacht besteedt aan deze aspecten.
- Aandacht voor deze aspecten maakt het mogelijk om vroegtijdig problemen te signaleren en het beleid zo nodig aan te passen in samenwerking met de neuroloog of parkinsonverpleegkundige. Vaak hebben huisartsen inzicht in de thuissituatie en in de draaglast en draagkracht van de mantelzorger.
- Bepaal de contactfrequentie aan de hand van de behoefte van de patiënt en diens naasten, en besteed aandacht aan bijkomende problemen of aandoeningen.
Voorlichting en advies
Naar Samenvatting ›Onderstaande aandachtspunten gelden in eerste instantie vooral voor de neuroloog, maar kunnen in bepaalde fasen van de ziekte ook relevant zijn voor de huisarts.
Bewegen
Naar Samenvatting ›Blijven bewegen heeft een gunstige invloed op de motorische symptomen en kwaliteit van leven. Stimuleer de patiënt actief te blijven. Verwijs zo nodig naar een fysio- of oefentherapeut voor begeleiding.
- De Multidisciplinaire richtlijn Ziekte van Parkinson adviseert patiënten te blijven bewegen. Dit dient onder andere de volgende doelen:
- fysieke en mentale fitheid bevorderen en achteruitgang voorkomen
- cognitieve achteruitgang zo mogelijk afremmen
- obstipatie voorkomen
- valrisico reduceren
- Meer bewegen lijkt niet te leiden tot meer valincidenten. Vanuit een oogpunt van veiligheid lijkt er dus geen bezwaar te zijn tegen interventieprogramma’s gericht op reductie van het valrisico.
- Een recente netwerkmeta-analyse van 156 RCT’s (n = 7939) laat zien dat verschillende beweeginterventies, zoals aquatraining, duurtraining, danstherapie en balans- en evenwichttraining, op korte termijn de motorische symptomen bij de ziekte van Parkinson verminderen en de kwaliteit van leven bevorderen.
Gewichtsverlies
Naar Samenvatting ›Onbedoeld gewichtsverlies is een continu, progressief proces dat soms al enkele jaren voor de diagnose ‘ziekte van Parkinson’ begint. Vaak zullen een diëtist (energie- en eiwitverrijkte voeding, dieetvoeding) en/of een logopedist (bij slikproblemen) zijn ingeschakeld.
- De precieze oorzaak van gewichtsverlies bij de ziekte van Parkinson is nog onduidelijk. De oorzaak is niet alleen een verminderde energie-inname. Andere mogelijk bijdragende factoren zijn ernstige dyskinesieën (waardoor verhoogd energieverbruik), cognitieve en gedragsstoornissen, depressie, angst voor verslikken bij slikstoornissen, bijwerkingen van de medicatie, reukstoornissen en mogelijk veranderingen in de energiehuishouding.
- De neuroloog of parkinsonverpleegkundige zal veelal energie- en eiwitverrijkte voeding adviseren, eventueel aangevuld met dieetvoeding. Ook voldoende beweging is van belang ter bevordering van de spierfunctionaliteit.
- De neuroloog zal zo vroeg mogelijk een diëtist inschakelen om de inname van en behoefte aan voeding te beoordelen. Dit moet in ieder geval gebeuren bij ongewenst gewichtsverlies (> 5% binnen 1 maand of > 10% binnen 6 maanden). Een op maat gesneden voedingsadvies kan conditieverlies en complicaties zoals decubitus helpen voorkomen. Dieetadviezen kunnen ook betrekking hebben op de inname en werkzaamheid van medicatie, zodat responsfluctuaties die samenhangen met het voedingspatroon worden voorkomen.
- Bij onbedoeld gewichtsverlies door mogelijke slikproblemen zal de neuroloog verwijzen naar de logopedist.
Valrisico
Naar Samenvatting ›- De ziekte van Parkinson leidt tot een verhoogd valrisico dat vaak multifactorieel bepaald is (bijvoorbeeld gestoorde houdingsreflexen, orthostatische hypotensie, freezing, ondervoeding).
- Verwijs (indien dit nog niet is gebeurd) bij een verhoogd valrisico of angst om te vallen naar:
- een oefen- of fysiotherapeut met expertise op het gebied van de ziekte van Parkinson
- een ergotherapeut met expertise op het gebied van de ziekte van Parkinson voor adviezen inzake verlaging van het valrisico en aanpassingen en hulpmiddelen in de thuissituatie.
- Voor verdere adviezen over valpreventie, zie Multidisciplinaire richtlijn Preventie van valincidenten bij ouderen.
Psychosociale problematiek
Naar Samenvatting ›- De volgende psychosociale problemen komen vaak voor bij patiënten en bij hun partners:
- ziekteacceptatie
- veranderingen in de relatie, bijvoorbeeld op het gebied van gelijkwaardigheid en seksuele relatie
- angst voor medicatie
- onzekerheid over de toekomst
- veranderingen die samenhangen met cognitieve problemen en/of gedragsveranderingen
- Verwijs zo nodig voor verdere begeleiding of behandeling naar een psycholoog of maatschappelijk werker (zie Consultatie en verwijzing).
Maatschappelijk functioneren
Naar Samenvatting ›Aandachtspunten zijn:
- sociale situatie
- woonomstandigheden en -voorzieningen
- dagbesteding
- huishouding
- arbeidsparticipatie
- De neuroloog wijst de patiënt bij de diagnose op de morele plicht om de aandoening bij het CBR te melden via een gezondheidsverklaring. Met name stoornissen in de aandacht en de visuoconstructieve verwerking (het combineren van perceptie, geheugen en planning met een motorische respons) kunnen de rijgeschiktheid nadelig beïnvloeden.
- De Regeling eisen geschiktheid 2000 acht mensen met de ziekte van Parkinson rijgeschikt voor groep 1 (motorfiets, auto en auto met aanhanger), als ze geen relevante lichamelijke of geestelijke functiebeperkingen hebben die interfereren met de geschiktheid tot het besturen van motorrijtuigen.
- De Regeling eisen geschiktheid 2000 schaart dopaminerge medicatie (levodopa, dopamineagonisten) onder geneesmiddelen uit categorie II. Deze middelen hebben een licht tot matig negatieve invloed op de rijvaardigheid. Aanbevolen wordt om de eerste dagen van het gebruik niet auto te rijden.
- Als bijwerking van dopaminerge medicatie kunnen plotselinge slaapaanvallen optreden. Autorijden wordt ontraden als deze bijwerking optreedt (zie rijveiligmetmedicijnen.nl, geraadpleegd 8 januari 2024).
- Van alle parkinsonpatiënten is 46% binnen 5 jaar na de diagnose gestopt met werken, 82% stopt binnen 10 jaar. Mediaan werken parkinsonpatiënten in Nederland nog 8,0 jaar vanaf het moment van diagnose.
- De meest voorkomende symptomen die arbeidsparticipatie belemmeren zijn vermoeidheid, traagheid van bewegen, aandacht- en concentratieproblemen, stijfheid, beven of trillen, verminderde kracht, beperkingen in loopvaardigheid, fijnmotorische vaardigheden, spraak- en balansproblemen.
- Werkgerelateerde activiteiten die als meest belemmerend ervaren worden, zijn:
- gebruiken van de handen (bijvoorbeeld bij computergebruik)
- uitvoeren van meerdere taken tegelijk (zoals notities maken bij een overleg)
- omgaan met stress of werkdruk
- praten en converseren in groepen
- Voorlichting aan directe collega’s over de ziekte en de ziekteverschijnselen levert een belangrijke bijdrage succesvolle arbeidsparticipatie. Ook is het zinvol de bedrijfsarts in te schakelen, of bij zelfstandig ondernemers de medisch adviseur van de verzekeraar, ook als er (nog) geen sprake is van arbeidsongeschiktheid.
- Verwijs de patiënt voor aanvullende informatie eventueel naar Parkinson&Werk.
Mantelzorg
Naar Samenvatting ›- Naarmate de ziekte vordert, kan de zorg voor de patiënt veel van de mantelzorgers vragen.
- Andere factoren die belastend zijn voor de mantelzorger en andere naasten, zijn onzekerheid over de toekomst, eventuele verandering van karakter en een andere rol in de relatie (zie LHV-toolkit Mantelzorg in de huisartsenpraktijk en de website van de Parkinson Vereniging).
Proactieve zorgplanning
Naar Samenvatting ›- De hoofdbehandelaar (meestal de neuroloog) bespreekt tijdig en met enige regelmaat de doelen en voorkeuren voor toekomstige behandeling en zorg met patiënt en diens naaste(n).
- Ook de huisarts kan een rol hebben, zeker bij gevorderde ziekte en co-morbiditeit.
- Houd er rekening mee dat patiënten in het beloop van de ziekte vaak cognitieve stoornissen of ernstige spraakproblemen ontwikkelen.
- Het is van belang dat alle betrokken zorgverleners op de hoogte zijn van de afspraken.
- Bespreek ook de optie om de wensen van de patiënt vast te leggen in een volmacht, levenstestament of wilsverklaring (zie Toolkit Advance Care Planning met betrekking tot het levenseinde, IKNL-richtlijn Proactieve zorgplanning en NHG-Standaard Dementie).
Thuisarts
Naar Samenvatting ›- Verwijs naar de informatie op thuisarts.nl. De informatie op Thuisarts is gebaseerd op deze NHG-Standaard.
- Verwijs eventueel naar de website van de Parkinson Vereniging.
Niet-medicamenteuze behandeling
Naar Samenvatting ›Voor een overzicht van de bij de behandeling betrokken paramedici en verwijsindicaties, zie Consultatie en verwijzing.
Medicamenteuze behandeling
Naar Samenvatting ›- De neuroloog start en controleert de medicamenteuze behandeling, en bepaalt de keuze van de medicatie in samenspraak met de patiënt.
- De keuze van parkinsonmedicatie is afhankelijk van onder andere de leeftijd, klinische verschijnselen en levensverwachting:
- bij patiënten met ziekteverschijnselen die de kwaliteit van leven beïnvloeden wordt vroeg in de ziekte gestart met een levodopapreparaat (levodopa in combinatie met een decarboxylaseremmer, zoals levodopa/carbidopa of levodopa/benserazide).
- bij patiënten < 40 jaar kan worden gestart met levodopasparende therapie (MAO-B-remmer, dopamineagonist) in plaats van levodopa, in verband met een verhoogd risico op dyskinesieën (uiteindelijke responsfluctuaties).
- indien bij progressie van het ziektebeeld responsfluctuaties optreden, kunnen doseringen worden aangepast en andere middelen (dopamineagonisten, MAO-B-remmers, COMT-remmers, amantadine) worden toegevoegd.
Keuze van geneesmiddelen
- Voor de meest gebruikte geneesmiddelen bij motorische symptomen, met hun belangrijkste bijwerkingen en interacties, zie tabel d3.
- De neuroloog kan kiezen voor een levodopapreparaat of voor dopaminesparende behandeling met een MAO-B remmer of dopamineagonist.
Levodopa
- Levodopapreparaten hebben het krachtigste effect en zijn aangetoond veilig. Na meerdere jaren gebruik kunnen dyskinesieën en responsfluctuaties ontstaan.
- Uitstel van een behandeling met levodopa verlaagt niet de kans op dyskinesieën maar wel de kwaliteit van leven. De duur van de ziekte, niet de duur van de behandeling lijkt het ontstaan van motorische complicaties te bepalen. Een zo laag mogelijke dosering levodopa verlaagt het risico op levodopageïnduceerde motorische responsfluctuaties.
- Responsfluctuaties zijn vooral geassocieerd met levodopapreparaten vanwege hun kortere halfwaardetijd. Voordat nieuwe medicatie toegevoegd wordt, zal eerst gekeken worden of aanpassen van de dosisintervallen een verbetering oplevert, evenals optimaliseren van de resorptie van levodopa in het geval van obstipatie.
Dopaminesparende behandeling
- Bij een begin van de ziekte < 40 jaar is de kans op het ontwikkelen van dyskinesieën groter dan bij een later begin. Bij deze patiënten kan dopaminesparende therapie (MAO-B remmer, dopamineagonist) overwogen worden.
- Deze middelen zijn minder effectief en hebben een grotere kans op bijwerkingen (hallucinaties, hypotensie, impulscontrolestoornis, toegenomen slaperigheid). De keuze is afhankelijk van de kenmerken en voorkeuren van de patiënt.
|
Groep (preparaat) |
Werking |
Bijwerkingen |
Interacties en contra-indicaties |
|
Levodopa (levodopa/carbidopa, levodopa/benserazide) |
Levodopa passeert de bloed-hersenbarrière, waarna het wordt omgezet in dopamine Een perifere decarboxylaseremmer (carbidopa, benserazide) verhindert de omzetting van levodopa tot dopamine buiten de bloed-hersenbarrière en verlaagt de kans op ‘perifere’ bijwerkingen (hypotensie, misselijkheid) |
|
|
|
Dopamineagonisten (pramipexol, ropinirol, rotigotine) |
Stimuleert dopaminerge receptoren in het corpus striatum |
Onder andere misselijkheid, braken, duizeligheid, vermoeidheid, obstipatie, wazig zien, verwardheid, hallucinaties, slapeloosheid, plotselinge slaapaanvallen, oedeem, impulscontrolestoornis |
Interactie met dopamineantagonisten*: vermindering van de werkzaamheid |
|
MAO-B-remmers (selegiline, rasagiline, safinamide) |
Selectieve, irreversibele remmer van MAO-B, dat dopamine in de hersenen afbreekt |
|
|
|
COMT-remmers (entacapon) |
Remt de omzetting van levodopa tot 3-methoxy-4-hydroxy-L-fenylalanine. |
Onder andere dyskinesieën, misselijkheid en roodbruine verkleuring van de urine, dystonie, hyperkinesie, diarree, buikpijn, droge mond, braken, obstipatie, ischemische hartaandoeningen, slapeloosheid, abnormaal dromen, hallucinaties, verwardheid, duizeligheid, vermoeidheid, overmatig zweten, vallen |
Interactie met ijzerpreparaten: bij gelijktijdige inname neemt de resorptie af door vorming van niet-oplosbaar complex, houd toedieningsinterval zo groot mogelijk (≥ 2-3 uur) |
|
NMDA-antagonisten (amantadine) |
Toename afgifte en werking dopamine |
Onder andere enkeloedeem, livedo reticularis, hallucinaties, verminderde eetlust, slapeloosheid, angst, hoofdpijn, duizeligheid, agitatie, hartkloppingen, obstipatie |
Interactie met dopamineantagonisten*: vermindering van de werkzaamheid |
|
MAO = monoamineoxidase. SSRI = selectieve seroptonineheropnameremmer; TCA = tricyclisch antidepressivum; COMT = catechol-O-methyltransferase; NMDA = N-methyl-D-aspartaat. * Dopamineantagonisten: antipsychotica, metoclopramide, pethidine, tramadol en dextromethorfan (hoestdrank) Bronnen: Farmacotherapeutisch Kompas, KNMP Kennisbank (geraadpleegd 1 december 2022). |
|||
Mucuna pruriens
De Multidisciplinaire richtlijn Ziekte van Parkinson beveelt gebruik van de fluweelboon of jeukboon (Mucuna pruriens) niet aan.
Mucuna pruriens is een snelgroeiende plant. De peulvruchten bevatten levodopa en worden in de traditionele Indiase geneeskunst gebruikt voor stoornissen van het centrale zenuwstelsel. Het bewijs voor het effect op kwaliteit van leven, parkinsonspecifieke symptomen en motorische en niet-motorische klachten is schaars. Er is 1 RCT uitgevoerd en deze liet geen significant verschil in langetermijneffect zien tussen de behandelgroep en de placebogroep. De samenstelling van preparaten met Mucuna pruriens is niet altijd duidelijk en kan variëren.
Geavanceerde behandeling
Naar Samenvatting ›- Bij responsfluctuaties die met orale medicatie onvoldoende onder controle zijn, kan de neuroloog kiezen voor apomorfine subcutaan of intraduodenale levodopa/carbidopa.
- Bij een therapieresistente tremor kan diepe hersenstimulatie overwogen worden.
- Voor meer informatie, raadpleeg de keuzekaarten bij de Multidisciplinaire richtlijn Ziekte van Parkinson. Deze keuzekaarten zijn ook te vinden op Thuisarts.
Apomorfine
Apomorfine is een niet-selectieve dopamineagonist met voornamelijk affiniteit voor dopamine D2-receptoren. Bij responsfluctuaties kan apomorfine snel worden toegediend via een subcutane pen of continu via een subcutane pomp. Vanwege de complexiteit van de behandeling en de eventuele bijwerkingen gebeurt de instelling op de medicatie (poli)klinisch in een gespecialiseerd centrum.
Intraduodenale infusie
Levodopa/carbidopa of levodopa/carbidopa/entacapon worden direct in het duodenum afgegeven als intestinale gel via een jejunale sonde. Omdat de levodopa direct in het jejunum of duodenum terechtkomt, zal een vertraagde maagontlediging minder invloed hebben op de absorptie in de darm dan bij orale inname. Er is een risico op complicaties door het gebruik van een PEG-sonde (lekkage, verstopping).
Diepe hersenstimulatie (DBS)
Bij DBS worden 1 of (meestal) 2 elektroden stereotactisch in de hersenen geïmplanteerd die worden aangestuurd door een onder de huid geplaatste interne neurostimulator. DBS wordt sinds 1987 (inmiddels routinematig) toegepast bij de ziekte van Parkinson. Chirurgische doelgebieden zijn de nucleus subthalamicus, de globus pallidus pars interna of ventrolaterale kern van de thalamus. De keuze hangt af van verschillende factoren, waaronder overheersende symptomen. Afhankelijk van het doelgebied kan bij DBS vaak de orale dopaminerge medicatie verlaagd worden. Afhankelijk van het doelgebied kan bij DBS vaak de orale dopaminerge medicatie verlaagd worden.
Aandachtspunten voor de huisarts
Naar Samenvatting ›- De huisarts heeft een rol bij het signaleren van bijwerkingen en veranderingen in de effectiviteit of het gebruik van de medicatie. Adviseer (vervroegd) de neuroloog te consulteren bij:
- bijwerkingen of veranderingen in het gebruik van parkinsonmedicatie
- veranderingen in de werkzaamheid van parkinsonmedicatie, zoals responsfluctuaties (peak-dose dyskinesieën, off-fasen)
- Klachten kort na de start of dosiswijziging van medicatie kunnen op bijwerkingen duiden (zie tabel d3).
- Bij sommige patiënten zal de symptoombestrijding tekortschieten bij progressie van de ziekte doordat de dopaminerge medicatie sneller is uitgewerkt.
- Wees alert op impulscontrolestoornissen als gevolg van (overmatig gebruik van) dopaminerge medicatie, bijvoorbeeld verslaving aan gokken, seks, winkelen of eten; verwijs hiervoor naar de neuroloog (zie Impulscontrolestoornissen).
- Wees extra alert op vroege verschijnselen van een dopaminedysregulatiesyndroom bij snelle dosisstijgingen en bij verzoeken om extra dopaminerge medicatie (zie Dopaminedysregulatiesyndroom (DDS)).
- Zorg dat dopaminerge medicatie indien mogelijk wordt gecontinueerd, ook rondom operaties en in de terminale fase. (Abrupt) staken van dopaminerge medicatie kan leiden tot rigiditeit en tremoren, en tot het maligne levodopa-onttrekkingssyndroom (zie Maligne levodopa-onttrekkingssyndroom).
Niet-motorische symptomen en aandoeningen
Naar Samenvatting ›- Niet-motorische klachten komen veel voor en hun intensiteit neemt toe met het vorderen van de ziekte; ze kunnen in een latere fase de voorgrond komen te staan en het functioneren van de patiënt ernstig belemmeren.
- De huisarts heeft een rol in het signaleren van deze klachten, zeker als de patiënt zelf de relatie met de ziekte van Parkinson nog niet heeft gelegd.
- Behandeling gebeurt meestal door of in overleg met de neuroloog.
Apathie
Naar Samenvatting ›- Er kan onderscheid worden gemaakt tussen geïsoleerde apathie en apathie door een stemmingsstoornis en/of cognitieve achteruitgang. Bij geïsoleerde apathie is sprake van passiviteit, desinteresse en affectvervlakking, maar de patiënt kan plezier beleven en is niet somber.
- Apathie kan ook een bijwerking zijn van medicatie, of juist van een tekort aan dopaminerge medicatie.
- De neuroloog of de parkinsonverpleegkundige zal bij apathie een interventie adviseren gericht op motivatie en activatie (bijvoorbeeld dagbesteding of ergotherapie).
Voor de onderbouwing van dit detail, zie Multidisciplinaire richtlijn Ziekte van Parkinson.
- Apathie komt voor bij 40% van de patiënten met de ziekte van Parkinson. Kenmerkend zijn gebrek aan motivatie, affectvervlakking, verminderd doelgericht gedrag en verminderde cognitieve activiteit.
- Naasten verwarren apathie vaak met depressie, zij klagen erover dat de patiënt passief en ongeïnteresseerd is, en geen initiatief meer neemt. Bij 'zuivere apathie' zal de patiënt bij navraag depressieve klachten echter ontkennen en zeggen best plezier te kunnen beleven, bijvoorbeeld bij bezoek van de kleinkinderen. Ook zal de patiënt ontkennen dat hij/zij zich verveelt – zelfs al zit hij de hele dag op de bank niets te doen.
- Apathie kan ook onderdeel zijn van een ander syndroom, zoals een depressieve stoornis of cognitieve achteruitgang, een bijwerking van de medicatie of een symptoom van een dopamineagonistonttrekkingsyndroom. Dit laatste ontstaat door snelle afbouw van een dopamineagonist, bijvoorbeeld na de start van DBS.
Depressie
Naar Samenvatting ›- Voor diagnostiek, zie NHG-Standaard Depressie.
- Beoordeel de patiënt in de on-fase, want symptomen zoals motorische vertraging, mimiekarmoede en traagheid in het denken kunnen overlappen met symptomen van de ziekte van Parkinson.
- De diagnostiek van depressie kan worden bemoeilijkt door een combinatie met cognitieve stoornissen.
- Overleg met of verwijs naar de neuroloog indien stemmingsklachten optreden na verandering van de parkinsonmedicatie of tijdens off-fasen (waarin de patiënt merkt dat de medicatie onvoldoende of niet werkt); aanpassing van de dopaminerge medicatie kan nodig zijn.
- Als de patiënt nog geen dopaminerge middelen gebruikt, kan het starten van deze middelen depressieve symptomen verminderen.
- Voor het beleid bij depressie, zie NHG-Standaard Depressie.
- geef de voorkeur aan SSRI’s met een korte halfwaardetijd, zoals (es)citalopram of sertraline, boven SSRI’s met een lange halfwaardetijd, zoals fluoxetine, want laatstgenoemde geven een verhoogd risico op extrapiramidale bijwerkingen.
- bij gebruik van MAO-B-remmers zijn SSRI’s en tricyclische antidepressiva gecontra-indiceerd vanwege de kans op een serotoninesyndroom.
Voor de onderbouwing van dit detail, zie Multidisciplinaire richtlijn Ziekte van Parkinson.
- Klinisch relevante depressieve symptomen komen voor bij ongeveer 30% van de patiënten met de ziekte van Parkinson. Vaak ontstaat de depressie tijdens het beloop van de ziekte, maar bij ongeveer 10% is een depressie al 3 jaar voor de diagnose aanwezig (geweest).
- Omdat de bewijskracht voor zowel niet-medicamenteuze als medicamenteuze behandelingen laag is, zijn de aanbevelingen in de MDR gebaseerd op expert opinion en op de geldende algemene richtlijnen bij depressie. De MDR adviseert bij een ernstige depressie de keuze tussen een SSRI of TCA te baseren op de symptomen en het bijwerkingenprofiel.
- Volgens de NHG-Standaard Depressie is een TCA niet langer het middel van eerste keus, vooral vanwege de bijwerkingen. Wij bevelen aan om hierbij aan te sluiten voor de behandeling van depressie bij de ziekte van Parkinson.
Dementie
Naar Samenvatting ›Verwijs naar de neuroloog bij twijfel over de aan- of afwezigheid van cognitieve stoornissen.
Voor de onderbouwing van dit detail, zie Multidisciplinaire richtlijn Ziekte van Parkinson.
- Naar schatting 48-80% van de patiënten met de ziekte van Parkinson ontwikkelt dementie in het beloop van de ziekte. Het risico neemt toe met leeftijd en ziekteduur.
- Soms heeft de patiënt bij diagnose al cognitieve stoornissen. Dit zijn meestal stoornissen in aandacht, tempo en executief functioneren. Ook stoornissen in het geheugen en de visueel-ruimtelijke oriëntatie komen echter voor.
- Bij Lewy body-dementie gaan de kernsymptomen daarvan (wanen of hallucinaties, vallen, orthostatische hypotensie) vooraf aan de motorische stoornissen.
Diagnostiek
- De diagnose ‘dementie bij ziekte van Parkinson’ berust op 4 criteria:
- diagnose ‘ziekte van Parkinson’
- de cognitieve stoornissen zijn progressief (globale achteruitgang, MMSE < 26)
- de cognitieve stoornissen beïnvloeden het dagelijks functioneren
- er zijn cognitieve stoornissen in ≥ 2 van de 4 domeinen geheugen, aandacht, executieve functies, en visuoconstructieve en visuospatiële functies)
- Aanwezigheid van ≥ 1 van de volgende symptomen maakt de diagnose ‘dementie’ waarschijnlijker:
- visuele hallucinaties
- wanen
- agitatie
- overmatige slaperigheid overdag
- depressieve symptomen
- angst of apathie
Angst
Naar Samenvatting ›Bij patiënten met de ziekte van Parkinson kan sprake zijn van:
- angst in het kader van een andere aandoening of symptoom, bijvoorbeeld een depressie, cognitieve stoornissen, hallucinaties
- verhoogde stressgevoeligheid van parkinsonpatiënten kan een rol spelen bij deze klachten
- zie NHG-Standaard Angst voor diagnostiek en behandeling.
- parkinsonspecifieke angststoornissen, zoals:
- angst tijdens het uitwerken van de dopaminerge medicatie (wearing-off anxiety) en tijdens off-fasen
- situatieve angst, bijvoorbeeld tijdens activiteiten waarbij er een valrisico bestaat.
Overleg of verwijs naar de neuroloog bij parkinsonspecifieke angststoornissen.
Voor de onderbouwing van dit detail, zie Multidisciplinaire richtlijn Ziekte van Parkinson.
- Van alle patiënten met de ziekte van Parkinson voldoet 31% aan de DSM-5-criteria voor een angststoornis: generaliseerde angststoornis (14%), sociale angststoornis (14%) en/of paniekstoornis (7%).
- Daarnaast is er ook een groep patiënten bij wie de diagnose ‘angststoornis ten gevolge van een somatische aandoening’ passender is. Tot deze angststoornissen behoren ook de parkinsonspecifieke angststoornissen.
- Ten tijde van de ontwikkeling van de MDR was er geen onderzoek gepubliceerd naar de effectiviteit van medicamenteuze behandeling van angstklachten bij de ziekte van Parkinson. Derhalve verwijzen wij voor de behandeling naar de NHG-Standaard Angst.
Hallucinaties en wanen
Naar Samenvatting ›- De oorzaak van wanen en (visuele) hallucinaties is meestal een delier; onderzoek mogelijke oorzaken (urineweginfectie, pneumonie, dehydratie, elektrolytstoornissen, hypoglykemie) en behandel deze (zie NHG-Standaard Delier).
- Beoordeel of visus en gehoor optimaal zijn gecorrigeerd.
- Overleg met de neuroloog over eventuele aanpassing van de parkinsonmedicatie.
- Verwijs naar de neuroloog bij beangstigende hallucinaties, indien aanpassing van de medicatie niet mogelijk of niet effectief is.
- De ziekte van Parkinson is een contra-indicatie voor klassieke antipsychotica zoals haloperidol en voor de atypische antipsychotica olanzapine en risperidon, vanwege de kans op toename van motorische symptomen.
Voor de onderbouwing van dit detail, zie Multidisciplinaire richtlijn Ziekte van Parkinson.
- Psychotische verschijnselen, met name hallucinaties en wanen, zijn veelvoorkomende bijwerkingen van dopaminerge medicatie, maar kunnen ook ontstaan zonder gebruik van medicatie of het gevolg zijn van een delier.
- Het is belangrijk dat patiënten en hun verzorgers zich ervan bewust zijn dat parkinsonmedicatie kan leiden tot psychotische verschijnselen. De aanwezigheid van deze symptomen moet bij elke (poliklinische)afspraak worden beoordeeld. Daarbij is het belangrijk om ook naasten te vragen of de patiënt tekenen vertoont van het ervaren van hallucinaties of wanen, omdat sommige patiënten zich hier zelf niet van bewust zijn.
- De aanbevelingen omtrent de behandeling zijn gebaseerd op de MDR. Gezien de kans op ernstige bijwerkingen en de noodzaak tot frequente bloedcontroles wordt aanbevolen om als huisarts geen clozapine te starten (zie ook NHG-Bijlage Voorzorgen bij patienten die clozapine gebruiken).
Impulscontrolestoornissen
Naar Samenvatting ›- Wees extra alert op impulscontrolestoornissen bij patiënten die dopaminerge medicatie gebruiken. Andere risicofactoren zijn:
- begin van de ziekte op jonge leeftijd
- mannelijk geslacht
- verslavingsgedrag in de voorgeschiedenis
- depressieve symptomen
- impulsief karakter
- Verwijs naar de neuroloog bij aanwijzingen voor een impulscontrolestoornis
Voor de onderbouwing van dit detail, zie Multidisciplinaire richtlijn Ziekte van Parkinson.
- Kenmerken geassocieerd met een verhoogd risico op een impulscontrolestoornis of dopaminedysregulatiesyndroom:
- ziekte van Parkinson op jonge leeftijd (< 45 jaar)
- mannelijk geslacht
- sensatiezoekende of impulsieve persoonlijkheidskenmerken
- alcoholmisbruik in de voorgeschiedenis of positieve familieanamnese voor alcoholmisbruik
- impulscontrolestoornis in de voorgeschiedenis
- gebruik van dopamineagonisten
- Gebruik van dopamineagonisten lijkt de grootste risicofactor voor een impulscontrolestoornis, maar ook andere anti-parkinsonmedicatie (inclusief levodopa) en zelfs DBS kan een risicofactor zijn.
- Schaamte is een beperkende factor bij de diagnostiek van impulscontrolestoornissen: patiënten en naasten vinden het lastig om over het onderwerp te spreken en behandelaren zijn er vaak onvoldoende alert op. Regelmatig worden de klachten door patiënt en/of naasten niet in verband gebracht met de ziekte of de medicatie.
- De behandeling bestaat uit educatie en aanpassen van de dopaminerge medicatie tot een niveau waarbij verbetering van de impulscontrolestoornis opweegt tegen mogelijke verslechtering van de motorische verschijnselen. Dit kan door het minderen of staken van een dopamineagonist, het omzetten van een dopamineagonist naar een levodopapreparaat en/of het verlagen van de dosering levodopa.
- Wanneer deze aanpak onvoldoende verbetering biedt, kan cognitieve gedragstherapie, naltrexon en amantadine (in geval van pathologisch gokken) overwogen worden.
Dopaminedysregulatiesyndroom (DDS)
Naar Samenvatting ›- Wees extra alert op vroege verschijnselen van DDS bij patiënten:
- bij wie de dosis dopaminerge medicatie plotseling snel toeneemt
- die in een on-fase (vaak zelfs met dyskinesieën) toch vragen om extra dopaminerge medicatie
- die zeer frequent extra dopaminerge escapemedicatie gebruiken vanwege subjectief ervaren off-fases
- Verwijs naar de neuroloog bij aanwijzingen voor DDS. De patiënt zal opnieuw ingesteld moeten worden op dopaminerge medicatie; het kan nodig zijn de medicatie blijvend gecontroleerd aan te bieden aan de patiënt.
Voor de onderbouwing van dit detail, zie Multidisciplinaire richtlijn Ziekte van Parkinson.
- De eerste stap in de behandeling van een DDS is het opnieuw instellen van de patiënt op een verantwoord schema van dopaminerge medicatie.
- Toegang tot extra medicatie of tot medicatie op tijden dat deze niet is voorgeschreven wordt voor de patiënt onmogelijk gemaakt.
- Om terugval te voorkomen kan het nodig zijn de dopaminerge medicatie blijvend gecontroleerd uit te reiken, bijvoorbeeld via een medicatiebox met tijdklok of via derden (thuiszorg of mantelzorger).
Slaapstoornissen
Naar Samenvatting ›- Slaapproblemen zijn vaak het gevolg van nachtelijke motorische onrust door nachtelijke off-symptomen zoals tremor, rigiditeit, akinesie, bradykinesie en dystonie. Andere mogelijke oorzaken:
- dyskinesieën
- REM-slaapgedragsstoornis (onvoldoende verslapping van de spieren tijdens de REM-slaap, zich uitend in complex motorisch en vocaal gedrag (het fysiek uitleven van een droom))
- restlesslegssyndroom
- nycturie
- nachtelijke pijn
- bijwerkingen van medicatie
- Slaperigheid overdag is vaak het gevolg van verstoorde nachtrust; het kan ook een bijwerking zijn van (met name dopamine-agonisten.)
- Overleg met de neuroloog over aanpassing van de medicatie bij aanwijzingen voor nachtelijke over- of onderdosering van medicatie.
- Geef voorlichting en advies (zie NHG-Standaard Slaapproblemen en slaapmiddelen).
- De neuroloog kan lichttherapie overwegen wanneer voorlichting en advies onvoldoende effectief zijn.
- Verwijs naar de neuroloog of naar een slaapcentrum bij vermoeden van een REM-slaapgedragsstoornis.
Voor de onderbouwing van dit detail, zie Multidisciplinaire richtlijn Ziekte van Parkinson.
- Naar schatting 70-90% van de patiënten met de ziekte van Parkinson ervaart slaapproblemen. Deze kunnen het gevolg zijn van de ziekte zelf of een bijwerking van de medicatie (zie tabel d3).
- Slaapproblemen kunnen optreden door nachtelijke off-symptomen (tremor, rigiditeit, akinesie, bradykinesie, dystonie), dyskinesieën, restlesslegssyndroom of REM-slaapgedragsstoornis.
- De REM-slaapgedragsstoornis wordt gekenmerkt door het verlies van spieratonie en de aanwezigheid van complex motorisch gedrag en vocale uitingen (praten, geluid maken, schreeuwen) tijdens de REM-slaap. Patiënten vertonen onrustige motorische activiteit, gerelateerd aan droomervaringen, in plaats van een fysiologische verslapping. Dit leidt soms tot verwondingen bij de patiënt zelf en soms bij de partner. Een REM-slaapstoornis kan erg hinderlijk zijn voor de partner.
- Slaapstoornissen bij de ziekte van Parkinson kunnen uitermate complex zijn en er zijn weinig goede onderzoeken, de behandeling berust vaak op klinische ervaring.
Pijn
Naar Samenvatting ›- Veelvoorkomende parkinsonspecifieke oorzaken van pijn zijn:
- verhoogde spierspanning
- houdingsproblemen, zoals vaak voorovergebogen staan
- neuropathische pijn
- Volg het beleid bij chronische pijn (zie NHG-Standaard Pijn), met de volgende ziektespecifieke aanbevelingen:
- pijnklachten die samenhangen met de on- en de off-fase kunnen vaak worden behandeld door het beter instellen van de parkinsonmedicatie; verwijs hiervoor naar de neuroloog
- als een opioïd geïndiceerd is, gaat de voorkeur uit naar sterkwerkende opioïden boven tramadol, vanwege anticholinerge bijwerkingen van tramadol.
Voor de onderbouwing van dit detail, zie Multidisciplinaire richtlijn Ziekte van Parkinson.Pijn is aanwezig bij 40-95% van de patiënten met de ziekte van Parkinson.
- Pijn kan het gevolg zijn van de ziekte zelf of van comorbiditeit en kan grote invloed hebben op het dagelijks functioneren.
- De veelgebruikte King’s Parkinson Disease Pain Scale onderscheidt 7 pijndomeinen:
- muskuloskeletale pijn (rond gewrichten)
- chronische pijn: centrale pijn (gegeneraliseerd, constant, dof) en viscerale pijn (gerelateerd aan een inwendig orgaan).
- fluctuatiegerelateerde pijn (door dyskinesieën, dystonie in off-fase of gegeneraliseerde pijn in off-fase).
- nachtelijke pijn (gerelateerd aan periodic limb movement disorder, restlesslegssyndroom of draaien)
- orofaciale pijn (door kauwen, nachtelijk tandenknarsen of burning mouth syndrome).
- verkleuring, oedeem of zwelling (brandende pijn in benen gerelateerd aan zwelling van benen of gegeneraliseerde laag-abdominale pijn).
- radiculaire pijn
Vermoeidheid
Naar Samenvatting ›- Onderzoek of de vermoeidheid een andere oorzaak heeft dan primair de ziekte van Parkinson (slaapstoornis, depressie, ondervoeding, anemie) en behandel deze zo mogelijk.
- Geef uitleg over vermoeidheid.
- Richt de aandacht op verbetering van de conditie (zo nodig onder begeleiding van de fysiotherapeut), betere verdeling van het activiteitenpatroon en het inbouwen van voldoende rustmomenten
- Overweeg verwijzing naar een ergotherapeut voor energiemanagement als de vermoeidheidsklachten het uitvoeren van dagelijkse activiteiten ernstig bemoeilijken.
Voor de onderbouwing van dit detail, zie Multidisciplinaire richtlijn Ziekte van Parkinson.
- De prevalentie van vermoeidheid als symptoom van de ziekte van Parkinson is 33-70%, afhankelijk van meetmethode en patiëntenpopulatie.
- Vermoeidheid kan zich al vroeg in het beloop van de ziekte presenteren.
- Vermoeidheid gaat vaak samen met andere niet motorische symptomen, waaronder depressie, apathie en slaapstoornissen, maar staat op zichzelf en kan blijven bestaan indien bijvoorbeeld depressieve klachten of slaapstoornissen succesvol zijn behandeld.
- Er is nog weinig bekend over de pathofysiologie.
- De MDR noemt cognitieve gedragstherapie, multidisciplinaire revalidatie en rasagiline als behandelopties.
Autonome stoornissen
Naar Samenvatting ›- Bij slikproblemen en speekselverlies: verwijs naar een logopedist
- Bij obstipatie: zie NHG-Standaard Obstipatie.
- Bij mictieklachten: onderzoek onderliggende oorzaken zoals een urineweginfectie, vooral indien de klachten plotseling optreden.
- Bij urgeklachten: zie NHG-Standaard Incontinentie voor urine bij vrouwen en NHG-Standaard Mictieklachten bij mannen. Wees terughoudend met anticholinerge medicatie, vooral bij ouderen en patiënten met cognitieve achteruitgang.
- Adviezen bij nycturie: minder vochtinname, vermijd alcohol en koffie ’s avonds, zet urinaal en postoel naast bed, gebruik condoomkatheter (zie ook NHG-Standaard Mictieklachten bij mannen).
- Bij seksuele problemen: besteed aandacht aan belemmerende factoren en onderliggende oorzaken (depressie, medicatie, rigiditeit, hypokinesie, autonome disfunctie; zie NHG-Standaard Seksuele klachten). Bij hyperseksualiteit: wees alert op een impulscontrolestoornis.
- Bij orthostatische hypotensie: analyseer het geneesmiddelgebruik en stop of wijzig antihypertensiva. Geef leefstijladviezen (zie NHG-Standaard Duizeligheid) en overweeg verwijzing naar een klinisch geriater bij hinderlijke klachten.
- Overmatig transpireren kan optreden bij dopaminerge medicatie tijdens het begin van de off-fase. Wees alert op andere oorzaken (infectie, thyreotoxicose, overgang). Verwijs naar de neuroloog om eventuele aanpassing van de parkinsonmedicatie te bespreken
Voor de onderbouwing van dit detail, zie Multidisciplinaire richtlijn Ziekte van Parkinson.
- Autonome stoornissen komen veel voor bij de ziekte van Parkinson doordat ook de catecholaminerge neuronen van het autonome zenuwstelsel degenereren.
- Ook parkinsonmedicatie kan autonome bijwerkingen veroorzaken.
Speekselverlies
Speekselverlies komt voor bij 30-73% van de patiënten, ook al is de speekselproductie vaak afgenomen. De oorzaak is waarschijnlijk hypokinesie van het slikken: gebrekkige speekselbeheersing in combinatie met een voorovergebogen houding en onvoldoende sluiting van de mond.
- Een logopedist kan de ernst van het speekselverlies inschatten en technieken aanleren voor het regelmatig doorslikken van speeksel.
- Bij onvoldoende effect van logopedie kunnen atropine oogdruppels sublinguaal worden toegediend. Ook kunnen de speekselklieren worden geïnjecteerd met botulinetoxine of behandeld worden met radiotherapie.
Obstipatie
Obstipatie is waarschijnlijk het gevolg van vertraagde gastro-intestinale motiliteit. In een prospectief observationeel cohortonderzoek bij 6790 mannen in Hawaï met een follow-up van 24 jaar werd een onafhankelijk positief verband gevonden tussen een lage defecatiefrequentie en het ontstaan van de ziekte van Parkinson. Het precieze verband is nog onduidelijk. Obstipatie kan ook het gevolg zijn van het gebruik van anticholinergica en dopamineagonisten.
Mictieklachten
Ongeveer 75% van de patiënten krijgt blaasproblemen. Nycturie is het vroegste en het meest voorkomende probleem bij de ziekte van Parkinson, ook urge-incontinentie komt frequent voor.
Seksuele klachten
Erectiele disfunctie en hyperseksualiteit kunnen zowel het gevolg zijn van de ziekte zelf als bijwerkingen van de medicatie.
- Levodopa leidt vaak tot een verhoogd libido. Patiënten kunnen dit ervaren als hervonden seksuele honger die niet noodzakelijk afhankelijk is van de aanwezigheid van erotische stimuli of intimiteit met de partner.
- Bij een impulscontrolestoornis kan (vaak heftige) seksuele ontremming optreden.
- Dopaminerge medicatie kan leiden tot vroegtijdige zaadlozing.
- Ook vermoeidheid en motorische klachten (rigiditeit, dyskinesieën) kunnen van invloed zijn op de seksualiteit.
Orthostatische hypotensie
Orthostatische hypotensie komt meestal voor in een gevorderd stadium van de ziekte. Degeneratie van het autonome zenuwstelsel speelt een rol, naast medicatie.
- Probeer bij vallen te achterhalen of dit veroorzaakt wordt door de bewegingsproblemen of door orthostatische hypotensie.
- De MDR noemt als leefstijladviezen:
- verhoging van het hoofdeinde van het bed
- bloeddrukverhogende manoeuvres (zie ook NHG-Standaard Duizeligheid)
- verhoging van de inname van vocht en zout
- steunkousen bij enkeloedeem of pretibiaal oedeem
- Andere opties zijn:
- lagere dosering antihypertensiva
- lagere dosering parkinsonmedicatie
- switch naar medicatie met minder risico op orthostatische hypotensie
- De neuroloog kan een perifere dopamineantagonist overwegen zoals domperidon, fludrocortison, midodrine of pyridostigmine.
Overmatig transpireren
- Overmatige transpiratie kan optreden in het begin van de off-fase als de dopaminerge medicatie net is uitgewerkt.
- Overmatig transpireren kan ook in de on-fase optreden en gaat dan vaak gepaard met dyskinesieën.
Terminale fase
Naar Samenvatting ›- In de terminale fase wordt de rol van de huisarts over het algemeen groter. Patiënten ervaren toenemend beperkingen en verlies van zelfredzaamheid; velen worden aan het einde van het ziekteproces opgenomen in een verpleeghuis.
- Indien de patiënt niet wordt opgenomen zal de huisarts, in samenspraak met de neuroloog, de coördinatie van de zorg in de terminale fase overnemen. De neuroloog blijft in dat geval op consultatiebasis betrokken.
- In de palliatieve fase kan naast een neuroloog ook een specialist ouderengeneeskunde of een regionaal palliatief team geconsulteerd worden, bijvoorbeeld omdat inname van de parkinsonmedicatie niet meer mogelijk is.
- Continueer bij voorkeur de dopaminerge medicatie, eventueel via een neus-maagsonde. Na het staken van de medicatie kunnen zeer hinderlijke motorische symptomen ontstaan. Abrupt staken kan leiden tot ernstige rigiditeit, tremoren en in het ernstigste geval tot een maligne levodopa-onttrekkingssyndroom (zie Maligne levodopa-onttrekkingssyndroom).
- Vermijd antidopaminerge medicatie (metoclopramide, haloperidol) en anticholinerge medicatie (atropine).
- Voor de medicamenteuze behandeling van specifieke symptomen en indien algemeen toegepaste medicatie, zoals metoclopramide, gecontra-indiceerd is, zie tabel 2.
|
Symptoom |
Orale toediening mogelijk? |
Behandelopties |
Dosering |
|
|---|---|---|---|---|
|
Ernstige rigiditeit, forse tremoren |
Ja |
Aanpassing parkinsonmedicatie |
In overleg met neuroloog |
|
|
Gastrostomie of neusmaagsonde |
Vermalen en oplossen van tabletten levodopa of dopamineagonist (tabletten met gereguleerde afgifte staken of omzetten, deze kunnen niet vermalen worden) |
|||
|
Levodopa/benserazide dispertablet |
||||
|
Nee |
Levodopa/carbidopa rectale suspensie (in overleg met apotheker) |
|||
|
Indien onvoldoende effect |
Midazolam injectie sc of neusspray |
|||
|
Maligne levodopa-onttrekkingssyndroom |
Ja |
Herstart dopaminerge medicatie |
In overleg met neuroloog |
|
|
Gastrostomie of neusmaagsonde |
Vermalen en oplossen van tabletten levodopa- of dopamineagonist |
|||
|
Nee |
Levodopa/carbidopa rectale suspensie (in overleg met apotheker) |
|||
|
Indien onvoldoende effect |
Midazolam injectie sc |
|||
|
Misselijkheid en braken (contra-indicatie voor metoclopramide en haloperidol) |
Ja |
Domperidon (smelt)tablet of suspensie |
1-3 dd 10-20 mg |
|
|
Dexamethason tablet |
1 dd 4-8 mg |
|||
|
Levomepromazine tablet (off-label) |
1 dd 6,25-12,5 mg voor de nacht |
|||
|
Nee |
Dexamethason injectie sc of iv |
1 dd 4-8 mg |
||
|
Levomepromazine injectie sc (bolus of continue toediening) (off -label) |
1 dd 3,12 mg zo nodig ophogen tot max. 12,5 mg/dag |
|||
|
Terminaal delier (contra-indicatie voor haloperidol) |
Ja |
Lorazepam drank of tablet |
6 dd 1-4 mg (evt. sublinguaal of in wangzak)
|
|
|
Nee |
Midazolam injectie sc |
|||
|
Reutelen (omgeving verzoekt ondanks adequate informatie om medicatie bij aanhoudend reutelen ondanks optimale houding) (contra-indicatie voor atropine) |
|
Scopolaminebutyl injectie sc of iv (bolus of continue toediening) (off-label) |
20 mg zo nodig ophogen naar 60-120 mg/24 uur |
|
|
Scopolamine pleister (off-label) |
1,5 mg/72 uur |
|||
|
Bronnen: IKNL-richtlijn Ziekte van Parkinson: de palliatieve fase, NHG-Spoedkaart Medicatie in acute palliatieve situaties, KNMP Kennisbank. |
||||
De aanbevelingen voor het beleid in de terminale fase zijn grotendeels overgenomen uit de IKNL-richtlijn Ziekte van Parkinson: de palliatieve fase.
Ernstige rigiditeit
In de laatste uren of dagen voor het overlijden kan er sprake zijn van ernstige spierrigiditeit, door de ziekte zelf of doordat de patiënt de orale parkinsonmedicatie niet meer kan innemen. Indien een neus-maagsonde of rectale toediening geen optie is, kan midazolam subcutaan overwogen worden. In de praktijk kan dit betekenen dat er sprake is van palliatieve sedatie.
Reutelen
Gebruik van anticholinergica bij de ziekte van Parkinson geeft een verhoogd risico op delier en hallucinaties. Atropine wordt daarom ontraden. Eventueel kan butylscopolamine (subcutaan of intraveneus) of een scopolaminepleister worden overwogen. Ook hierbij is er het risico op delier verhoogd, maar het anticholinerge effect is veel minder sterk omdat (butyl)scopolamine de bloed-hersenbarrière niet passeert.
Misselijkheid en braken
De IKNL-richtlijn noemt quetiapine als aanvullende behandeloptie indien domperidon, dexamethason en levomepromazine onvoldoende effectief zijn.
Terminaal delier
Een terminaal delier kan bij de ziekte van Parkinson moeilijk te herkennen zijn. Dit delier uit zich door onrust en plukkerig gedrag in de laatste uren voor het overlijden. Antipsychotica zijn bij een terminaal delier nauwelijks/niet effectief en klassieke antipsychotica zijn gecontra-indiceerd. Daarom is het advies om palliatieve sedatie in te zetten indien lorazepam onvoldoende effectief is of orale behandeling niet mogelijk is.
Maligne levodopa-onttrekkingssyndroom
Hoe meer spiermassa een patiënt heeft, groter de kans op een maligne levodopa-onttrekkingssyndroom. De basis van de behandeling is het weer toedienen van dopaminerge medicatie, in overleg met neuroloog.
- Als de patiënt een levodopapomp heeft, wordt geadviseerd deze zo mogelijk voort te zetten.
- Het starten van rotigotinepleisters wordt niet aanbevolen omdat hiermee vaak geen equivalente dosering bereikt kan worden en de benodigde hoge startdosering gepaard gaat met bijwerkingen zoals misselijkheid, die in deze fase ongewenst zijn.
- Apomorfine wordt niet aanbevolen omdat ook dit middel gepaard gaat met ongewenste bijwerkingen.
Dopamineagonistonttrekkingssyndroom
Het dopamineagonistonttrekkingssyndroom lijkt op het beeld bij onttrekking van opiaten en andere psychoactieve stoffen. Het syndroom komt vrijwel uitsluitend voor bij patiënten met impulscontrolestoornissen door dopamineagonisten. Symptomen zijn angst, agitatie, slaapproblemen, depressie, moeheid en pijn. Daarnaast kunnen er autonome verschijnselen optreden zoals orthostatische hypotensie, duizeligheid, misselijkheid en hevige transpiratie. Het dopamineagonistonttrekkingssyndroom kan behandeld worden door rotigotinepleisters of apomorfine. Het toedienen of verhogen van levodopa is niet zinvol.
Consultatie en verwijzing
Naar Samenvatting ›- Overweeg verwijzing bij klachten of problemen die gerelateerd zijn aan de ziekte van Parkinson (zie tabel 3):
- overleg met of informeer de neuroloog bij verwijzingen naar andere zorgverleners.
- verwijs bij voorkeur naar een hulpverlener met parkinsonspecifieke kennis (zie Parkinsonzorgzoeker of ParkinsonNet).
- Verwijs direct naar de neuroloog bij vermoeden van:
- maligne levodopa-onttrekkingssyndroom
- serotoninesyndroom
Organisatie van zorg
Naar Samenvatting ›- Door het progressieve beloop van de ziekte en door bijkomende aandoeningen zijn vaak verscheidene gespecialiseerde zorgverleners betrokken bij de zorg voor een patiënt. De huisarts, neuroloog en parkinsonverpleegkundige of verpleegkundig specialist zijn altijd bij de zorg betrokken.
- ParkinsonNet is een landelijk netwerk van zorgverleners die gespecialiseerd zijn in de begeleiding van parkinsonpatiënten.
- Eenduidige afspraken over het behandeltraject, de samenwerking en de overdracht zijn belangrijk. Het moet duidelijk zijn wie verantwoordelijk is voor welk deel van de zorg en de patiënt een duidelijk aanspreekpunt hebben bij problemen.
- In het algemeen is de neuroloog hoofdbehandelaar van de gezondheidsproblemen die gerelateerd zijn aan de ziekte van Parkinson.
- In overleg kan hiervan worden afgeweken en kan de neuroloog als consulent optreden, bijvoorbeeld in de terminale fase.
- De parkinsonverpleegkundige of verpleegkundig specialist heeft onder andere tot taak het signaleren van (veranderingen in) de zorg- en informatiebehoefte en het (samen met de neuroloog) initiëren en coördineren van de hiervoor benodigde zorg.
- De rollen van andere zorgverleners kunnen regionaal verschillen en overlappen (zie tabel 3).
Referenties
- O'Sullivan SS, Evans AH, Lees AJ. Dopamine dysregulation syndrome: an overview of its epidemiology, mechanisms and management. CNS Drugs 2009;23:157-70.
- NVN. Ziekte van Parkinson (2020), geraadpleegd november 2023. Ga naar bron: NVN. Ziekte van Parkinson (2020), geraadpleegd november 2023.
- Nelis EA, Berendse HW, Van den Heuvel OA. Hyperseksualiteit en andere impulscontrolestoornissen bij de ziekte van Parkinson. Ned Tijdschr Geneeskd 2016;160.
- Van der Velden RMJ, Broen MPG, Kuijf ML, Leentjens AFG. Stemmingsfluctuaties bij patiënten met de ziekte van Parkinson. Ned Tijdschr Geneeskd 2019;163.
- Van Hommerig J, Overbeek L. Cijfers over ziekten op jaarbasis - hoe gezond is Nederland? Utrecht: Nivel, 2023. http://www.nivel.nl/nl/nivel-zorgregistraties-eerste-lijn, geraadpleegd november 2023. Ga naar bron: Van Hommerig J, Overbeek L. Cijfers over ziekten op jaarbasis - hoe gezond is Nederland? Utrecht: Nivel, 2023. http://www.nivel.nl/nl/nivel-zorgregistraties-eerste-lijn, geraadpleegd november 2023.
- VZinfo.nl. Ziekte van Parkinson. Bilthoven: RIVM 2022. http://www.vzinfo.nl/levensverwachting/leeftijd-en-geslacht, geraadpleegd juli 2022. Ga naar bron: VZinfo.nl. Ziekte van Parkinson. Bilthoven: RIVM 2022. http://www.vzinfo.nl/levensverwachting/leeftijd-en-geslacht, geraadpleegd juli 2022.
- Post B, Van den Heuvel L, Van Prooije T, Van Ruissen X, Van de Warrenburg B, Nonnekes J. Young onset Parkinson's disease: a modern and tailored approach. J Parkinsons Dis 2020;10:S29-s36.
- Haaxma CA, Bloem BR, Borm GF, Oyen WJ, Leenders KL, Eshuis S, al. e. Gender differences in Parkinson's disease. J Neurol Neurosurg Psychiatry 2007;78:819-24.
- Vlaanderen FP, De Man Y, Krijthe JH, Tanke MAC, Groenewoud AS, Jeurissen PPT, al. e. Sex-specific patient journeys in early Parkinson's disease in the Netherlands. Front Neurol 2019;10:794.
- Sauerbier A, Aris A, Lim EW, Bhattacharya K, Ray Chaudhuri K. Impact of ethnicity on the natural history of Parkinson disease. Med J Aust 2018;208:410-14.
- De Baat C, Van Stiphout MAE, Lobbezoo F, Van Dijk KD, Berendse HW. Ziekte van Parkinson: pathogenese, etiologie, symptomen, diagnostiek en beloop. Nederlands tijdschrift voor tandheelkunde 2018;125:509-15.
- Samii A, Nutt JG, Ransom BR. Parkinson's disease. Lancet 2004;363:1783-93.
- Poewe W, Seppi K, Tanner CM, Halliday GM, Brundin P, Volkmann J. Parkinson disease. Nat Rev Dis Primers 2017;3:17013.
- Ascherio A, Schwarzschild MA. The epidemiology of Parkinson's disease: risk factors and prevention. Lancet Neurol 2016;15:1257-72.
- Breckenridge CB, Berry C, Chang ET, Sielken RL, Jr., Mandel JS. Association between Parkinson's disease and cigarette smoking, rural living, well-water consumption, farming and pesticide use: systematic review and meta-analysis. PLoS One 2016;11:e0151841.
- Vaccari C, El Dib R, Gomaa H, Lopes LC, De Camargo JL. Paraquat and Parkinson's disease: a systematic review and meta-analysis of observational studies. J Toxicol Environ Health B Crit Rev 2019;22:172-202.
- Schrag A, Horsfall L, Walters K, Noyce A, Petersen I. Prediagnostic presentations of Parkinson's disease in primary care: a case-control study. Lancet Neurol 2015;14:57-64.
- Plouvier AO, Hameleers RJ, Van den Heuvel EA, Bor HH, Olde Hartman TC, Bloem BR, al. e. Prodromal symptoms and early detection of Parkinson's disease in general practice: a nested case-control study. Fam Pract 2014;31:373-8.
- De Lau LM, Schipper CM, Hofman A, Koudstaal PJ, Breteler MM. Prognosis of Parkinson disease: risk of dementia and mortality: the Rotterdam study. Arch Neurol 2005;62:1265-9.
- Dommershuijsen LJ, Heshmatollah A, Darweesh SKL, Koudstaal PJ, Ikram MA, Ikram MK. Life expectancy of parkinsonism patients in the general population. Parkinsonism Relat Disord 2020;77:94-9.
- De Lau LM, Verbaan D, Marinus J, Van Hilten JJ. Survival in Parkinson's disease. Relation with motor and non-motor features. Parkinsonism Relat Disord 2014;20:613-6.
- Ghosh R, Liddle BJ. Emergency presentations of Parkinson's disease: early recognition and treatment are crucial for optimum outcome. Postgrad Med J 2011;87:125-31.
- Simonet C, Tolosa E, Camara A, Valldeoriola F. Emergencies and critical issues in Parkinson's disease. Pract Neurol 2020;20:15-25.
- Van der Kolk NM, Huvenaars MMJ, Bethlehem C, Roelofs S, Post B. Adviezen voor optimale parkinsonzorg rondom ziekenhuisopnames en operaties. Tijdschr Neurol Neurochir 2018;119:198-205.
- Van de Warrenburg BPC, Snijders AH, Munneke M, Bloem BR. Loopstoornissen door neurologische aandoeningen. Ned Tijdschr Geneeskd 2007;151:395-400.
- Kuks JBM, Snoek JW. Klinische neurologie. 16e druk ed. Houten: Bohn, Stafleu en Van Loghum, 2007.
- Visser M, Marinus J, Bloem BR, Kisjes H, Van den Berg BM, Van Hilten JJ. Clinical tests for the evaluation of postural instability in patients with parkinson's disease. Arch Phys Med Rehabil 2003;84:1669-74.
- Ernst M, Folkerts AK, Gollan R, Lieker E, Caro-Valenzuela J, Adams A, al. e. Physical exercise for people with Parkinson's disease: a systematic review and network meta-analysis. Cochrane Database Syst Rev 2023;1:CD013856.
- Aronson JK. Meyler's side effects of drugs: the international encyclopedia of adverse drug reactions and interactions. 15 ed. Amsterdam: Elsevier, 2006.