COVID-19
Richtlijnen diagnostiek
Naar Volledige tekst ›Anamnese
Naar Volledige tekst ›Vraag naar:
- klachten passend bij COVID-19:
- koorts
- hoesten
- verkoudheidsklachten, keelpijn
- plotseling verlies van smaak- en/of reukvermogen (zonder neusverstopping)
- kortademigheid/benauwdheid, vermoeidheid/verminderde inspanningstolerantie
- duur van de klachten, of er sprake is van een snelle achteruitgang
- risicofactoren voor een ernstig beloop (zie Risicogroepen)
- vaccinatiestatus COVID-19
- angst voor COVID-19
- gevolgen voor de werk- en thuissituatie en eventuele (thuis)zorg
- behandelwensen van de patiënt (zoals wel/geen ziekenhuisopname)
Lichamelijk onderzoek
Naar Volledige tekst ›- Let op algemene toestand en mate van ziek zijn, waaronder koorts, verwardheid en sufheid.
- Bepaal zuurstofsaturatie, adem- en hartfrequentie en zo nodig de bloeddruk. Let op: het komt geregeld voor dat patiënten bij een lage saturatie niet benauwd lijken.
- Onderzoek de longen.
- Verder lichamelijk onderzoek op geleide van de anamnese.
Aanvullend onderzoek
Naar Volledige tekst ›- Verricht diagnostiek naar COVID-19, wanneer de diagnose consequenties heeft voor het beleid.
- De PCR-test heeft de voorkeur boven de antigeensneltest.
- Houd rekening met een fout-negatieve testuitslag. Overweeg bij aanhoudende klachten opnieuw een PCR-test af te nemen bij een sterk vermoeden van COVID-19.
- CRP en X-thorax: zie voor indicaties en beleid de NHG-Standaard Acuut hoesten.
Evaluatie
Naar Volledige tekst ›- Stel de diagnose COVID-19 bij klachten passend bij COVID-19 en een positieve PCR- of antigeensneltest (ook indien zelf-afgenomen).
- Denk differentiaaldiagnostisch onder andere aan: longembolie, acuut coronair syndroom, longaanval astma/COPD, hartfalen of een luchtweginfectie door een andere verwekker (bacterieel/viraal).
Richtlijnen beleid
Naar Volledige tekst ›Voorlichting en advies
Naar Volledige tekst ›- Informeer de patiënt over het te verwachten beloop.
- Vraag de patiënt contact op te nemen bij verslechtering, vooral bij kortademigheid, ernstige vermoeidheid en/of beperkte inspanningstolerantie, bij verwardheid en bij aanhoudende klachten.
- Adviseer bedlegerige patiënten om regelmatig even te bewegen, bijvoorbeeld door 2 tot 3 keer per dag 5 tot 10 minuten uit bed te komen.
- Verwijs naar de informatie over COVID-19 op thuisarts.nl of verwijs naar Pharos voor eenvoudige uitleg en afbeeldingen over COVID-19 en informatie over COVID-19 in andere talen.
Medicamenteuze behandeling
Naar Volledige tekst ›- Schrijf geen middelen voor waarvan de werkzaamheid niet is aangetoond.
- Adviseer bij griepachtige klachten, zoals keel- of spierpijn, zo nodig paracetamol en als tweede keus NSAID’s conform de NHG-Standaard Pijn.
Nirmatrelvir/ritonavir
Naar Volledige tekst ›- We bevelen behandeling met nirmatrelvir/ritonavir niet aan bij patiënten met COVID-19, met uitzondering van de hieronder genoemde groepen patiënten.
- Overweeg nirmatrelvir/ritonavir alleen bij de zeer kleine groep niet-zwangere volwassen patiënten die contact opnemen met de huisarts vanwege klachten die ≤ 5 dagen bestaan, EN die een sterk verhoogd risico hebben op een ernstig beloop, vanwege:
- een ernstig verminderde afweer en onder behandeling zijn bij een medisch specialist, ongeacht vaccinatiestatus (zie Risicogroepen; vaak zal het voorschrijven via de behandelend specialist gaan).
OF - verondersteld SARS-CoV-2-naïef zijn (ongevaccineerd en COVID-19 niet doorgemaakt) EN een sterk verhoogd risico hebben op een ernstig beloop door comorbiditeit of klinische conditie (bijvoorbeeld kwetsbare ouderen of patiënten met een ernstige cardiale of pulmonale aandoening)
- een ernstig verminderde afweer en onder behandeling zijn bij een medisch specialist, ongeacht vaccinatiestatus (zie Risicogroepen; vaak zal het voorschrijven via de behandelend specialist gaan).
- Neem relevante interacties en de risicofactoren voor een ernstig beloop mee in de afweging om nirmatrelvir/ritonavir voor te schrijven. Bespreek de voor- en nadelen met de patiënt.
- Geef bij de keuze voor behandeling, uiterlijk 5 dagen na begin van de klachten, nirmatrelvir 2 dd 300 mg tegelijkertijd met ritonavir 2 dd 100 mg gedurende 5 dagen (eGFR 30-60: verlaag dosering nirmatrelvir naar 2 dd 150 mg).
- Overleg laagdrempelig met de internist, longarts of apotheker.
Antibiotica
Naar Volledige tekst ›- Wees terughoudend met antibiotica.
- In sommige gevallen zal de huisarts toch besluiten antibiotica voor te schrijven. Bijvoorbeeld bij een sterk vermoeden van een bacteriële co-infectie. Of bij kwetsbare of klinisch zieke patiënten omdat het risico op een bacteriële verwekker van de pneumonie, hoewel weinig voorkomend naast COVID-19, met de bijbehorende risico’s op een ernstig beloop bij de betreffende patiënt, zwaarder weegt dan de risico’s op overbehandeling. Schrijf dan antibiotica voor conform de voorkeursmiddelen in de NHG-Standaard Acuut hoesten.
Inhalatiecorticosteroïden
Naar Volledige tekst ›We bevelen het voorschrijven van inhalatiecorticosteroïden als behandeling van COVID-19 niet aan.
Controles
Naar Volledige tekst ›- Monitor het beloop.
- Overleg met de patiënt hoe vaak contactmomenten nodig zijn. Dit hangt af van de ernst van de klachten, comorbiditeit en persoonsgebonden factoren. Overweeg dagelijks contact bij patiënten behorend tot een risicogroep (zie Risicogroepen).
- Instrueer de patiënt in ieder geval contact op te nemen bij:
- toename klachten of achteruitgang
- kortademigheid/benauwdheid, extreme vermoeidheid of verminderde inspanningstolerantie
- aanhoudende klachten, terugkerende koorts en/of andere klachten, zoals verwardheid
Consultatie en verwijzing
Naar Volledige tekst ›- Overleg bij twijfel met een longarts/internist, bijvoorbeeld bij patiënten met toename klachten of bij patiënten uit een risicogroep.
- Criteria voor overleg met longarts/internist en waarschijnlijk ziekenhuisopname:
- ernstig zieke patiënt
- ademfrequentie > 24/min in rust
- saturatie < 92-94%
- klinische achteruitgang, zoals progressieve dyspneu of inspanningsintolerantie
Evaluatie meerwaarde verwijzing tweede lijn bij kwetsbare patiënten
Naar Volledige tekst ›Weeg bij kwetsbare patiënten af of ziekenhuisopname meerwaarde heeft.
- Houd rekening met de voor- en nadelen/risico’s van ziekenhuisopname.
- Bepaal of ziekenhuisopname met eventueel IC-opname meerwaarde heeft. Een ziekenhuisopname biedt mogelijkheid voor medicatie en ondersteuning door toediening van infuusvloeistof, zuurstof en/of beademing.
- De Clinical Frailty Score kan bij de afweging behulpzaam zijn.
- Bepaal of aanvullend onderzoek naar en/of behandeling van andere ziektes in het ziekenhuis nodig is.
- Bespreek de wensen en doelen van de patiënt.
Beleid bij zuurstofbehoeftige, niet-terminale patiënten die niet opgenomen willen worden
Naar Volledige tekst ›Als ziekenhuisopname niet gewenst is (zie Consultatie en verwijzing), maar herstel nog wel het uitgangspunt is, overweeg dan:
- zuurstofbehandeling thuis via een neusbril bij saturatie < 92% en/of ademfrequentie > 24/min in rust (bij patiënten met COPD: saturatie < 88-90%, afhankelijk van de uitgangssaturatie)
- Start met 2 L/min, controleer minimaal 30 minuten na start de saturatie in rust.
- Streefwaarde saturatie 92-96% (bij patiënten met COPD 88-92%, afhankelijk van de uitgangssaturatie).
- Hoog zo nodig de dosering op met 1 L/min tot max. 5 L/min).
- dexamethason bij patiënten met zuurstofbehandeling thuis
- Geef bij volwassenen 6 mg 1 dd gedurende 10 dagen of korter bij eerder herstel.
- Schrijf geen dexamethason voor aan COVID-19 patiënten die niet zuurstofbehoeftig zijn.
- profylactisch laagmoleculairgewicht heparine (LMWH)
- Geef zolang de patiënt behandeld wordt met zuurstof, enoxaparine subcutaan 1 dd 4000 IE (= 40 mg), nadroparine subcutaan 1 dd 2850 IE of dalteparine subcutaan 1 dd 5000 IE.
- Verdubbel de dosering bij patiënten met een BMI ≥ 40.
- Schrijf geen profylactisch LMWH voor als de patiënt al anticoagulantia (vitamine K-antagonisten, DOAC’s) gebruikt.
- voor de indicatie antibiotica, zie Antibiotica.
Belangrijkste wijzigingen
Naar Samenvatting ›November 2023
- De NHG-Standaard COVID-19 is een reguliere richtlijn geworden in plaats van een levende richtlijn.
- Diverse paragrafen zijn komen te vervallen omdat ze niet meer passen bij de huidige endemische fase van COVID-19.
- De paragraaf Risicogroepen is aangepast naar patiënten die door leeftijd of comorbiditeit een verhoogd risico hebben op een ernstig beloop van COVID-19 en patiënten met een ernstig verminderde afweer waardoor vaccinatie onvoldoende werkzaam kan zijn.
- De aanbeveling voor inhalatiecorticosteroïden is gewijzigd; inhalatiecorticosteroïden als behandeling van COVID-19 bevelen we niet meer aan.
Oktober 2022
Nirmatrelvir/ritonavir kan overwogen worden bij een zeer kleine groep patiënten met een sterk verhoogd risico op een ernstig beloop.
Juni 2022
De aanbeveling waarin vernevelen werd afgeraden is komen te vervallen.
April 2022
- De diagnose COVID-19 kan ook gesteld worden bij klachten passend bij COVID-19 en een positieve antigeensneltest die door de patiënt zelf is afgenomen.
- Overweeg profylactisch laagmoleculair gewicht heparine (LMWH) alleen bij COVID-19-patiënten die thuis behandeld worden met zuurstof.
Kernboodschappen
Naar Samenvatting ›- Sommige COVID-19-patiënten met een lage saturatie lijken klinisch niet ernstig benauwd te zijn.
- Verricht diagnostiek naar COVID-19 als het bevestigen van de diagnose consequenties heeft voor het beleid.
- Bij een saturatie < 92-94% en/of ademfrequentie > 24/min en/of klinisch snelle achteruitgang is ziekenhuisopname geïndiceerd.
- Bij een specifieke groep patiënten met een sterk verhoogd risico op een ernstig beloop kunt u antivirale behandeling met nirmatrelvir/ritonavir overwegen.
Inleiding
Naar Samenvatting ›Deze NHG-Standaard behandelt de medisch-inhoudelijke aspecten van COVID-19. Raadpleeg voor organisatorische zaken, zoals infectiepreventie, het NHG-dossier Infectieziekten.
Scope
Naar Samenvatting ›Richtlijnen voor de diagnostiek en behandeling van COVID-19 in de acute fase. De acute fase duurt tot ongeveer 4 weken na start van de klachten.
Buiten de scope
Naar Samenvatting ›- Aanhoudende klachten en nazorg van COVID-19 ≥ 4 weken na start van de klachten; raadpleeg hiervoor de NHG-Standaard Langdurige klachten na COVID-19.
- Vervroegd ontslag van COVID-19-patiënten die naar huis gaan met zuurstof en een saturatiemeter. Zie hiervoor de Leidraad Vervroegd ontslag van COVID-19 patiënten met zuurstofbehoefte naar huis of naar een andere zorglocatie met monitoring.
Samenwerking en afstemming
Naar Samenvatting ›Deze NHG-Standaard sluit inhoudelijk aan bij de volgende leidraden/documenten:
- Leidraad zuurstofgebruik thuis bij (verdenking op/bewezen) COVID-19
- Leidraad triage thuisbehandeling versus verwijzen naar het ziekenhuis bij oudere patiënt met (verdenking op) COVID-19
- Documenten Symptoombestrijding in de thuissituatie bij patiënten met een COVID-19 (Corona) in de laatste levensfase, Symptoombestrijding in de palliatieve fase bij krapte aan mensen, medicatie, pompen en/of PBM, naar aanleiding van Covid-19 en de bijbehorende samenvattingskaart
- SWAB/FMS-richtlijn Medicamenteuze behandeling voor patiënten met COVID-19
Achtergronden
Naar Samenvatting ›Epidemiologie
Naar Samenvatting ›- Op 27 februari 2020 werd de eerste patiënt met COVID-19 in Nederland gemeld. Op 25 mei 2021, 15 maanden later, waren er tot dan toe in totaal 1.631.384 bevestigde patiënten met COVID-19 in Nederland. Het aantal gemelde personen met COVID-19 is gerelateerd aan het testbeleid en de testbereidheid; het aantal personen dat COVID-19 heeft doorgemaakt, zal in werkelijkheid hoger liggen. Op 25 mei 2021 waren tot dan toe 56.412 bewezen of verdachte COVID-19-patiënten opgenomen op de verpleegafdeling van een Nederlands ziekenhuis, van wie 7.627 patiënten overleden. Voor 12.623 patiënten was een IC-opname nodig; 3.432 van deze patiënten overleden.
- Nederlandse cijfers van december 2020 tot en met 21 februari 2021 laten zien dat in die periode 3,3% van de positief geteste personen in het ziekenhuis werd opgenomen. Van de opgenomen patiënten ging zo’n 17% naar de IC.
- De kans op een ernstig beloop is, sinds het begin van de COVID-19-pandemie, afgenomen door toename van het aantal personen in Nederland met antistoffen tegen COVID-19.
Nederlandse situatie en regionale prevalentie
Het RIVM houdt actuele informatie bij over het aantal patiënten met een bevestigde SARS-CoV-2-infectie in Nederland, per regio en per gemeente. Zie Actuele informatie (geraadpleegd 25-5-2021). Stichting Nationale Intensive Care Evaluatie (NICE) toont de registratie van COVID-19-patiënten op de Nederlandse intensive care (IC) en op verpleegafdelingen (https://www.stichting-nice.nl/, geraadpleegd 25-5-2021).
De regionale prevalentie kan beïnvloed worden door het bestaan van zogenaamde clusters.
Er wordt gesproken van een cluster bij meerdere besmette mensen die aan elkaar gerelateerd zijn.
Veiligheidsregio’s
Nederland is opgedeeld in 25 veiligheidsregio’s. Per regio wordt op het coronadashboard van de Rijksoverheid aangegeven wat het risiconiveau van de regio is. Het risiconiveau wordt bepaald op basis van het aantal ziekenhuisopnames en het aantal nieuwe besmettingen per 100.000 inwoners. Er zijn 4 niveaus: ‘waakzaam’ (niveau 1), ‘zorgelijk’ (niveau 2), ‘ernstig’ (niveau 3) en ‘zeer ernstig’ (niveau 4). De coronamaatregelen van de Rijksoverheid worden afgestemd op het risiconiveau in de verschillende regio’s.
Nivel-surveillance
Het Nivel publiceert wekelijks cijfers over infectieziektengerelateerde symptomen en diagnoses, waaronder COVID-19, op basis van HIS-gegevens van zo’n 350 praktijken verdeeld over Nederland.
Ziekenhuisopnames
Sinds 1 juni 2020 is het landelijk beleid dat iedereen met klachten zich kan laten testen op SARS-CoV-2. Vanaf 1 december 2020 kunnen ook personen zonder klachten zich laten testen als zij risico hebben gelopen op een besmetting. Het is aannemelijk dat niet alle met SARS-CoV-2 besmette personen daadwerkelijk getest worden; de cijfers zijn daarom niet volledig. Gezien de wijziging in het testbeleid per 1 december 2020 is gerekend met cijfers vanaf deze periode. Sinds 30 november 2020 tot en met 21 februari 2021 zijn er 536.363 personen positief getest op SARS-CoV-2 en gemeld aan de GGD. Volgens de stichting NICE zijn er in deze periode 17.760 patiënten in het ziekenhuis opgenomen met COVID-19, ofwel 3,3% van het totaal aantal positief geteste personen. Van de patiënten die opgenomen werden in het ziekenhuis, werd 17% opgenomen op de IC.
Wereldwijd
Het ECDC en de WHO houden officiële cijfers over het aantal bevestigde patiënten met COVID-19 wereldwijd en de geografische verspreiding bij.
Sterftecijfer
Naar Samenvatting ›De infection fatality rate (IFR), het percentage van de besmette patiënten dat overlijdt, werd in 2020 in Nederland geschat op 1% tot 1,3%. Deze schatting is gebaseerd op Nederlandse data over oversterfte en het aantal SARS-CoV-2-besmette personen. Het is een gemiddelde voor de gehele populatie, waarbij er significante verschillen zijn tussen de verschillende leeftijdsgroepen. De IFR stijgt met het toenemen van de leeftijd.
In verschillende onderzoeken uit 2020 wordt de mondiale case fatality rate (CFR) berekend op 2,5-4,2%. De samenstelling van een populatie (leeftijd, geslacht, comorbiditeit), kwaliteit en toegankelijkheid van zorg en testbeleid zijn onder andere van invloed op deze cijfers. Voor de infection fatality rate (IFR) wordt geschat hoe het aantal doden zich verhoudt tot het aantal geïnfecteerden (bij de CFR gaat het om het aantal bevestigde personen met COVID-19). Op basis van Nederlandse data uit 2020 over oversterfte en het aantal met SARS-CoV-2 besmette personen wordt de IFR geschat op 1-1,3%.
Op basis van leeftijd is er een significant verschil in CFR bij verschillende leeftijdsgroepen. Gebaseerd op cijfers uit Duitsland was deze in de periode van 6 juli t/m 6 september 2020 voor 35- tot 59-jarigen 1%, voor 60- tot 79-jarigen 2%, en voor 80-plussers 11%. In Spanje is een IFR van 1,1% geschat op basis van de oversterfte en seroprevalentie van april tot medio juli 2020. Vanaf 50 jaar stijgt de IFR, waarbij het voor 80-plussers oploopt tot 6,5% voor vrouwen en 16,4 % voor mannen.
Incubatietijd
Naar Samenvatting ›De incubatietijd bedraagt 2 tot maximaal 14 dagen, gemiddeld 5 tot 6 dagen.
Besmettingsweg
Naar Samenvatting ›- SARS-CoV-2 is van mens op mens overdraagbaar. Transmissie vindt waarschijnlijk voornamelijk plaats via druppels die vrijkomen uit de neus- en keelholte (druppeltransmissie).
- Ook aerosolen (zwevende deeltjes) spelen in bepaalde situaties een rol bij de verspreiding van SARS-CoV-2. De Federatie Medisch Specialisten (FMS) heeft medische procedures beschreven die een infectieuze aerosol genereren met SARS-CoV-2.
- SARS-CoV-2 kan zich via de handen verspreiden. Transmissie vindt ook plaats via indirect contact met besmette oppervlakten of voorwerpen; de grootte van de rol van indirecte overdracht in de verspreiding van SARS-CoV-2 is nog onduidelijk.
- De kans op besmetting is afhankelijk van een aantal factoren: frequentie van contacten met besmette patiënten, intensiteit en duur van het contact met besmette patiënten en de hoeveelheid virusdeeltjes van besmette patiënten.
Directe overdracht
SARS-CoV-2 is van mens op mens overdraagbaar. Het virus wordt waarschijnlijk, zoals andere coronavirussen, met name overgedragen via druppels die vrijkomen uit de neus- en keelholte (druppeltransmissie) binnen een afstand van 1,5 meter. SARS-CoV-2 is ook aangetroffen in de feces van patiënten, maar fecaal-orale besmetting is niet met zekerheid vastgesteld.
Indirecte overdracht
Er zijn aanwijzingen dat ook indirecte overdracht mogelijk is bij COVID-19. Indirecte overdracht kan plaatsvinden wanneer een persoon besmette oppervlakten en voorwerpen heeft aangeraakt waarop voldoende infectieus virus aanwezig is en daarna de mond, ogen of neus aanraakt. Er is geen bewijs voor indirecte overdracht in de publieke ruimte. De grootte van de rol van indirecte overdracht in de verspreiding van SARS-CoV-2 is nog onduidelijk.
Aerogene overdracht
Bij aerogene overdracht van een virus vindt overdracht plaats via zwevende deeltjes (aerosolen) in de lucht. Aerosolen spelen in bepaalde situaties een rol bij de verspreiding van SARS-CoV-2. De Federatie Medisch Specialisten (FMS) heeft een overzicht gepubliceerd van medische procedures, zoals bijvoorbeeld intubatie, die een infectieuze aerosol genereren met SARS-CoV-2. Vaak betreft dit handelingen op de IC.
Aerosolvormende handelingen die (zelden) in de huisartsenpraktijk plaatsvinden zijn:
- cardiopulmonaire reanimatie
- niet-invasieve beademing
- handmatige beademing
- elektrochirurgie (afhankelijk van materiaal)
- vernevelen
Varianten van SARS-CoV-2
Bij een aantal nieuwe SARS-CoV-2-varianten blijkt de hoeveelheid virusdeeltjes in de bovenste luchtwegen aanzienlijk hoger te zijn dan bij de eerdere varianten. Door een opgetreden mutatie vindt er een betere hechting plaats aan de receptor van menselijke cellen. Hierdoor dringt het virus gemakkelijker de cel binnen, is het aantal benodigde virusdeeltjes om een infectie te veroorzaken lager en wordt de hoeveelheid virusdeeltjes in de cel hoger. Het is met de huidige kennis niet aannemelijk dat door deze mutatie de wijze van overdracht verandert van voornamelijk druppeltransmissie naar voornamelijk aerogene transmissie.
Besmettelijke periode en besmettelijkheid
Naar Samenvatting ›- De hoeveelheid virusdeeltjes van besmette patiënten lijkt het hoogst 1 tot 2 dagen voor de start van de symptomen tot 5 dagen na de start van de symptomen.
- Zowel patiënten met milde als met ernstige COVID-19-klachten kunnen virus uitscheiden in de (pre)symptomatische fase van de ziekte.
- In de presymptomatische fase kan transmissie plaatsvinden 1 tot 5 dagen voor de start van de symptomen. Het is echter lastig om goed te definiëren wanneer iemand helemaal geen klachten had of milde of vroege symptomen.
- Asymptomatische patiënten lijken initieel vergelijkbare hoeveelheden virus te hebben, maar de uitscheiding duurt korter. De rol van asymptomatische transmissie is nog onduidelijk.
- Hoelang een patiënt met COVID-19 besmettelijk blijft, lijkt afhankelijk te zijn van de ernst van de doorgemaakte ziekte en of een patiënt immuungecompromitteerd is. Zie Isolatieduur wanneer de isolatie van een patiënt met COVID-19 kan worden opgeheven.
- Herinfecties met SARS-CoV-2 komen voor. Er is echter nog weinig bekend over de mate en de duur van natuurlijke immuniteit na een doorgemaakte infectie. Het lijkt dat de bescherming tegen herinfectie gedurende minstens een half jaar aanwezig is en dat deze bescherming minder is bij personen > 65 jaar dan bij jongere personen. Daarnaast is het nog niet duidelijk of (en in welke mate) personen besmettelijk zijn bij een herinfectie.
Klinisch beeld
Naar Samenvatting ›Een groot deel van de COVID-19-patiënten presenteert zich met ≥ 1 van de volgende klachten:
- hoesten
- koorts/verhoging
- verkoudheidsklachten (loopneus, neusverkoudheid, niezen en keelpijn)
- benauwdheid/kortademigheid.
- plotseling verlies van smaak (dysgeusie/ageusie) of reuk (hyposmie/anosmie)
Daarnaast wordt een grote verscheidenheid aan andere klachten gemeld, waaronder koude rillingen, algehele malaise, vermoeidheid, algehele pijnklachten, oculaire pijn, spierpijn, hoofdpijn, schorre stem, pijn bij de ademhaling, duizeligheid, prikkelbaarheid, verwardheid, delier, buikpijn, verlies van eetlust (anorexie), diarree, overgeven, misselijkheid, conjunctivitis en verschillende huidafwijkingen (waaronder maculopapulair exantheem, urticaria, vasculaire en vesiculaire huiduitslag en huidafwijkingen lijkend op perniones). De meest voorkomende minder specifieke klachten zijn algehele malaise, plotseling optredende vermoeidheid, gastro-intestinale klachten, hoofdpijn en spierpijn.
Bij ouderen kan de klinische presentatie vaker atypisch verlopen, dat wil zeggen zonder de klassieke klachten van koorts, hoesten en benauwdheid. Zij presenteren zich vaker met een atypisch beeld zoals vallen, een knik in het functioneren of een delier.
De frequentie waarmee de verschillende symptomen van COVID-19 worden gemeld is nog onduidelijk. Dit wisselt sterk per onderzoek en is afhankelijk van de onderzochte populatie.
Zowel de klassieke luchtwegklachten als ook niet-respiratoire symptomen kunnen het ziektebeeld COVID-19 typeren. Zo zijn anosmie/ageusie (soms als enige symptoom) en koorts in alle onderzoeken onderscheidend en worden ook spierpijn, vermoeidheid en anorexie genoemd.
Ouderen
Ook oudere patiënten met COVID-19 presenteren zich met variërende klachten. Veelvoorkomende symptomen bij ouderen zijn koorts en hoesten. Een Nederlands onderzoek waarin gegevens van een reeks oudere patiënten met COVID-19 opgenomen in het ziekenhuis beschreven worden, laat zien dat de klinische presentatie bij oudere patiënten vaker atypisch verloopt.
Kinderen
Viner et al. laten in een systematische review van reviews zien dat ook voor kinderen en jongvolwassenen (< 20 jaar) koorts en hoesten de meest voorkomende symptomen lijken. Andere symptomen, zoals neusverkoudheid, keelpijn, diarree en overgeven, bleken minder vaak voor te komen. Veel onderzoeken betroffen kinderen die opgenomen waren in het ziekenhuis met COVID-19, vroeg in de pandemie. In de review varieert het aantal asymptomatische kinderen met SARS-CoV-2 tussen de 14,6 en 42%.
Gastro-intestinale klachten
Volgens een meta-analyse komen gastro-intestinale symptomen bij 15% van de patiënten voor, met misselijkheid, overgeven, diarree en verminderde eetlust als de meest voorkomende symptomen. Patiënten met ernstige COVID-19 hadden frequenter gastro-intestinale symptomen in vergelijking met niet-ernstig zieke patiënten.
Conjunctivitis
Ook conjunctivitis wordt bij COVID-19-patiënten beschreven.
Neurologische verschijnselen
Neurologische verschijnselen zijn frequent beschreven, waaronder perifeer neurale aandoeningen zoals verlies van reukzin (anosmie) en smaakzin (ageusie). Deze klachten worden soms als enige symptoom gezien bij COVID-19-patiënten. Daarnaast zijn er andere symptomen/complicaties van het centrale zenuwstelsel gemeld: hoofdpijn, duizeligheid, ataxie, epileptisch insult en acuut cerebrovasculaire ziekte.
Huidafwijkingen
Bij COVID-19-patiënten worden regelmatig huidafwijkingen gemeld. De huiduitslag varieert van maculopapulair exantheem, urticaria, vasculaire en vesiculaire huiduitslag tot atypische vormen van huidafwijkingen. Huidafwijkingen lijkend op perniones (wintertenen/winterhanden) komen vaker voor bij jongere patiënten. Mogelijk is (een deel van) de vesiculaire uitslag een gevolg van herpesvirus co-infecties. De meeste patiënten kregen huidafwijkingen na begin van respiratoire symptomen.
Beloop
Naar Samenvatting ›- Het ziektebeeld varieert van milde, niet-specifieke klachten tot (meer) ernstige ziektebeelden met koorts, kortademigheid en pneumonie die kunnen leiden tot acute respiratory distress syndrome (ARDS). Bij een ARDS-beeld kan ook sepsis optreden met eindorgaanfalen, activatie van de stolling en trombo-embolische complicaties (meestal longembolieën en soms een herseninfarct). Ook cardiale complicaties, waaronder myocarditis, worden gezien.
- Er zijn ook personen die (bijna) geen klachten ontwikkelen tijdens een infectie met SARS-CoV-2.
- Bij een deel van de patiënten kent COVID-19 een bifasisch beloop. Tijdens een eerste milde fase van meestal 7 tot 10 dagen worden de klachten vooral door de virusinfectie zelf veroorzaakt. In deze fase is er meestal geen hypoxemie. In de tweede fase ontstaat er verslechtering, die gekenmerkt wordt door toenemende benauwdheid/kortademigheid, hypoxemie en eventueel respiratoir falen. Deze verslechtering lijkt veroorzaakt te worden door hyperinflammatie met een toename van ontstekingsverschijnselen als gevolg.
Trombo-embolische complicaties
Naar Samenvatting ›Bij patiënten die ernstig ziek zijn door COVID-19 wordt een hogere incidentie gezien aan trombo-embolische complicaties ten opzichte van andere infectieziekten. COVID-19-patiënten die opgenomen zijn op een verpleegafdeling van het ziekenhuis hebben een 3 tot 7 keer verhoogd risico op veneuze trombo-embolie (VTE) ten opzichte van andere patiënten opgenomen op de verpleegafdeling.
Risico op veneuze trombo-embolie bij COVID-19-patiënten in de eerste lijn
In een onderzoek naar de incidentie van veneuze trombo-embolie (VTE) bij 715 patiënten met een bewezen COVID-19-infectie die buiten het ziekenhuis verbleven, werden geen gevallen van VTE geconstateerd na 30 dagen follow-up. Uit een Brits bevolkingsonderzoek met 272.423 patiënten blijkt de incidentie van trombo-embolische complicaties hoger te zijn geweest tijdens de COVID-19-pandemie (met name tijdens het begin) ten opzichte van de jaren daarvoor: RR 1,43 (95%-BI 1,41-1,44). Dit betroffen vooral longembolieën. Ook de sterfte door trombo-embolische complicaties nam met 6,7% toe tijdens de pandemie.
Risico op veneuze trombo-embolie bij COVID-19-patiënten in de tweede lijn
In een groot retrospectief onderzoek met 10.871 patiënten met COVID-19 in een Amerikaans ziekenhuis bleken 118 patiënten (1%) een longembolie (101/118) of diepveneuze trombose (17/118) te hebben bij opname. Het risico op VTE bij COVID-19-patiënten op een gewone ziekenhuisafdeling was 3% in een Nederlands cohortonderzoek. Dit percentage is hoger dan gebruikelijk bij opgenomen patiënten: gemiddeld 0,4%-0,8%.
Bij systemische infecties kan er activatie van de stolling optreden, die kan variëren van mild tot ernstig. Ook bij patiënten met COVID-19 (met name op de IC) kan er activatie van de stolling optreden. Het beeld lijkt net wat anders dan bij andere infectieziekten (minder bloedingen en minder trombocytopenie), zodat er in plaats van diffuse intravasale coagulopathie (DIC) nu wordt gesproken over een systemische intravasale coagulopathie (SIC). Dit kan gepaard gaan met trombotische complicaties, meestal een longembolie en soms een herseninfarct. Deze trombotische complicaties zijn gecorreleerd met een hoger risico op overlijden.
Uit Nederlands onderzoek is gebleken dat de cumulatieve incidentie van trombosecomplicaties bij COVID-19-patiënten op de IC 49% was na gemiddeld 14 dagen.
Risicogroepen
Naar Samenvatting ›Het risico op een ernstig beloop van COVID-19 is verhoogd bij patiënten met:
- leeftijd > 70 jaar. Hoe hoger de leeftijd hoe hoger het risico.
- comorbiditeit:
- chronische hematologische maligniteit of hematologische maligniteit die < 5 jaar geleden gediagnosticeerd is
- sikkelcelziekte
- neurologische aandoening waardoor de ademhaling gecompromitteerd is
- downsyndroom
- morbide obesitas (arbitrair BMI > 40)
- (ernstige) chronische nierschade
- hart- en vaatziekten, inclusief hartfalen
- verminderde afweer
- levercirrose
- diabetes mellitus
- COPD
Bij mannen is het risico hoger dan bij vrouwen. De kans op een gecompliceerd beloop neemt toe naarmate er meer risicofactoren aanwezig zijn.
Bij patiënten met een ernstig verminderde afweer kan vaccinatie onvoldoende werkzaam zijn, zoals na orgaantransplantatie, bij (behandeling voor) hematologische maligniteit en bij ernstig nierfalen. Zie het detail voor een volledig overzicht en meer specifieke informatie.
Het RIVM heeft in een adviesnota vastgesteld welke volwassen medische risicogroepen er zijn voor de COVID-19-vaccinatiecampagn. Daarbij is onderzoek bekeken uit de periode vóór de COVID-19-vaccinatie en vergeleken met onderzoeken over de risicofactoren voor een gecompliceerd beloop na vaccinatie. COVID-19-vaccinatie is over het algemeen werkzaam en effectief in het voorkomen van een ernstig beloop van COVID-19. De verkregen immuniteit door de vaccinatie neemt echter na verloop van tijd af (waning immunity) Patiënten die een verhoogd risico hebben op een ernstig beloop zijn onder te verdelen in patiëntengroepen die geen of onvoldoende respons laten zien op vaccinatie en patiënten die op basis van leeftijd en/of comorbiditeit een hoger risico hebben op een gecompliceerd beloop.
Gezondheidsraad
De Gezondheidsraad heeft risicogroepen voor een gecompliceerd beloop van COVID-19 (ernstig beloop van de ziekte en/of overlijden door COVID-19) gedefinieerd voor het advies aan de overheid over de Nederlandse vaccinatiestrategie in het ‘Toepassingskader revaccinatie tegen COVID-19’.
Voor vaccinatie
De Gezondheidsraad beschrijft dat op basis van wetenschappelijk onderzoek uitgevoerd vóór de beschikbaarheid van vaccins, leeftijd de belangrijkste risicofactor blijkt: vanaf 60 jaar neemt het risico op sterfte door COVID-19 sterk toe (ten opzichte van 50-60 jarigen is het risico voor 60-jarigen 2,5-5 x hoger, voor 70-jarigen 6-8 x hoger en voor 80-jarigen 11-21x hoger). Onderliggende aandoeningen geven ook een verhoogd risico op een ernstig beloop. Op basis van internationaal onderzoek van vóór vaccinatie wordt een aantal groepen genoemd met het hoogste risico op een ernstig beloop. Deze groepen worden door de Gezondheidsraad en in de LCI-richtlijn ook wel de hoogrisicogroepen genoemd:
- patiënten met een hematologische maligniteit gediagnosticeerd in de laatste 5 jaar
- patiënten met ernstig nierfalen of dialyse
- patiënten na orgaan- of beenmergtransplantatie
- patiënten met een primaire immuundeficiëntie
- patiënten met neurologische aandoeningen waardoor de ademhaling gecompromitteerd is
- mensen met het syndroom van Down;
- mensen met morbide obesitas (BMI > 40).
Daarnaast beschrijft de Gezondheidsraad zogeheten ‘medische risicogroepen’: patiënten die een 1-2 x hoger risico hebben op sterfte ten opzichte van leeftijdsgenoten zonder andere aandoeningen:
- patiënten met afwijkingen en functiestoornissen van de luchtwegen en longen
- patiënten met een chronische stoornis van de hartfunctie
- patiënten met diabetes mellitus
- patiënten met chronische nierinsufficiëntie
- patiënten met een afweerstoornis of behandeld met immuunsuppressiva leidend tot verminderde weerstand tegen luchtweginfecties
- mensen met een verstandelijke beperking wonend in instellingen.
Na vaccinatie
Op basis van enkele onderzoeken beschrijft de Gezondheidsraad dat vergelijkbare groepen ook na vaccinatie, hoewel in mindere mate, nog steeds een hoger risico hebben op een ernstig beloop (ziekenhuisopname en sterfte) dan andere gevaccineerde mensen. Leeftijd blijkt nog steeds de belangrijkste risicofactor. Daarnaast wordt een kleine groep patiënten benoemd met een ernstig gecompromitteerd immuunsysteem. Deze groep liet geen of onvoldoende immuunrespons zien na twee doses van een mRNA-vaccin. Deze groep is vastgesteld door een groep medisch specialisten.
LCI-Richtlijn COVID-19
Ook het LCI benoemt risicogroepen met een verhoogde kans op een ernstig beloop van COVID-19.
De groepen genoemd door de Gezondheidsraad en het LCI komen in grote lijnen overeen, maar er zijn enkele discrepanties. In de LCI-richtlijn wordt met patiënten wonend in instellingen voor langdurige zorg alle instellingen bedoeld waar ouderen, verstandelijk gehandicapten en ggz-cliënten wonen met zorg of begeleiding. De Gezondheidsraad benoemt alleen mensen met een verstandelijke beperking wonend in instellingen. De Gezondheidsraad stelt dat het risico op een ernstig beloop vanaf 60 jaar sterker stijgt, terwijl in de LCI-richtlijn als leeftijdsgrens 70 jaar wordt aangehouden. De Gezondheidsraad benoemt verschillende groepen minder specifiek dan de LCI-richtlijn, bijvoorbeeld ‘patiënten met diabetes mellitus’ versus ‘met diabetes mellitus: slecht ingestelde diabetes of diabetes met secundaire complicaties’. De Gezondheidsraad noemt chronische nierinsufficiëntie, de LCI-richtlijn noemt alleen de groep patiënten met ernstig nierfalen (dialyse of voorbereiding voor dialyse). Patiënten met sikkelcelziekte worden alleen in de LCI-richtlijn genoemd.
In de LCI bijlage COVID-19-vaccinatie van immuungecompromitteerde patiënten wordt een selecte groep ernstig immuungecompromitteerde patiënten benoemd, bij wie mogelijk de standaarddosering van 2 doses onvoldoende vaccinatierespons geeft.
Prognostische risicomodellen
Sinds de start van de COVID-19-pandemie is veel onderzoek verricht naar prognostische risicomodellen voor een gecompliceerd beloop op COVID-19. De definitie van een gecompliceerd beloop bestaat doorgaans uit sterfte en ziekenhuisopname.
Voor vaccinatie
De beschikbare literatuur over prognostische risicomodellen voordat vaccins beschikbaar waren is samengevat in een levende systematische review. De beschreven prognostische modellen zijn echter van onvoldoende kwaliteit en niet gevalideerd voor gebruik in de (Nederlandse) huisartsenpraktijk. Determinanten die frequent gerapporteerd worden als gecorreleerd aan een slechte prognose bij COVID-19 zijn leeftijd, mannelijk geslacht en comorbiditeit. Uit Engels onderzoek vóór de beschikbaarheid van vaccins (data uit 1205 huisartsenpraktijken) naar het risico op COVID-19-gerelateerde sterfte (primaire eindpunt) en ziekenhuisopname (secundair eindpunt) bleek dat de kans op overlijden ten gevolge van COVID-19 tijdens de ‘eerste golf’ sterk verhoogd was bij patiënten met een recente beenmergtransplantatie, ernstig nierfalen, chronisch hartfalen, patiënten die chemotherapie ontvingen en patiënten > 80 jaar. Een aantal andere patiëntengroepen bleek eveneens een verhoogd risico op overlijden te hebben, maar een minder hoog risico dan de genoemde groepen. Het betreft patiënten met hart- en vaatziekten (anders dan hartfalen), diabetes mellitus type 2, COPD, actieve behandeling tegen kanker (niet al in de eerste groep opgenomen), levercirrose en morbide obesitas (arbitrair, BMI > 40).
Na vaccinatie
Een Engels prospectief cohortonderzoek in de algemene bevolking op basis van gegevens van volwassenen na 1 of 2 COVID-19-vaccinaties liet zien dat de incidentie van sterfte en ziekenhuisopname door COVID-19 hoger werd bij stijgende leeftijd en mannelijk geslacht. Daarnaast werden de hoogste hazard ratio’s (HR > 2) voor sterfte gevonden voor patiënten met downsyndroom, niertransplantatie, sikkelcelziekte, wonend in een instelling, chemotherapie, hiv/aids, levercirrose, neurologische aandoeningen, orgaantransplantatie of recente beenmergtransplantatie, dementie en ziekte van Parkinson. Andere aandoeningen die in het onderzoek een 1,2-2 x verhoogd risico gaven, zijn chronische nierschade, hematologische maligniteit, epilepsie, COPD, hart- en vaatziekten, hartfalen en diabetes mellitus type 2.
Een Engels retrospectief cohortonderzoek op basis van gegevens van volledig gevaccineerde personen met een doorbraakinfectie liet zien dat de kans op COVID-19-gerelateerde ziekenhuisopname en overlijden toeneemt met oplopende leeftijd en bij obesitas. Comorbiditeiten met de hoogste kans op ziekenhuisopname of overlijden waren onder andere (nier)transplantatie, dialyse en chronische nierziekte.
Een onderzoek op basis van gegevens van een gezondheidszorgdatabase in de Verenigde Staten (n = 2246) naar de frequentie van en risicofactoren voor een gecompliceerd beloop van COVID-19 (onder andere ziekenhuisopname met acuut respiratoir falen, opname op IC en overlijden) na volledige vaccinatie liet zien dat het risico op een ernstig beloop hoger was bij patiënten ≥ 65 jaar, patiënten die immuungecompromitteerd waren en patiënten met een van de volgende aandoeningen: chronische longaandoening, chronische leverziekte, chronische nierziekte, chronische neurologische aandoening, diabetes mellitus of chronische hartziekte.
Conclusie
Hoge leeftijd en comorbiditeit geven een verhoogd risico op een gecompliceerd beloop van COVID-19. Het risico op een ernstig beloop door een onderliggende aandoening kan sterk uiteenlopen. Ondanks onderzoek is het exacte risico per aandoening niet goed in te schatten. Waarschijnlijk is de kans op een ernstig beloop van COVID-19 groter naarmate (het stadium van) de onderliggende aandoening ernstiger is.
De werkgroep is ten aanzien van comorbiditeit gekomen tot een lijst met aandoeningen op basis van de beschikbare literatuur en sluit in grote lijnen aan bij de LCI-richtlijn COVID-19 en de Gezondheidsraad.
Bij de kleine groep patiënten met een ernstig verminderde afweer geeft vaccinatie tegen COVID-19 geen of onvoldoende respons waardoor deze patiënten een verhoogd risico hebben op een ernstig beloop van COVID-19. De volgende patiënten vallen hieronder:
- Patiënten na orgaantransplantatie.
- Patiënten na beenmerg- of stamceltransplantatie (autoloog of allogeen)*.
- Patiënten die behandeling voor een kwaadaardige hematologische aandoening ondergaan of recent hebben ondergaan, waaronder CAR(Chimere Antigeen Receptor)-T cel therapie*.
- Patiënten met een hematologische maligniteit waarvan bekend is dat dit geassocieerd is met ernstige immuundeficiëntie (bijv. chronische lymfatische leukemie, multiple myeloom, ziekte van Waldenström)*.
- Patiënten met een solide tumor die in de laatste 6 maanden behandeld zijn met chemotherapie en/of radiotherapie**.
- Patiënten met ernstig nierfalen die door een specialist gecontroleerd worden, met eGFR <30ml/min 1.73m2 met immunosuppressiva.
- Patiënten met nierdialyse.
- Personen met een ernstig aangeboren afweerstoornis (primaire immuundeficiëntie) die door de NIV-NVII zijn aangemerkt als risicogroep.
- Patiënten die behandeld worden met de volgende immunosuppressiva:
- B-cel depleterende medicatie: anti-CD20 therapie, zoals rituximab, ocrelizumab;
- sterk lymfopenie-inducerende medicatie: fingolimod (of soortgelijke S1P agonisten), cyclofosfamide; mycofenolaatmofetil in combinatie met (langdurig gebruik van) 1 of meerdere andere immunosuppressiva.
* wanneer hiervoor onder behandeling of in de afgelopen 2 jaar hiervoor onder behandeling geweest.
** aangepast n.a.v. adviesnota RIVM omdat niet immunotherapie maar radiotherapie kans lijkt te geven op onvoldoende werkzaamheid van vaccinatie.
Etniciteit
Naar Samenvatting ›Bepaalde etnische minderheidsgroepen lijken meer kans te hebben om geïnfecteerd te worden met SARS-CoV-2. Hier zijn veel mogelijke verklaringen voor, zoals het leven in grotere huishoudens met meerdere generaties bij elkaar, vaker een laag sociaaleconomische status met grotere kans op kleine behuizing of accommodatie met gedeelde faciliteiten, vaker een beroep met minder mogelijkheden tot afstand houden of minder de gelegenheid om thuis te werken met daardoor meer kans op besmetting. Er is geen onbetwist bewijs dat een specifieke etniciteit een onafhankelijke risicofactor is voor een ernstig beloop van COVID-19.
In een systematische review en meta-analyse laten Sze et al. zien dat bepaalde etnische minderheidsgroepen meer kans hebben om geïnfecteerd te worden met SARS-CoV-2. Er is geen bewijs van hoge kwaliteit dat een specifieke etniciteit een onafhankelijke risicofactor is voor een ernstig beloop van COVID-19.
Zwangerschap en lactatie
Naar Samenvatting ›Kans op infectie
Naar Samenvatting ›Op basis van de huidige inzichten lijken zwangere vrouwen geen verhoogd risico te hebben om geïnfecteerd te worden met SARS-CoV-2. Transmissie van SARS-CoV-2 vindt waarschijnlijk, net als bij andere virale luchtweginfecties, niet plaats via borstvoeding.
Kans op ernstig beloop
Naar Samenvatting ›- COVID-19 kan, net als de meeste andere virale luchtweginfecties, ernstiger verlopen tijdens de zwangerschap, met name in het derde trimester (≥ 28 weken).
- Zwangere vrouwen met COVID-19 hebben, vooral in de tweede helft van de zwangerschap, meer kans dan niet-zwangere vrouwen op een ernstig beloop met IC-opname en invasieve beademing.
- Extra risicofactoren voor een ernstiger beloop van COVID-19 tijdens de zwangerschap zijn hoge BMI, comorbiditeit en hogere leeftijd van de zwangere vrouw.
- Vaccinatie wordt met nadruk geadviseerd aan alle zwangere vrouwen, ongeacht de termijn van de zwangerschap. Vaccinatie is veilig en effectief, en beschermt ook het kind doordat de antistoffen de placenta passeren.
Zwangerschapscomplicaties
Naar Samenvatting ›Een infectie met SARS-CoV-2 tijdens de zwangerschap geeft een toegenomen kans op pre-eclampsie, medische vroeggeboorte en intra-uteriene vruchtdood. Er zijn vooralsnog geen aanwijzingen dat SARS-CoV-2 de kans op een miskraam verhoogt.
Een ernstig beloop van COVID-19 bij vrouwen in de vruchtbare leeftijdsfase komt weinig voor. Vrouwen die tijdens de zwangerschap een infectie met SARS-CoV-2 doormaken, hebben echter een grotere kans dan niet-zwangere vrouwen om opgenomen te worden op de intensive care en hebben vaker invasieve beademing nodig (die kans was 2-3 × hoger bij de deltavariant, bij de omikronvariant is dit onbekend). Dit verhoogde risico geldt vooral in het tweede helft van de zwangerschap. Andere bekende risicofactoren voor een ernstig beloop tijdens de zwangerschap zijn hogere leeftijd, hoge BMI en comorbiditeit.
Vrouwen die tijdens hun zwangerschap COVID-19 doormaken, lijken vaker een vroeggeboorte te hebben dan zwangere vrouwen die geen COVID-19 doormaken. Het gaat daarbij echter vooral om medische of iatrogene vroeggeboorten; de kans op een spontane vroeggeboorte is niet toegenomen. Een SARS-CoV-2-infectie vergroot ook de kans op pre-eclampsie en intra-uteriene vruchtdood. Precieze percentages hieromtrent zijn niet te geven omdat er vooralsnog geen cijfers zijn over het aantal SARS-CoV-2-besmettingen in de totale zwangere populatie en de uitkomsten daarvan. Ook is er weinig bekend over SARS-CoV-2-besmettingen en het risico op een miskraam. Vooralsnog zijn er geen aanwijzingen dat de infectie het risico op een miskraam verhoogt.
Vaccinatie van zwangere vrouwen is van groot belang, omdat zwangere vrouwen meer risico hebben op een ernstig beloop van COVID-19 dan niet-zwangere vrouwen en omdat de ziekte bij hen ook het risico op zwangerschapscomplicaties verhoogt. Vaccinatie is veilig en effectief gebleken, en als de vaccinatie ≥ 3 weken voor de bevalling plaatsvindt, geeft de passage van antistoffen via de placenta ook bescherming aan het kind.
Kinderen
Naar Samenvatting ›- De besmettelijkheid neemt toe met de leeftijd.
- De ziekte verloopt bij kinderen in het algemeen veel milder dan bij volwassenen. Voor de meeste kinderen met een chronische aandoening lijkt een infectie met SARS-CoV-2 niet ernstiger te verlopen dan bij gezonde kinderen.
COVID-19 verloopt bij kinderen in het algemeen mild; zij hoeven bijna nooit opgenomen te worden in het ziekenhuis. Indien kinderen symptomatisch zijn, hebben zij dezelfde symptomen als volwassenen. De meest voorkomende klachten zijn koorts en hoesten. In 2020 was 0,7% van alle patiënten met COVID-19 in het ziekenhuis < 18 jaar, waarvan de meerderheid < 4 jaar. De Nederlandse vereniging voor Kindergeneeskunde (NVK) heeft voor kinderen < 18 jaar met onderliggend lijden separaat adviezen opgesteld. In zeldzame gevallen zal de behandelend kinderarts een aangepast advies geven.
Multisystem Inflammatory Syndrome – Children (MIS-C)
Naar Samenvatting ›- MIS-C is een zeer zeldzame, levensbedreigende ontstekingsreactie die op kan treden bij kinderen na doorgemaakte COVID-19.
- De complicatie MIS-C wordt enkele weken tot enkele maanden na doorgemaakte COVID-19 gezien. Het beeld begint vaak met koorts en de klachten nemen toe in ernst in de loop van enkele dagen.
- MIS-C kan zich uiten als:
- een beeld dat lijkt op de ziekte van Kawasaki (conjunctivitis of mucocutane inflammatie) (1)
- een beeld dat zich uit met cardiale betrokkenheid (onder andere hartfalen) en/of gastro-intestinale klachten (onder andere buikpijn) en/of coagulopathie (2)
- een mengbeeld van 1 en 2
- De cardiale problematiek kan na enkele dagen plots verergeren. Het buikbeeld kan imponeren als een acute buik.
MIS-C (Multisystem Inflammatory Syndrome – Children) is een ernstige ontstekingsreactie die kan optreden bij kinderen na COVID-19, waarbij meerdere orgaansystemen zijn aangedaan. Dit hyperinflammatiesyndroom wordt ook wel aangeduid als ‘paediatric multisystem inflammatory syndrome temporally related to SARS-CoV-2’ (PIMS-TS).
Achtergrond
Kort na de 'eerste golf' van de COVID-19-pandemie in het voorjaar van 2020 meldden meerdere landen een stijgende incidentie van een M. Kawasaki-achtig ziektebeeld bij kinderen, dat in verband werd gebracht met COVID-19. Een causale relatie is vooralsnog niet aangetoond, maar wegens het hoge aandeel COVID-19 positief geteste patiënten en de relatie in de tijd met de COVID-19-pandemie wordt inmiddels gesproken van een 'COVID-geassocieerd' syndroom.
Epidemiologie
In Nederland was er in september 2020 bij 30 patiënten de diagnose gesteld.
Klinisch beeld en beloop
- De complicatie MIS-C ontwikkelt zich meestal 2 tot 6 weken na COVID-19, maar kan zich ook nog na langere tijd (maanden) manifesteren.
- Het ziektebeeld kenmerkt zich door een ontstekingsreactie waarbij meerdere orgaansystemen betrokken kunnen zijn.
- Patiënten krijgen veelal eerst koorts en worden toenemend ziek in de daaropvolgende dagen. Afhankelijk van het betrokken orgaansysteem kan MIS-C zich uiten als:
- een beeld dat lijkt op de ziekte van Kawasaki: rash, bilaterale non-purulente conjunctivitis of mucocutane inflammatie (mond, handen of voeten)
- een beeld dat zich uit met cardiale betrokkenheid (onder andere hartfalen) en/of gastro-intestinale klachten (diarree, braken of buikpijn) en/of tekenen van co-agulopathie
- een mengbeeld van bovenstaande
De buikklachten kunnen zo ernstig zijn dat het imponeert als een acute buik. De cardiale problemen kunnen na enkele dagen plots verergeren.
Veelvoorkomende symptomen bij MIS-C
- Persisterende koorts > 38,5 °C
- Hoofdpijn
- Buikpijn, braken en/of diarree
- Verwardheid
- Conjunctivitis
- Collaps
- Hoesten, keelpijn en/of respiratoire klachten
- Lymfadenopathie
- Zuurstofbehoefte
- Huiduitslag
- Pijn op de borst
- Roodheid van de tong, lippen en/of farynx
- Hypotensie (cardiogene en/of vasoplege shock)
- Vervellingen en/of zwelling extremiteiten
Differentiaaldiagnose
De differentiaaldiagnose bevat andere (zeldzame) veelal infectieuze dan wel inflammatoire aandoeningen, zoals (incomplete) M. Kawasaki, Toxic Shock Syndroom, sepsis, macrofagen activatie syndroom (MAS), virale myocarditis, HLH, SLE, systemische JIA, systemische vasculitiden en hematologische maligniteiten.
Diagnose
De diagnose MIS-C wordt gesteld in de tweede lijn. De WHO heeft de volgende casusdefinitie opgesteld:
- Kinderen en adolescenten 0-19 jaar met koorts ≥ 3 dagen
- EN 2 van de volgende kenmerken:
- Rash of bilaterale non-purulente conjunctivitis of mucocutane inflammatie (mond, handen of voeten)
- Hypotensie/shock
- Tekenen van mycarddysfunctie: pericarditis, valvulitis, coronairafwijkingen (inclusief echografische bevindingen of verhoogd troponine/NT-proBNP)
- Tekenen van coagulopathie (PT, APTT, D-dimeren)
- Acute gastro-intestinale verschijnselen (diarree, braken of buikpijn)
- EN verhoogde inflammatiemarkers (BSE, CRP of calcitonine)
- EN geen andere voor de hand liggende microbiële verwekker van inflammatie, zoals bacteriële sepsis, stafylokokken of streptococcen toxic shock syndroom
- EN bewijs van COVID-19 (RT-PCR, antigeentest of serologie), of gedocumenteerd contact met COVID-19-patiënt.
Conclusie
MIS-C is een postinfectieuze, zeer zeldzame, maar levensbedreigende complicatie van COVID-19 op de kinderleeftijd.
Richtlijnen diagnostiek
Naar Samenvatting ›Patiënten met COVID-19 presenteren zich met een verscheidenheid aan klachten (zie Klinisch beeld). De aanbevelingen in deze standaard zijn aanvullend op reeds bestaande NHG-Standaarden.
Spoed
Naar Samenvatting ›Gebruik bij twijfel over de klinische stabiliteit van de patiënt de ABCDE-systematiek. Wanneer de patiënt ABCDE-instabiel is zie NHG-Behandelrichtlijn Geneesmiddelen en zuurstof in spoedeisende situaties.
Anamnese
Naar Samenvatting ›De ingangsklacht(en) kan/kunnen zeer verschillend zijn.
Vraag naar:
- koorts
- hoesten
- verkoudheidsklachten, keelpijn
- kortademigheid/benauwdheid, vermoeidheid/inspanningstolerantie. Vraag concreet naar bijvoorbeeld toiletgang, traplopen, verschil in inspanningstolerantie ten opzichte van de vorige dag
- plotseling verlies van smaak- en/of reukvermogen (zonder neusverstopping)
Vraag, afhankelijk van de ingangsklacht(en) en de ernst van de klachten, naar meer of minder van mogelijk bijkomende klachten:
- algemene klachten: koude rillingen, algehele malaise, spierpijn, algehele pijnklachten
- gastro-intestinale klachten: buikpijn, verlies van eetlust, diarree, overgeven, misselijkheid
- centraal zenuwstelsel: hoofdpijn, duizeligheid, prikkelbaarheid/verwardheid/delier
- overig: oculaire pijn, conjunctivitis, huidafwijkingen
Vraag daarnaast naar:
- duur van de klachten en of er sprake is van een snelle achteruitgang.
- risicofactoren voor een ernstig beloop (zie Risicogroepen)
- vaccinatiestatus COVID-19
Besteed aandacht aan de zorgen van de patiënt en ga na wat de hulpvraag is:
- angst voor COVID-19
- gevolgen voor de werksituatie, thuissituatie en eventuele (thuis)zorg
- behandelwensen van de patiënt (zoals wel/geen ziekenhuisopname)
Patiënten met COVID-19 ervaren relatief weinig klachten van kortademigheid, terwijl er toch sprake kan zijn van hypoxemie; mogelijk geven vermoeidheid en verminderde inspanningstolerantie hier een betere indruk van.
Lichamelijk onderzoek
Naar Samenvatting ›Algemeen
Naar Samenvatting ›- Beoordeel de algemene toestand en mate van ziek zijn, waaronder koorts, verwardheid en sufheid. Let op tekenen van dehydratie.
- Bepaal zuurstofsaturatie, adem- en hartfrequentie en zo nodig de bloeddruk.
- De saturatie geeft een indruk van de ernst van COVID-19. Een niet-benauwd ogende patiënt met een normale of licht verhoogde ademhalingsfrequentie kan toch een (zeer) lage saturatie hebben. Meet bij twijfel de saturatie nogmaals nadat de patiënt zich kort heeft ingespannen.
- Vergelijk de situatie zo mogelijk met eerdere dagen.
Betrouwbaarheid van saturatiemeting
De belangrijkste factoren die de betrouwbaarheid van een meting met een saturatiemeter beïnvloeden zijn:
- de accuratesse van de meter
- de omstandigheden waarin de meting wordt afgenomen
Omstandigheden
Voorbereiding
- Meet binnenshuis en in rust.
- Verwijder zo nodig nagellak.
- Verwarm koude vingers voor de meting.
Meting
- Gebruik bij voorkeur de wijs- of middelvinger.
- Meet gedurende 30-60 seconden en neem de meest voorkomende waarde.
- Herhaal de meting bij een afwijkende waarde.
- Gebruik alleen waarden als er ook een sterk hartslagsignaal is.
In de paragraaf ‘Lichamelijk onderzoek’ zijn geen verrichtingen opgenomen specifiek gericht op kinderen. Het overgrote deel van de kinderen met COVID-19 heeft milde klachten en deze paragraaf zal daarom met name gebruikt worden voor volwassenen. Voor de beoordeling van de mate van ziek zijn bij kinderen, verwijzen we naar de NHG-Standaard Acuut hoesten.
Symptomen die passen bij een bovensteluchtweginfectie
Naar Samenvatting ›Onderzoek het kno-gebied op geleide van de anamnese.
Symptomen die passen bij een ondersteluchtweginfectie
Naar Samenvatting ›Onderzoek de longen. Let hierbij op:
- mogelijke aanwijzingen voor een pneumonie, verslechtering of longaanval astma/COPD of andere aandoening
- longgeluiden en lokale afwijkingen (pleurawrijven, crepitaties, éénzijdige auscultatoire afwijking, demping (zie ook NHG-Standaard Acuut hoesten))
Overig
Naar Samenvatting ›Verricht zo nodig ander lichamelijk onderzoek op geleide van de anamnese.
Aanvullend onderzoek
Naar Samenvatting ›Voor de diagnostiek naar COVID-19 kan onderscheid gemaakt worden tussen testen naar een acute infectie met SARS-CoV-2 (PCR-test en antigeensneltest met behulp van een neus(keel)uitstrijk) en testen naar een in het verleden doorgemaakte COVID-19 (serologische antilichaamtest in het bloed).
Diagnostiek naar acute infectie SARS-CoV-2
Naar Samenvatting ›- Verricht diagnostiek naar COVID-19 bij een vermoeden van COVID-19, wanneer de diagnose consequenties heeft voor het beleid. Zoals het eventueel starten met nirmatrelvir/ritonavir; of dexamethason, zuurstof en tromboseprofylaxe.
- Om de diagnose COVID-19 te stellen bij patiënten met klachten in de huisartsenpraktijk heeft de PCR-test de voorkeur boven de antigeensneltest. Indien een snelle diagnose gewenst is, bijvoorbeeld voor het verdere medische beleid of voor de organisatie van de zorg, kan een antigeensneltest ingezet worden.
- Houd rekening met een foutnegatieve testuitslag. Overweeg bij aanhoudende klachten (opnieuw) een PCR-test af te nemen bij een sterk vermoeden van COVID-19.
Landelijk testbeleid
Sinds 1 juni 2020 is het landelijk beleid dat iedereen met vermoeden van COVID-19 zich kan laten testen door de GGD. Met de GGD zijn afspraken gemaakt wie welke patiënten test. Zie voor meer informatie over de rolverdeling de Leidraad uitvoering testen op COVID-19 bij patiënten extramuraal.
Diagnostiek naar acute infectie
De klinische sensitiviteit van PCR naar SARS-CoV-2 wordt geschat op ongeveer 70-90%. De betrouwbaarheid van deze test wordt beïnvloed door meerdere factoren, waaronder de ziektedag en de afnametechniek. De PCR-test wordt gezien als de gouden standaard in de diagnostiek naar SARS-CoV-2. De sensitiviteit van een PCR-test is hoger dan die van een antigeensneltest. Patiënten die getest worden in de huisartsenpraktijk zijn patiënten die gezien worden omdat een klinische inschatting gewenst is. Betrouwbare diagnostiek is bij deze patiënten daarom extra van belang. De PCR-test heeft daarom de voorkeur boven de antigeensneltest.
PCR-diagnostiek (praktische uitvoering)
Naar Samenvatting ›Neem een keel- en neusuitstrijk af in de acute fase (grofweg de eerste week). Kijk voor de juiste afnametechniek op de LCI-website.
Betrouwbaarheid PCR-test
- PCR naar SARS-CoV-2 in neus- en keelswabs is het meest sensitief in de acute fase (deze fase loopt tot 6 tot 9 dagen na het ontstaan van de klachten).
- Een test kan al afgenomen worden op de eerste ziektedag.
- De klinische sensitiviteit van PCR naar SARS-CoV-2 wordt geschat op ongeveer 70-90%, de specificiteit op minimaal 95%.
- De betrouwbaarheid van de test wordt beïnvloed door een aantal factoren:
- stadium van de ziekte
- ernst van de symptomen
- het moment van monstername ten opzichte van de start van klachten
- het soort patiëntmateriaal (bijvoorbeeld neus- en/of keelmonster, of dieper uit de luchtwegen, zoals sputum of bronchoalveolaire lavage (BAL))
- de juiste afnametechniek
- het soort wattenstok en transport medium en bewaar- en transportcondities
Uitvoering
Om materiaal te besparen is het mogelijk om met 1 wattenstok zowel neus als keel te bemonsteren of 2 wattenstokken in 1 buis met verzendmedium te versturen.
Antigeensneltest en antigeenzelftest (praktische uitvoering)
Naar Samenvatting ›Neem een neus(keel)uitstrijk af in de acute fase (grofweg de eerste week) en bij voorkeur tijdens de eerste ziektedagen.
Wat is een antigeensneltest?
Een antigeensneltest toont met antilichamen, op 1 specifiek moment, de aanwezigheid van viruseiwit (antigeen) aan in materiaal dat is verkregen met een uitstrijk uit de (keel- en) neusholte.
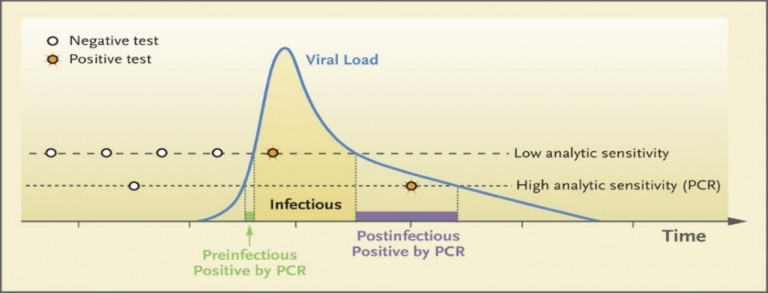
Antigeensneltesten detecteren virussen bij personen met een grotere hoeveelheid virusdeeltjes. Dit zijn de personen die potentieel, op dat moment, als het meest besmettelijk worden beschouwd (zie figuur 1).
Testeigenschappen
De antigeensneltesten die tot nu toe geëvalueerd zijn in een (voornamelijk) mild symptomatische populatie geven gemiddeld 0 tot 33% fout-negatieve uitslagen ten opzichte van de PCR-test. Als er alleen gekeken wordt naar monsters met een relatief hoge hoeveelheid virusdeeltjes (Cycle Treshold (Ct)-waarde < 30), is het percentage fout-negatieve uitslagen sterk gereduceerd (~ 5 tot 10%). De sensitiviteit van de antigeensneltesten is het hoogst rondom het begin van de klachten. Bij personen met langer durende klachten (langer dan een week) daalt de sensitiviteit aanzienlijk. De specificiteit van antigeensneltesten is hoog; een positieve antigeensneltest wordt daarom als betrouwbaar beschouwd.
Landelijk beleid
Antigeensneltesten worden op dit moment vooral ingezet in de GGD-teststraten voor de screening van personen met milde klachten. Personen die in de zorg werken, personen die in contact staan met kwetsbare personen en personen die deel uitmaken van een bron- en contactonderzoek krijgen in de GGD-teststraat in principe de gevoeligere PCR-test.
Ook bij ernstig zieke of kwetsbare personen bij wie er een vermoeden is van COVID-19 heeft de PCR-test de voorkeur. Indien er bij deze personen een antigeensneltest is uitgevoerd, adviseert het RIVM om bij een negatieve testuitslag deze uitslag te controleren met een PCR-test.
Antigeensneltesten in de huisartsenpraktijk
De huisarts verricht diagnostiek naar COVID-19 bij patiënten bij wie een klinische inschatting gewenst is. Dit kan met een PCR-test. Indien een snelle diagnose gewenst is, bijvoorbeeld voor het verdere medische beleid of voor de organisatie van de zorg, kan de huisarts een antigeensneltest uitvoeren.
Conclusie
Antigeensneltesten zijn in staat om COVID-19 aan te tonen bij personen met een verhoogde hoeveelheid virusdeeltjes. De grootste piek wordt gezien rondom de eerste ziektedag. Na de eerste ziektedagen neemt de sensitiviteit van antigeensneltesten af.
Voor het stellen van de diagnose COVID-19 bij personen met klachten in de huisartsenpraktijk heeft de PCR-test de voorkeur boven de antigeensneltest. Indien een snelle diagnose gewenst is, bijvoorbeeld voor het verdere medische beleid of voor de organisatie van de zorg, kan de huisarts een antigeensneltest inzetten.
Randvoorwaarden voor het uitvoeren van antigeensneltesten
- De test heeft een CE-markering.
- De test is gevalideerd* voor de doelgroep en het doel.
- De (keel-/)neusuitstrijk wordt afgenomen door een goed geïnstrueerde persoon in volledige PBM.
- De uitvoer van de antigeensneltest vindt plaats in een flowkast of door personeel in volledige PBM.
- De uitvoerende instantie draagt er zorg voor dat monsters en cassette ondubbelzinnig traceerbaar zijn tot een geïdentificeerd persoon.
- De uitvoerende instantie draagt er zorg voor dat gebruikt afnamemateriaal en antigeencassettes als biologisch besmet materiaal afgevoerd worden. In de huisartsenpraktijk conform de richtlijn infectiepreventie (als materiaal met infectierisico), zie bijlage B en C op https://www.nhg.org/themas/publicaties/infectiepreventief-handelen-specifieke-situaties-de-praktijk.
- Testresultaten worden vastgelegd in een (laboratorium)informatiesysteem.
- Zoals bij elk Point of Care (POC)-gebruik maakt de uitvoerende instantie afspraken over wie waarvoor verantwoordelijk is. Zie ook de Richtlijn point of care testing (POCT) in de huisartsenzorg.
- Bij de uitvoerende instantie is adequate kennis aanwezig om de testresultaten te interpreteren en vervolgacties uit te zetten (zoals noodzaak aanvullende PCR-test, quarantaineplicht en besmettelijkheid). De huisarts is ter plekke beschikbaar voor overleg en ondersteuning.
- De uitvoerende instantie draagt zorg voor goede (schriftelijke), tijdige communicatie naar de geteste persoon over het testresultaat en de interpretatie ervan.
* In de Rapportage Status validatie SARS-CoV-2 Antigeen sneltesten (versie 27 mei 2021 > tabel 3) staan antigeensneltesten vermeld die zijn gevalideerd door ISO 15189 geaccrediteerde laboratoria voor mensen met klachten passend bij COVID-19. Er lopen meerdere validatiestudies voor antigeensneltesten naar COVID-19.
Antigeenzelftests zijn antigeensneltests die afgenomen zijn door de patiënt zelf. Per 3 december 2021 is het landelijke beleid rondom zelftests voor COVID-19 aangepast en doen de meeste mensen bij klachten een zelftest. Alleen voor specifieke groepen wordt geadviseerd een COVID-19-test bij de GGD-teststraat te laten afnemen. Ook kan bij de GGD een confirmatietest worden gedaan na een positieve zelftest.
De sensitiviteit van antigeensneltests die door de patiënt zelf zijn afgenomen is 49-97% ten opzichte van de PCR-test. De sensitiviteit is hoger als alleen naar hogere viral loads (lagere CT-waarden) gekeken wordt; de laagste sensitiviteit stijgt dan van 49 naar 80%. Ook laat onderzoek zien dat de sensitiviteit hoger is bij patiënten met klachten dan bij patiënten zonder klachten. De specificiteit van een zelftest is 82-100%, waarbij de meeste onderzoeken een specificiteit > 98% laten zien.
Bij een lage prevalentie van SARS-CoV-2 zal de negatief voorspellende waarde van de test hoger zijn. De positief voorspellende waarde is dan echter lager. Bij een hoge prevalentie stijgt de positief voorspellende waarde, terwijl de negatief voorspellende waarde daalt. Zie voor rekenvoorbeelden de LCI-bijlage Aanvullende informatie diagnostiek COVID-19.
In sommige gevallen zullen patiënten met COVID-19-klachten contact opnemen met de huisartsenpraktijk op basis van een positieve zelftest. Bij patiënten die u ziet omdat een klinische inschatting gewenst is, kan een snelle diagnose van belang zijn voor bijvoorbeeld het verdere medische beleid of de organisatie van de zorg. Ook met een positieve antigeenzelftest (een in Nederland gevalideerde antigeen(snel)test afgenomen door de patiënt zelf) kan een infectie met SARS-CoV-2 vastgesteld worden.
Houd rekening met een foutnegatieve testuitslag. Indien van belang voor het behandelbeleid, blijft de PCR-test de voorkeur houden boven een antigeensneltest, aangezien de PCR-test sensitiever is dan de antigeensneltest. Overweeg daarom bij een sterk vermoeden van COVID-19 en een negatieve antigeenzelftest om een PCR-test af te nemen.
Serologische diagnostiek naar doorgemaakte COVID-19
Naar Samenvatting ›We bevelen het aantonen van antistoffen tegen COVID-19 in het bloed (serologische diagnostiek) niet aan.
Inleiding
Er worden verschillende serologische testen (‘immuniteitstesten’) aangeboden om te bepalen of iemand COVID-19 heeft doorgemaakt. Het gaat zowel om een laboratoriumtest (veneuze bloedafname) als om een point-of-care test (POCT/sneltest, vingerprik), waarbij de uitslag binnen enkele minuten bekend is.
Het doel van serologische diagnostiek is het aantonen van antilichamen (immuunreactie). Dit is dus anders dan het doel van een PCR-test, waarbij het gaat om het aantonen of uitsluiten van een huidige infectie met COVID-19.
Serologische diagnostiek in het laboratorium
Landelijk zijn verschillende serologische tests (IgM/IgG) onderzocht onder leiding van artsen-microbiologen en het RIVM, verenigd in de Taskforce serologie. De hoogste gevoeligheid van een serologische laboratoriumtest werd gevonden zo’n 4 weken na het begin van de klachten.
Point-of-care tests (sneltesten)
Sneltests op COVID-19-antilichamen blijken onvoldoende betrouwbaar voor gebruik in de huisartsenpraktijk.
Beperkingen serologische diagnostiek naar antilichamen
Serologische diagnostiek kent een aantal beperkingen:
- Het duurt enige tijd voordat antilichamen gevormd zijn. Het lijkt erop dat het tot een maand na de eerste ziektedag duurt totdat > 90% van de geïnfecteerden met COVID-19 antilichamen gevormd heeft.
- Een deel van de met SARS-CoV-2 geïnfecteerde mensen die asymptomatisch zijn gebleven of slechts milde klachten hebben gehad, lijkt nauwelijks of geen antilichamen te vormen.
- Antilichamen verdwijnen vaak na enige tijd. De snelheid waarmee antilichamen verdwijnen is onderhevig aan persoonlijke variatie en is afhankelijk van de ziekteverwekker en de ernst van de doorgemaakte infectie.
De interpretatie van serologische antilichaamtests is dus afhankelijk van een aantal factoren, zoals de fase van de ziekte, de mate van ziek zijn én de validatie van de gebruikte laboratoriumtest. Interpretatie van serologische antilichaamtests gebeurt dan ook bij voorkeur door een expert (de medisch microbioloog van het laboratorium).
Plaats van serologische diagnostiek naar antilichamen voor doorgemaakte COVID-19 in de huisartsenpraktijk
In de huisartsenpraktijk zal de vraag naar serologische diagnostiek met name aan de orde zijn bij patiënten met persisterende klachten na mogelijke COVID-19, bij wie geen PCR verricht is of deze negatief was. Een serologische test naar doorgemaakte COVID-19 heeft in de huidige fase echter geen meerwaarde meer.
- Het overgrote deel van de bevolking heeft antistoffen tegen SARS-CoV-2 in het bloed. In het voorjaar van 2022 had, volgens het PIENTER coronaonderzoek van het RIVM, ongeveer 95% van de bevolking antistoffen in het bloed. Bij ongeveer 60% van de bevolking werd bewijs van infectie in het bloed aangetroffen.
- Aantonen van antistoffen laat niet zien wanneer een SARS-CoV-2-infectie is doorgemaakt.
Serologische diagnostiek om vast te stellen of antistoffen tegen SARS-CoV-2 ontbreken
In de tweede (of derde) lijn kan het ontbreken van antistoffen tegen SARS-CoV-2 bij patiënten met een zeer hoog risico op een ernstig beloop meegewogen worden in de keuze om te behandelen met nirmatrelvir/ritonavir.
Diagnostiek naar DVT en longembolie
Naar Samenvatting ›- Bij een vermoeden van een DVT of longembolie: bepaal de risicoscore volgens de beslisregels (zie NHG-Standaard Diepveneuze trombose en longembolie).
- Verricht bij patiënten met COVID-19 alleen een D-dimeertest bij een klinisch vermoeden van DVT of longembolie. Bij een hoge score op de beslisregel is een D-dimeertest niet nodig; zie voor vervolgstappen de NHG-Standaard Diepveneuze trombose en longembolie.
- Hoewel een negatieve D-dimeer minder vaak voor zal komen bij COVID-19, sluit een lage score op de beslisregel in combinatie met een negatieve D-dimeer VTE vrijwel uit. Een positieve D-dimeer moet gevolgd worden door nader radiologisch onderzoek. Zie verder de NHG-Standaard Diepveneuze trombose en longembolie.
De strategie van een beslisregel in combinatie met een D-dimeertest is niet gevalideerd voor patiënten met (een hoge verdenking op) COVID-19. Bij patiënten met COVID-19 is het te verwachten dat de D-dimeertest vaker positief zal zijn door de infectie. De negatief voorspellende waarde is echter nog altijd hoog. Een lage score op de beslisregel in combinatie met een negatieve D-dimeer sluit VTE vrijwel uit. Een positieve D-dimeer moet gevolgd worden door nader radiologisch onderzoek. Zie verder de NHG-Standaard Diepveneuze trombose en longembolie.
Diagnostiek bij patiënten met acuut hoesten
Naar Samenvatting ›- CRP: zie voor de indicaties en de interpretatie en consequenties voor het beleid de NHG-Standaard Acuut hoesten.
- X-thorax: zie voor de indicaties de NHG-Standaard Acuut hoesten. Overleg van tevoren met het ziekenhuis vanwege de te nemen isolatiemaatregelen.
Evaluatie
Naar Samenvatting ›- Stel de diagnose COVID-19 bij klachten passend bij COVID-19 en een positieve PCR- of antigeensneltest (ook zelf-afgenomen).
- Bij een positieve SARS-CoV-2-test en afwezigheid van klachten is er sprake van een a- of presymptomatische SARS-CoV-2-besmetting.
Differentiaaldiagnose (niet uitputtend)
Naar Samenvatting ›De differentiële diagnostiek bij vermoeden van COVID-19 of complicaties daarvan kan moeilijk zijn. Hieronder staan enkele ziektebeelden met klachten die kunnen lijken op COVID-19 of kunnen samengaan met COVID-19. De diagnostiek en het beleid van deze aandoeningen vallen buiten het bestek van deze standaard.
Luchtweginfectie door verwekker anders dan SARS-COV-2
Naar Samenvatting ›Koorts, hoesten, verkoudheidsklachten, eenzijdige auscultatoire afwijkingen; zie NHG-Standaard Acuut hoesten.
Longembolie
Naar Samenvatting ›Onverklaard en relatief plotselinge toename van benauwdheid; benauwdheid en een tachycardie (arbitrair > 100 per minuut); zie NHG-Standaard Diepveneuze trombose en longembolie.
Acuut coronair syndroom
Naar Samenvatting ›Plotselinge (toename van) (hevige) retrosternale pijn, al dan niet met uitstraling, zeker indien het gepaard gaat met vegetatieve verschijnselen; bij ouderen en patiënten met diabetes mellitus ook bij plotseling optredende dyspneu; zie NHG-Standaard Acuut coronair syndroom.
Hartfalen
Naar Samenvatting ›Kortademigheid, orthopneu, verminderde inspanningstolerantie, vermoeidheid, zwelling van de enkels; zie NHG-Standaard Hartfalen.
Longaanval astma/COPD
Naar Samenvatting ›Toename van dyspneuklachten, hoesten of piepen, auscultatoire afwijkingen bij bekende astma of COPD; zie NHG-Standaarden COPD, Astma bij volwassenen en Astma bij kinderen.
Richtlijnen beleid
Naar Samenvatting ›Voorlichting en advies
Naar Samenvatting ›Voorlichting over de aandoening
Naar Samenvatting ›- Informeer de patiënt over het te verwachten beloop. COVID-19 is een virale luchtweginfectie en kent een wisselend beloop. In de meeste gevallen verloopt de ziekte mild tot matig ernstig. Bij een klein deel van de COVID-19-patiënten verloopt de infectie ernstig en kan een ziekenhuisopname en soms IC-opname noodzakelijk zijn, een heel klein deel overlijdt. De kans op een ernstig beloop is afhankelijk van de leeftijd en de aanwezigheid van risicofactoren en is het hoogst bij de oudste ouderen en kwetsbare ouderen.
- Leg uit dat in sommige gevallen een verslechtering optreedt. De patiënt kan dit herkennen door achteruitgang die vooral gekenmerkt wordt door kortademigheid, ernstige vermoeidheid en/of beperkte inspanningstolerantie. Dit zijn redenen om direct contact op te nemen met de huisarts.
- Vraag de patiënt ook contact op te nemen bij verwardheid en bij verergering of aanhoudende klachten.
- Adviseer voldoende vochtinname.
- Adviseer patiënten die bedlegerig zijn om regelmatig even te bewegen, bijvoorbeeld door 2 tot 3 keer per dag 5 tot 10 minuten uit bed te komen.
- Leg uit dat de ziekte en de herstelfase lang kunnen duren. Een klein deel van de patiënten houdt langdurig (> 4 weken) klachten na het doormaken van COVID-19.
Voorlichting over voeding
Naar Samenvatting ›Patiënten met COVID-19 verkeren regelmatig in ondervoede toestand doordat ze van uitputting en vermoeidheid nauwelijks nog eten en drinken.
- Leg aan patiënten uit dat zij voldoende blijven eten en drinken. Hun voedingstoestand is van invloed op hun herstel.
- Overweeg om laagdrempelig de diëtiste te consulteren voor bijvoorbeeld het inzetten van drinkvoeding.
Thuisarts
Naar Samenvatting ›- Verwijs naar de informatie over COVID-19 op thuisarts.nl. De informatie op Thuisarts is gebaseerd op deze NHG-Standaard.
- Of verwijs naar de website van Pharos met eenvoudige uitleg en afbeeldingen over COVID-19 en informatie over COVID-19 in andere talen.
Medicamenteuze behandeling
Naar Samenvatting ›Voor het beleid bij zuurstofbehoeftige patiënten met een opname-indicatie, met wie u overeengekomen bent dat ziekenhuisopname niet gewenst is, en bij wie herstel het uitgangspunt is, zie Beleid bij zuurstofbehoeftige, niet-terminale patiënten die niet opgenomen willen worden.
Algemeen
Naar Samenvatting ›Schrijf geen middelen voor waarvan de werkzaamheid (nog) niet is aangetoond (zie Niet aanbevolen overige medicamenteuze behandelingen).
Symptoombestrijding
Naar Samenvatting ›Adviseer bij de symptoombestrijding van griepachtige klachten, zoals keel- of spierpijn, zo nodig paracetamol en als tweede keus NSAID’s conform de NHG-Standaard Pijn.
Het lijkt niet aannemelijk dat het gebruik van NSAID’s het herstel van COVID-19 vertraagt.
Nirmatrelvir/ritonavir
Naar Samenvatting ›We bevelen behandeling met nirmatrelvir/ritonavir niet aan bij patiënten met COVID-19, met uitzondering van de hieronder genoemde groepen patiënten.
Patiënten met een sterk verhoogd risico op een ernstig beloop
- Overweeg nirmatrelvir/ritonavir alleen bij de zeer kleine groep niet-zwangere volwassen patiënten met een sterk verhoogd risico op een ernstig beloop, die contact opnemen met de huisarts vanwege klachten die ≤ 5 dagen bestaan, EN die:
- een ernstig verminderde afweer hebben en onder behandeling zijn bij een medisch specialist, ongeacht vaccinatiestatus (bijvoorbeeld patiënten met een tekort aan afweerstoffen of na een orgaantransplantatie, zie Risicogroepen; vaak zal het voorschrijven van nirmatrelvir/ritonavir bij deze groep via de behandelend specialist gaan).
OF - verondersteld SARS-CoV-2-naïef zijn (ongevaccineerd en COVID-19 niet doorgemaakt) EN een sterk verhoogd risico hebben op een ernstig beloop door comorbiditeit of klinische conditie (bijvoorbeeld kwetsbare ouderen of patiënten met een ernstige cardiale of pulmonale aandoening)
- een ernstig verminderde afweer hebben en onder behandeling zijn bij een medisch specialist, ongeacht vaccinatiestatus (bijvoorbeeld patiënten met een tekort aan afweerstoffen of na een orgaantransplantatie, zie Risicogroepen; vaak zal het voorschrijven van nirmatrelvir/ritonavir bij deze groep via de behandelend specialist gaan).
- Overleg laagdrempelig met de internist of longarts en verwijs zo nodig voor eventuele diagnostiek (naar antistoffen) en/of behandeling.
- Overleg, indien er een indicatie voor nirmatrelvir/ritonavir is, laagdrempelig met de apotheker en/of de internist of longarts in verband met de vele interacties. Neem de relevante interacties en de risicofactoren voor een ernstig beloop mee in de afweging om nirmatrelvir/ritonavir voor te schrijven.
- Bespreek de voor- en nadelen met de patiënt: de combinatie nirmatrelvir/ritonavir verlaagt mogelijk de kans op ziekenhuisopname of overlijden; nadelen zijn bijwerkingen zoals dysgeusie (smaakstoornis) en misselijkheid, de zeer beperkte gegevens over de veiligheid en de potentieel ernstige interacties met andere medicijnen.
Praktische toepassing
- Ga het medicatiegebruik van de patiënt na (inclusief vrij verkrijgbare medicijnen en kruidensupplementen zoals sint-janskruid) om te beoordelen of er sprake is van een interactie met nirmatrelvir/ritonavir (zie kader Interacties van nirmatrelvir/ritonavir). Bij relevante interacties: overleg met apotheker en/of internist of longarts.
- Geef bij behandeling nirmatrelvir 2 dd 300 mg tegelijkertijd met ritonavir 2 dd 100 mg gedurende 5 dagen (combinatieverpakking met per dag 1 blister). Evalueer bijwerkingen en meld deze (of laat deze melden) bij Lareb.
- Start de behandeling zo snel mogelijk, uiterlijk 5 dagen na begin van de klachten en onafhankelijk van de ernst van de klachten.
- Bij verminderde nierfunctie:
- eGFR 30-60 ml/min/1,73 m2: geef nirmatrelvir 2 dd 150 mg tegelijkertijd met ritonavir 2 dd 100 mg gedurende 5 dagen
- eGFR < 30 ml/min/1,73 m2: vermijd gebruik
- Bij ernstig verminderde leverfunctie: vermijd gebruik.
- Bij (wens tot) zwangerschap of borstvoeding:
- gebruik geen nirmatrelvir/ritonavir tijdens zwangerschap
- geef geen borstvoeding tijdens en ≤ 7 dagen na afloop van de behandeling
- adviseer niet zwanger te worden tijdens en ≤ 7 dagen na afloop van de behandeling.
- Nirmatrelvir/ritonavir verlaagt mogelijk de kans op ziekenhuisopnames of sterfte bij niet-opgenomen ongevaccineerde volwassenen met COVID-19 met een (licht) verhoogd risico op een ernstig beloop. Er zijn beperkte gegevens over de veiligheid op korte termijn en het ontbreekt aan gegevens over de veiligheid op (middel)lange termijn.
- Hoewel er nog geen RCT gepubliceerd is over de effectiviteit van nirmatrelvir/ritonavir bij gevaccineerde COVID-19-patiënten op het moment dat de omikronvariant de dominant circulerende stam is, weten we uit observationeel onderzoek dat het absolute voordeel van nirmatrelvir/ritonavir bij deze patiënten mogelijk klein zal zijn en niet klinisch relevant (de werkgroep heeft een klinisch relevant verschil vastgesteld van > 3% absolute daling voor ziekenhuisopname). Het effect van nirmatrelvir/ritonavir is mogelijk alleen klinisch relevant in de groep patiënten die niet-immuun zijn (ongevaccineerd en geen COVID-19 doorgemaakt) met een verhoogd risico op een ernstig beloop.
- De werkgroep geeft op basis van de momenteel beschikbare gegevens een sterk negatieve aanbeveling voor de combinatie nirmatrelvir/ritonavir in de huisartsenpraktijk. Hoewel het middel mogelijk effectief is, is de kans op ziekenhuisopname of overlijden bij de meeste COVID-19-patiënten dermate laag dat het absolute effect van het middel bij deze patiënten te klein is om klinisch relevant te zijn. Dit geldt zeker in het licht van dat het merendeel van de Nederlandse populatie ondertussen een vorm van immuniteit tegen COVID-19 heeft ontwikkeld door vaccinatie of het doormaken van COVID-19, in combinatie met de huidige omikronvariant.
- Voor een kleine groep patiënten met een sterk verhoogd risico op een ernstig beloop is de werkgroep van mening dat het voorschrijven van nirmatrelvir/ritonavir overwogen kan worden. Het kan dan bijvoorbeeld gaan om SARS-CoV-2-naïeve patiënten (ongevaccineerd en geen COVID-19 doorgemaakt) met een ernstige cardiale of pulmonale aandoening die ondanks medicatie een grote kans hebben op decompensatie, om SARS-CoV-2-naïeve kwetsbare ouderen en om patiënten met een ernstig verminderde afweer die onder behandeling zijn bij een medisch specialist (zie voor deze laatste groep het advies over nirmatrelvir/ritonavir in de SWAB-richtlijn Medicamenteuze behandeling voor patiënten met COVID-19).
- Er zijn veel interacties met andere medicijnen en een deel daarvan is potentieel ernstig. De werkgroep is van mening dat per individuele patiënt de interacties die naar verwachting relevant zijn moeten worden meegenomen in de overweging of de voordelen opwegen tegen de nadelen van nirmatrelvir/ritonavir.
- Zoals geldt voor alle nieuwe geneesmiddelen, komt ook nirmatrelvir/ritonavir onder aanvullende monitoring te staan wanneer het in de handel is. Bijwerkingen kunnen gemeld worden bij Lareb.
Voor- en nadelen
Mogelijk verlaagt nirmatrelvir/ritonavir de kans op ziekenhuisopname of overlijden, indien gestart wordt ≤ 5 dagen na de start van de symptomen bij niet-opgenomen, niet-gevaccineerde volwassenen met COVID-19 en een licht verhoogd risico op een ernstig beloop.
Er is vooralsnog geen RCT gepubliceerd over de effectiviteit van nirmatrelvir/ritonavir bij (gevaccineerde) volwassenen met een COVID-19-infectie tijdens de huidige dominante omikronvariant. In een groot retrospectief cohortonderzoek uitgevoerd op het moment dat de omikronvariant de dominant circulerende stam is bij voor het grootste deel patiënten met eerdere immuniteit door vaccinatie en/of doorgemaakte infectie (78%) lijkt nirmatrelvir/ritonavir zijn effectiviteit te behouden, met name bij patiënten ≥ 65 jaar. Aangezien de kans op ziekenhuisopname momenteel (bij de omikronvariant en de in hoge mate aanwezige antistoffen in de bevolking) laag is, is het absolute voordeel van nirmatrelvir/ritonavir bij volwassenen met COVID-19 met eerdere immuniteit mogelijk klein en niet meer klinisch relevant.
Mogelijk geeft nirmatrelvir/ritonavir meer bijwerkingen dan placebo, zoals dysgeusie (smaakstoornis) en diarree. Nirmatrelvir is een nieuw geneesmiddel waarvan de veiligheid bij mensen zeer beperkt onderzocht is. De veiligheid van het middel is met name onduidelijk, omdat het bij te weinig patiënten onderzocht is en langetermijneffecten onbekend zijn. Fase 4-onderzoek waarin zeldzamere bijwerkingen en bijwerkingen met een langere latentietijd aan het licht kunnen komen, is er nog niet. Nirmatrelvir/ritonavir is niet onderzocht bij zwangere vrouwen en vrouwen die borstvoeding geven.Er zijn zeer veel interacties bekend, voornamelijk voor ritonavir, onder andere met DOAC’s, clopidogrel, enkele anti-epileptica, salmeterol, calciumkanaalblokkers, enkele antiaritmica, diazepam, enkele atypische antipsychotica, enkele statinen en sint-janskruid. Een deel van deze interacties is potentieel ernstig. Veel patiënten met risico op een ernstig beloop van COVID-19 gebruiken chronische medicatie die mogelijk interacties heeft met ritonavir. Dit heeft implicaties voor de toepasbaarheid van nirmatrelvir/ritonavir, omdat het bij sommige patiënten meer bijwerkingen of toxiciteit kan geven (KNMP Kennisbank, geraadpleegd april 2022).
Resistentieontwikkeling kan op populatieniveau een knelpunt zijn. Tot nu toe treedt bij alle virusremmers snelle resistentieontwikkeling op, met name bij patiënten met een afweerstoornis en bij jonge patiënten. Het is nog onduidelijk in welke mate resistentieontwikkeling bij nirmatrelvir een rol speelt.
Kwaliteit van bewijs
De kwaliteit van bewijs is zeer laag, vanwege ernstig risico op bias (invloed farmaceutische industrie) en zeer ernstige onnauwkeurigheid (1 onderzoek, weinig events, betrouwbaarheidsinterval overschrijdt grens klinische relevantie).
Waarden en voorkeuren
De werkgroep is onzeker over de waarden en voorkeuren van patiënten, maar verwacht dat een deel van de patiënten niet zal kiezen voor een behandeling met nirmatrelvir/ritonavir. Het is een nieuw geneesmiddel dat nog beperkt onderzocht is en waarvan de langetermijneffecten onbekend zijn. Daarnaast is van ritonavir bekend dat het zeer veel interacties kent. De werkgroep verwacht dat een meerderheid van de ongevaccineerde patiënten niet zal kiezen voor behandeling met nirmatrelvir/ritonavir.
Het geneesmiddel dient gestart te worden ≤ 5 dagen na de start van de symptomen. Dit is vaak de periode dat patiënten nog niet ernstig ziek zijn. Dit kan een reden zijn voor patiënten om af te wachten in plaats van te kiezen voor behandeling met nirmatrelvir/ritonavir.
Kosten
De kosten van nirmatrelvir/ritonavir zijn €1.242,00 per kuur van 5 dagen (Zorginstituut Nederland).
Aanvaardbaarheid
De patiënt moet bij deze behandeling 3 tabletten tegelijkertijd innemen, en dat 2 × per dag gedurende 5 dagen. Dit zal naar verwachting weinig belastend zijn voor de patiënt, maar omdat het 2 verschillende geneesmiddelen betreft (in combinatieverpakking met per dag 1 blister), is een goede uitvoering mogelijk een knelpunt.
Haalbaarheid
Nirmatrelvir/ritonavir dient in een zo vroeg mogelijk stadium gestart te worden, uiterlijk 5 dagen na het begin van de symptomen. Voor de meeste patiënten duurt het na de start van de klachten enkele dagen totdat zij zich testen. Een groot deel van de patiënten neemt niet zelf contact op met de huisarts of pas na enige tijd. De haalbaarheid van starten ≤ 5 dagen na de start van de symptomen is daarom een issue.
Er zijn veel interacties met andere medicijnen; een deel van deze interacties kan ernstig zijn. Wanneer patiënten ook andere medicatie gebruiken, kan dit nadelige gevolgen hebben voor de haalbaarheid van de inzet van nirmatrelvir/ritonavir.
Uitgangsvraag
Is nirmatrelvir/ritonavir (I) aan te bevelen bij de behandeling van volwassen patiënten met bevestigde COVID-19 in de huisartsenpraktijk (P)?
| Patiënten | Volwassen patiënten met bevestigde COVID-19 in de huisartsenpraktijk |
|---|---|
| Interventie | Nirmatrelvir/ritonavir |
| Vergelijking | Placebo Gebruikelijke zorg |
| Uitkomstmaten | Cruciaal:
Belangrijk:
|
De NHG-werkgroep heeft de volgende grenzen voor klinisch relevante verschillen vastgesteld:
- ziekenhuisopname: absolute daling > 3%
- overlijden: absolute daling > 1%
- duur van de klachten: ≥ 1 dag korter
- bijwerkingen: risico ratio > 1,25
De grenzen van klinische relevantie kunnen verschillen tussen middelen onderling (zie Totstandkoming).
Achtergrond
In het kader van een veilige en effectieve medicamenteuze behandeling voor COVID-19 in de huisartsenpraktijk wordt onder meer onderzoek verricht naar nirmatrelvir (PF-07321332), een nieuw oraal antiviraal geneesmiddel. Nirmatrelvir richt zich op het enzym SARS-CoV-2 3-chymotrypsin-like cysteine protease (Mpro). Mpro is essentieel in de virale replicatiecyclus. In vitro remt nirmatrelvir de activiteit van Mpro en zorgt op die manier voor de inhibitie van virusreplicatie bij meerdere coronavirussen. Door de snelle metabole klaring is de biologische beschikbaarheid van nirmatrelvir echter laag. Toevoeging van een lage dosis ritonavir remt het CYP3A-afhankelijke metabolisme van nirmatrelvir sterk en verhoogt de concentratie nirmatrelvir in het bloed. Ritonavir is onder andere geregistreerd als farmacokinetische booster bij hiv-remmers. Of het gebruik van nirmatrelvir/ritonavir bij COVID-19-patiënten in de huisartsenpraktijk effectief en veilig is, is onduidelijk.
Methode
In februari 2022 is een literatuurzoekactie naar systematische reviews en gerandomiseerde gecontroleerde trials (RCT’s) uitgevoerd in PubMed en Embase (zie Bijlage 4 in de Totstandkoming). Om geen recente onderzoeken te missen werd de zoekactie in augustus 2023 herhaald.
Resultaten
Resultaat zoekactie
De zoekactie leverde een RCT op over nirmatrelvir/ritonavir voor de behandeling van niet-opgenomen, ongevaccineerde volwassenen met bevestigde COVID-19 en een licht verhoogd risico op een ernstig beloop. Er is een tweede onderzoek gaande naar nirmatrelvir/ritonavir bij niet-opgenomen COVID-19-patiënten (EPIC-SR, NCT05011513), maar de resultaten zijn nog niet gepubliceerd.
Onderzoekskarakteristieken
Hammond 2022: fase 2/3 RCT (EPIC-HR) waarin niet-opgenomen, ongevaccineerde volwassenen met COVID-19 met < 5 dagen klachten met hogere kans op complicaties (onder andere ≥ 60 jaar, BMI ≥ 25, roken, hypertensie, diabetes, of hart- en vaatziekte) werden gerandomiseerd (n=2246, 21 landen; mediane leeftijd 46 jaar; 51% man; 80% BMI ≥ 25; 39% roken; 33% hypertensie; 66% ≤ 3 dagen na start symptomen; 51% in het verleden COVID-19 doorgemaakt) over 2 groepen: (1) nirmatrelvir 2 dd 300 mg plus ritonavir 2 dd 100 mg voor 5 dagen, (2) placebo. De follow-upperiode was 28 dagen, uitkomstmaten waren COVID-19-gerelateerde ziekenhuisopnames, overlijden en bijwerkingen.
Effectiviteit en bijwerkingen
Zie de tabel voor de samenvatting van de resultaten. Vergelijkbare resultaten werden gevonden bij patiënten die binnen 3 (in plaats van 5) dagen na start symptomen werden behandeld. De publicatie van resultaten van de follow-up tot 24 weken volgen nog. De EPIC-HR trial vond plaats toen de deltavariant de overheersende circulerende variant was. Een groot retrospectief onderzoek uitgevoerd tijdens de omikronvariant bij voor het grootste deel patiënten met eerdere immuniteit (door vaccinatie en/of doorgemaakte infectie (78%)) laat vergelijkbare resultaten zien, met name bij patiënten ≥ 65 jaar (gecorrigeerde HR 0,27; 95%-BI 0,15 tot 0,49. Ook een systematische review van 7 observationele cohortonderzoeken over grotendeels gevaccineerde patiënten ondersteunt de effectiviteit van nirmatrelvir/ritonavir. Omdat de kans op ziekenhuisopname bij de omikronvariant en bij in hoge mate aanwezige antistoffen lager is (gemiddeld 1,9% vs. 6,0% ), is het absolute voordeel van nirmatrelvir/ritonavir mogelijk klein en niet meer klinisch relevant.
Conclusies
- Voor niet-opgenomen, ongevaccineerde volwassenen met COVID-19 (grotendeels deltavariant) met een licht verhoogd risico op een ernstig beloop geldt:
- mogelijk verlaagt nirmatrelvir/ritonavir de kans op ziekenhuisopname of overlijden, indien gestart wordt ≤ 5 dagen na de start van de symptomen (5,4% absolute daling, kwaliteit van bewijs laag)
- we zijn onzeker, maar mogelijk verlaagt nirmatrelvir/ritonavir de kans op overlijden (kwaliteit van bewijs zeer laag).
- mogelijk geeft nirmatrelvir/ritonavir meer bijwerkingen dan placebo, zoals dysgeusie (smaakstoornis) en diarree (gebaseerd op effectiviteitsonderzoek, kwaliteit van bewijs laag).
- er is niet gerapporteerd over de duur van de klachten.
- Omdat de kans op ziekenhuisopname momenteel laag is (bij de huidige omikronvariant en de in hoge mate aanwezige antistoffen in de bevolking), is het absolute voordeel van nirmatrelvir/ritonavir bij volwassenen met COVID-19 met eerdere immuniteit (door vaccinatie of doorgemaakte infectie) mogelijk klein en niet meer klinisch relevant.
Interacties van nirmatrelvir/ritonavir
Naar Samenvatting ›Ritonavir is verantwoordelijk voor vrijwel alle interacties van de combinatie nirmatrelvir/ritonavir met andere geneesmiddelen. Bij hiv-geïnfecteerden die langdurig ritonavir gebruiken, zijn heel veel interacties beschreven, waarvan sommige potentieel ernstig zijn. De klinische relevantie van deze interacties bij gebruik van ritonavir gedurende 5 dagen is onduidelijk; voor slechts een paar interacties van de combinatie nirmatrelvir/ritonavir met andere geneesmiddelen is een specifiek advies beschikbaar. Het beleid hangt af van de indicatie voor het interacterende geneesmiddel: niet starten van nirmatrelvir/ritonavir, tijdelijk de andere medicatie staken met eventueel een alternatief middel, of dosisaanpassing. Omdat het om zoveel interacties gaat, is een volledig advies in deze standaard niet mogelijk. Tabel 1 geeft een overzicht.
| Interacterend middel | Afhandeling interactie |
|---|---|
| Simvastatine, atorvastatine, alfuzosine | Stop interacterend middel vanaf de start tot ten minste 3 dagen na de kuur nirmatrelvir/ritonavir (stop in totaal 8 dagen) Herstart interacterend middel ten minste 3 dagen na het einde van de kuur nirmatrelvir/ritonavir |
| Immunosuppressiva | Overleg met de voorschrijvend arts; gezien de complexiteit van het onderliggende ziektebeeld is het beleid per patiënt verschillend |
| Geneesmiddelen met interactiemelding in medicatiebewaking | Consulteer laagdrempelig apotheker en/of internist of longarts. Raadpleeg eventueel de interactiewebsite van de Universiteit van Liverpool |
Antibiotica
Naar Samenvatting ›- Wees terughoudend met antibiotica.
- In sommige gevallen zal de huisarts toch besluiten antibiotica voor te schrijven. Bijvoorbeeld bij een sterk vermoeden van een bacteriële co-infectie. Of bij kwetsbare of klinisch zieke patiënten omdat het risico op een bacteriële verwekker van de pneumonie, hoewel weinig voorkomend naast COVID-19, met de bijbehorende risico’s op een ernstig beloop bij de betreffende patiënt, zwaarder weegt dan de risico’s op overbehandeling. Schrijf dan antibiotica voor conform de voorkeursmiddelen in de NHG-Standaard Acuut hoesten.
In enkele Nederlandse onderzoeken is bekeken hoe vaak een bacteriële coverwekker voorkomt bij een COVID-19-pneumonie. De onderzoeken vonden plaats in het ziekenhuis en betroffen patiënten op de Spoedeisende Hulp en patiënten die opgenomen waren in het ziekenhuis, al dan niet op de IC. Bij 1,2 tot 8% van de patiënten werd een bacteriële co-infectie vastgesteld. Kanttekening hierbij is dat een aanzienlijk deel van de patiënten empirisch al antibiotica gekregen had voor presentatie in het ziekenhuis. Ook in een rapid review en meta-analyse van Langford et al. werd gemiddeld bij 6,9% van de COVID-19-patiënten die in het ziekenhuis opgenomen lagen een bacteriële infectie gevonden, maar ook hier ontvingen de meeste patiënten antibiotica. Bacteriële co-infecties lijken niet veelvuldig voor te komen bij COVID-19, maar zijn desondanks niet uitgesloten. Het onderscheid tussen de verschillende (co)verwekkers van een pneumonie is echter op klinische gronden moeilijk te maken.
In een tweedelijns richtlijn van de SWAB wordt aanbevolen terughoudend te zijn met antibiotica bij patiënten met COVID-19. Tevens wordt aanbevolen maximaal in te zetten op aanvullend onderzoek naar een mogelijke bacteriële coverwekker, onder andere met behulp van sputum- en bloedkweken, een pneumokokken antigeentest en een legionella antigeentest. Aangezien deze onderzoeken in de huisartsenpraktijk niet verricht worden, is het aantonen dan wel uitsluiten van een bacteriële coverwekker niet goed mogelijk.
Het CRP kan wel laagdrempelig bepaald worden in de eerste lijn. De hoogte van het CRP is duidelijk gerelateerd aan de aan- of afwezigheid van een pneumonie, maar er zijn vooralsnog geen bewijzen dat CRP bij volwassenen veel waarde heeft in het onderscheid tussen bacteriële en virale ondersteluchtweginfecties (zie NHG-Standaard Acuut hoesten). Er is geen reden om aan te nemen dat dit anders is bij COVID-19.
De werkgroep kwam op basis van voorgaande overwegingen tot het volgende:
Antibiotica zijn meestal niet zinvol bij COVID-19. De werkgroep beveelt daarom aan om terughoudend te zijn met antibiotica bij COVID-19. In sommige gevallen zal de huisarts toch besluiten antibiotica voor te schrijven. Bijvoorbeeld bij een sterk vermoeden van een bacteriële co-infectie. Of bij kwetsbare of klinisch zieke patiënten omdat het risico op een bacteriële verwekker van de pneumonie, hoewel weinig voorkomend naast COVID-19, met de bijbehorende risico’s op een ernstig beloop bij de betreffende patiënt, zwaarder weegt dan de risico’s op overbehandeling.
Volg bij de keuze voor het soort antibioticum en de dosering de NHG-Standaard Acuut hoesten. De gerapporteerde bacteriële pathogenen bij patiënten met een community-acquired luchtweginfectie én COVID-19 lijken overeen te komen met de pathogenen bij patiënten met een ‘reguliere’ bacteriële community-acquired pneumonie (CAP), zoals beschreven in de SWAB CAP richtlijn. Pneumonie door atypische pathogenen naast COVID-19 wordt zelden in onderzoeken gerapporteerd. Daarnaast is er geen bewijs voor een specifieke betere behandelingsstrategie bij patiënten met COVID-19 en een bacteriële superinfectie.
Inhalatiecorticosteroïden
Naar Samenvatting ›We bevelen het voorschrijven van inhalatiecorticosteroïden als behandeling van COVID-19 niet aan.
- Op basis van het huidige bewijs is het onzeker of het gebruik van ICS de duur van de COVID-19-klachten verkort bij grotendeels ongevaccineerde patiënten met een verhoogd risico op een ernstig beloop van COVID-19. Bovendien verlagen ICS mogelijk niet of nauwelijks de kans op ziekenhuisopname of overlijden. Bij de gehele groep ongevaccineerde patiënten met milde tot matig ernstige klachten zijn er geen gunstige effecten van ICS gevonden.
- Er zijn geen RCT’s bekend over de effectiviteit van ICS bij (grotendeels) gevaccineerde patiënten, zoals momenteel de situatie in de bevolking is. Daarnaast zijn de huidige onderzoeken uitgevoerd voordat de omikronvariant de dominant circulerende stam werd.
- De werkgroep geeft een sterk negatieve aanbeveling voor de behandeling van ICS bij COVID-19.
Voor- en nadelen
- We zijn onzeker of het gebruik van een hoge dosering ICS de duur van COVID-19-klachten verkort bij grotendeels ongevaccineerde patiënten met een verhoogde kans op een ernstig beloop door leeftijd en/of comorbiditeit (≥ 65 jaar, of ≥ 50 jaar met comorbiditeit in het onderzoek van Yu 2021 en ≥ 60 jaar, of ≥ 50 jaar met comorbiditeit in het kleinere onderzoek van Duvignaud 2022. ICS verlagen bij deze patiënten niet of nauwelijks de kans op ziekenhuisopname of overlijden.
- Bij de gehele groep ongevaccineerde patiënten met milde tot matige klachten van COVID-19 wordt niet of nauwelijks effect gezien van ICS op ziekenhuisopname, sterfte en duur van de klachten.
- De huidige onderzoeken zijn uitgevoerd voordat de omikronvariant de dominant circulerende stam werd en bij grotendeels ongevaccineerde patiënten. Momenteel zijn er in hoge mate antistoffen aanwezig in de bevolking.
- De meest voorkomende bijwerkingen van ICS zijn orofaryngeale candidiasis, milde irritatie van de keelholte, slikproblemen, heesheid, hoest en droge mond. COPD-patiënten die ICS gebruiken, hebben een verhoogd risico op een pneumonie. Zelden komen ontregeling van diabetes mellitus en overgevoeligheidsreacties zoals bronchospasmen en huidreacties voor (KNMP Kennisbank, geraadpleegd juni 2023).
Kwaliteit van bewijs
De kwaliteit van bewijs is laag wegens een risico op bias en door onnauwkeurigheid (de betrouwbaarheidsintervallen voor de primaire uitkomsten overschrijden de grens voor klinische relevantie).
Waarden en voorkeuren
De werkgroep verwacht dat de meeste patiënten ICS niet willen, omdat het geneesmiddel mogelijk niet of nauwelijks effect heeft op het beloop van COVID-19.
Kosten
De kosten voor ICS in hogere doseringen gedurende 14 dagen zijn rond de 15-25 euro (medicijnkosten.nl, geraadpleegd op 03-10-23).
Aanvaardbaarheid
De werkgroep verwacht dat de meeste patiënten de behandeling acceptabel zullen vinden.
Haalbaarheid
ICS zijn veelgebruikte geneesmiddelen bij astma en COPD, waarmee de huisarts veel ervaring heeft. Wel is een juiste inhalatietechniek essentieel voor de behandeling. Er dient aandacht te zijn voor eventuele patiëntgebonden factoren die een adequaat gebruik in de weg kunnen staan, zoals kortademigheid die goed inademen belemmert, of onvermogen om de instructies te begrijpen. Deze potentiële haalbaarheidsproblemen kunnen (deels) worden ondervangen door het gebruik van een voorzetkamer en hulp bij de toediening.
Uitgangsvraag
Is een inhalatiecorticosteroïd (I) aan te bevelen bij de behandeling van bevestigde volwassen COVID-19-patiënten met milde tot matige klachten in de huisartsenpraktijk (P)?
| Populatie | Bevestigde volwassen COVID-19-patiënten met milde tot matige klachten in de huisartsenpraktijk |
|---|---|
| Interventie | Inhalatiecorticosteroïd |
| Vergelijking | Placebo Geen behandeling of gebruikelijke zorg |
| Uitkomstmaten | Cruciaal:
Belangrijk:
|
De NHG-werkgroep heeft de volgende grenzen voor klinisch relevante verschillen vastgesteld:
- ziekenhuisopname: absolute daling ≥ 2%
- overlijden: absolute daling ≥ 1%
- duur van de klachten: ≥ 1 dag korter
- bijwerkingen: absolute stijging 10%
De grenzen van klinische relevantie kunnen verschillen tussen middelen onderling (zie Totstandkoming).
Achtergrond
Onderzoeken naar patiëntkarakteristieken van opgenomen COVID-19-patiënten toonden een onverwacht laag aantal astma- en COPD-patiënten. Nadat in vitro-onderzoeken lieten zien dat inhalatiecorticosteroïden (ICS) in staat waren om virusreplicatie van COVID-19 in de luchtwegen te verminderen, ontstond de hypothese dat ICS mogelijk een bijdrage leveren aan het voorkomen van klinische achteruitgang bij SARS-CoV-2-infecties. Het is onduidelijk of het gebruik van ICS effectief is bij patiënten met milde en matige COVID-19-klachten in de huisartsenpraktijk.
Methoden
In april 2021 is een literatuurzoekactie naar systematische reviews en gerandomiseerde gecontroleerde trials (RCT’s) uitgevoerd in PubMed, Embase, bioRxiv (biorxiv.org), Preprints (preprints.org), EuropePMC (europepmc.org) en Medrxiv (medrxiv.org). Zie Bijlage 4 Zoekstrategie in het Totstandkomingsdocument. Om geen recente onderzoeken te missen werd de zoekactie maandelijks tot augustus 2023 herhaald.
Resultaten
Resultaat zoekactie
De oorspronkelijke zoekactie leverde 2 RCT’s op naar de effectiviteit van budesonide ten opzichte van gebruikelijke zorg. Bij diverse updates van de zoekactie vonden we 3 RCT’s over ciclesonide ter behandeling van COVID-19.
Onderzoekskarakteristieken
- Ramakrishnan 2021: open-label fase 2-RCT (STOIC) waarin niet-gevaccineerde patiënten met milde COVID-19-symptomen (< 7 dagen) werden gerandomiseerd over budesonide inhalatie (2 dd 800 mcg, mediane duur 7 dagen) of gebruikelijke zorg (n = 146; Engeland; eerstelijnspatiënten; gemiddeld 45 jaar (bandbreedte 19-79 jaar); 58% vrouw, mediane duur symptomen: 3 dagen; percentage PCR bevestigde COVID-19: 94%). Follow-upduur 28 dagen. Patiënten die de voorgaande 7 dagen ICS of systemische corticosteroïden gebruikten, zijn geëxcludeerd. Het onderzoek werd voortijdig gestaakt omdat onafhankelijke analyse liet ziet dat verdere inclusies geen effect meer zouden hebben op de resultaten. Oorspronkelijk zouden 398 patiënten worden geïncludeerd.
- Yu 2021: open-label fase 3-RCT (PRINCIPLE) waarin patiënten met COVID-19-symptomen (< 14 dagen) met hogere kans op complicaties (leeftijd ≥ 65 jaar of ≥ 50 jaar met comorbiditeit) werden gerandomiseerd over budesonide inhalatie (2 dd 800 mcg voor 14 dagen) of gebruikelijke zorg (subgroep met PCR-bevestigde COVID-19: n = 1959; Engeland; eerstelijnspatiënten; gemiddeld 64 jaar; 52% vrouw, mediane duur symptomen 6 dagen; 11% gevaccineerd (10% met 1 dosis, 1% met 2 doses). Patiënten die al ICS of systemische corticosteroïden gebruikten, zijn geëxcludeerd. Follow-upduur 28 dagen.
- Ezer 2021: placebogecontroleerde fase 2-RCT (CONTAIN) waarin niet-opgenomen en niet-gevaccineerde volwassenen met PCR-bevestigde COVID-19 die voornamelijk respiratoire klachten hadden (< 5 dagen na start symptomen) werden gerandomiseerd over ciclesonide (inhalatie 2 dd 600 mcg en intranasaal 1 dd 200 mcg) of placebo gedurende 14 dagen (n = 203; Canada; mediane leeftijd 35 jaar; 54% vrouw, mediane duur symptomen 3 dagen). Follow-upduur 14 dagen. Patiënten die al ICS gebruikten, zijn geëxcludeerd. Het onderzoek werd voortijdig gestaakt omdat de inclusie sterk terugliep (stijgende vaccinatiegraad). Oorspronkelijk zouden 318 patiënten worden gerandomiseerd.
- Clemency 2022: placebo-gecontroleerde fase 3-RCT waarin niet-opgenomen, niet-gevaccineerde patiënten ≥ 12 jaar (n = 400; VS; gemiddeld 43 jaar; 55% vrouw) met symptomatische COVID-19 (< 72 uur na diagnose) werden gerandomiseerd over ciclesonide (inhalatie 2 dd 320 mcg) of placebo gedurende 30 dagen. Geëxcludeerd zijn patiënten die in de afgelopen 14 dagen inhalatie- of intranasale corticosteroïden gebruikten, of in de afgelopen 90 dagen systemische corticosteroïden.
- Duvignaud 2022: open-label fase 3-RCT (COVERAGE) waarin niet-opgenomen patiënten met COVID-19-symptomen (< 7 dagen) met een hogere kans op een gecompliceerd beloop (≥ 60 jaar, ≥ 50 jaar met comorbiditeit) werden gerandomiseerd over ciclesonide inhalatie (2 dd 320 mcg gedurende 10 dagen) of een controlegroep (combinatie van vitaminen en sporenelementen 1 dd 2 pillen) (n = 217; Frankrijk; mediane leeftijd 63 jaar; 51% vrouw, 14% gevaccineerd (13% met 1 dosis, 1% met 2 dosis)). Patiënten die al ICS gebruikten, zijn geëxcludeerd. Follow-upduur 28 dagen. Het onderzoek werd voortijdig gestaakt omdat onafhankelijke analyse liet zien dat verdere inclusies geen effect meer zouden hebben op de resultaten. Oorspronkelijk zouden 1332 patiënten worden geïncludeerd.
Zie bijlage 7 in de Totstandkoming voor een gedetailleerde beschrijving van de onderzoekskarakteristieken.
Effectiviteit en bijwerkingen
Zie de tabellen voor de samenvatting van de resultaten. Tabel ICS laat de resultaten zien van ICS ten opzichte van placebo/gebruikelijke zorg bij patiënten met milde tot matige klachten van COVID-19. Tabel ICS bij hoog risico laat de resultaten zien van ICS ten opzichte van gebruikelijke zorg bij hoog risico patiënten met milde tot matige klachten van COVID-19.
Conclusies
Niet-gevaccineerde patiënten met milde tot matige klachten van COVID-19
- ICS verlagen mogelijk niet of nauwelijks de kans op ziekenhuisopname of overlijden (kwaliteit van bewijs: laag).
- We zijn onzeker over het effect van ICS op de kans op COVID-19-gerelateerd SEH-bezoek en/of ziekenhuisopname (kwaliteit van bewijs: zeer laag)
- Er is mogelijk niet of nauwelijks verschil in duur van de klachten of bijwerkingen (kwaliteit van bewijs: laag).
Hoogrisicopatiënten (≥ 65 jaar of 50-64 jaar met comorbiditeit; grotendeels niet gevaccineerd) met mild tot matige klachten van COVID-19
- ICS verlagen mogelijk niet of nauwelijks de kans op ziekenhuisopname of overlijden (kwaliteit van bewijs: laag).
- We zijn onzeker of ICS de duur van COVID-19-klachten verkorten (kwaliteit van bewijs: zeer laag).
Dexamethason
Naar Samenvatting ›We bevelen dexamethason niet aan voor COVID-19-patiënten die niet zuurstofbehoeftig zijn (zie ook Beleid bij zuurstofbehoeftige, niet-terminale patiënten die niet opgenomen willen worden).
Niet aanbevolen overige medicamenteuze behandelingen
Naar Samenvatting ›Er worden diverse middelen onderzocht op basis van een theoretisch werkingsmechanisme, effectiviteit in vitro of werkzaamheid bij andere virussen (zoals hiv en griep).
Hydroxychloroquine
Naar Samenvatting ›We bevelen de off-label behandeling met hydroxychloroquine, hydroxychloroquine in combinatie met azitromycine en hydroxychloroquine met azitromycine en zink niet aan voor patiënten met (een vermoeden van) COVID-19 in de huisartsenpraktijk.
Omdat een (combinatie)behandeling met hydroxychloroquine waarschijnlijk geen effect heeft op de kans op ziekenhuisopname en overlijden, noch op de tijd tot aan het verdwijnen van de klachten, geven we een sterke aanbeveling tegen hydroxychloroquine, hydroxychloroquine met azitromycine en hydroxychloroquine met azitromycine en zink.
Bovendien kent de behandeling bijwerkingen, waarvan sommige potentieel ernstig zijn. De kans op potentieel ernstige bijwerkingen neemt toe bij gecombineerd gebruik van hydroxychloroquine en azitromycine.
Voor- en nadelen
Een (combinatie)behandeling met hydroxychloroquine geeft waarschijnlijk niet of nauwelijks verschil in de kans op ziekenhuisopname of overlijden, noch in het verminderen van de duur van de klachten bij niet-opgenomen patiënten met COVID-19.
Een publicatie van het Nederlands bijwerkingencentrum Lareb over 1071 Nederlandse meldingen van bijwerkingen met betrekking tot hydroxychloroquine in de periode 1988-2020 laat zien dat de meest gemelde bijwerkingen gastro-intestinale klachten (16,2%) en huidreacties (19,7%) zijn. Dit komt overeen met de meest voorkomende bijwerkingen in onderzoeken bij COVID-19-patiënten in de eerste lijn. Verder worden oogklachten, neurologische of psychische klachten regelmatig gemeld. Cardiale problemen (palpitaties, cardiomyopathie, ritmestoornis, AV-blok, hartstilstand, ecg-afwijking, zoals QTc-verlenging en afwijking van het QRS-complex) worden minder frequent gemeld (2,6%).
De meeste ernstige bijwerkingen bij Lareb betreffen levensbedreigende huidreacties en psychische klachten, naast ernstige cardiale, neurologische en respiratoire klachten.
Het risico op cardiale bijwerkingen is waarschijnlijk groter indien hydroxychloroquine gecombineerd wordt met andere middelen die ook een verhoogde kans op een verlengde QT-tijd geven, zoals azitromycine.
Kwaliteit van bewijs
De kwaliteit van bewijs is redelijk: er is sprake van ernstige onnauwkeurigheid omdat het betrouwbaarheidsinterval de grens van klinische relevantie overschrijdt of vanwege weinig events.
Waarden en voorkeuren
We verwachten dat de meeste patiënten een (combinatie)behandeling met hydroxychloroquine niet willen, omdat het geneesmiddel waarschijnlijk geen effect heeft op het beloop van COVID-19 en het wel (ernstige) bijwerkingen kan geven.
Kosten
Hydroxychloroquinetabletten kosten circa € 9,87 tot € 13,16 (1 week, 600-800 mg/dag, bij € 0,47 per tablet van 200 mg). De combinatiebehandeling hydroxychloroquine met azitromycine kost circa € 11,37 tot 14,66 (500 mg azitromycine eenmalig, gevolgd door 250 mg op dag 2-5, bij circa € 0,25 per tablet van 250 mg) (www.medicijnkosten.nl, geraadpleegd 25-02-2021). Zink is zonder recept verkrijgbaar en kost circa € 2,00 tot 3,50 per week.
Aanvaardbaarheid
De werkgroep verwacht dat het merendeel van de patiënten een kortdurende orale behandeling aanvaardbaar zal vinden.
Haalbaarheid
De werkgroep verwacht dat toepassing van hydroxychloroquine, azitromycine en zink in de huisartsenpraktijk haalbaar is, aangezien hydroxychloroquine en azitromycine verkrijgbaar zijn bij de apotheek. Zink is een vrij verkrijgbaar supplement.
Uitgangsvraag
Is hydroxychloroquine, hydroxychloroquine met azitromycine of hydroxychloroquine met azitromycine en zink (I) vergeleken met symptomatische behandeling zonder deze middelen (C) aan te bevelen voor de behandeling van patiënten met milde tot matige COVID-19-klachten in de huisartsenpraktijk (P)?
| Patiënten | COVID-19-bevestigde of -verdachte volwassenen in de eerste lijn met milde tot matige klachten |
|---|---|
| Interventie |
|
| Vergelijking | Placebo of gebruikelijke zorg |
| Uitkomstmaten | Cruciaal Ziekenhuisopname Overlijden Belangrijk Bijwerkingen Ernst van de klachten Tijd tot verdwijnen van klachten |
Achtergrond
Er wordt gezocht naar een veilige en effectieve medicamenteuze behandeling voor COVID-19 bij patiënten in de eerste lijn. In dit kader is er onder meer onderzoek verricht naar hydroxychloroquine. Hierbij gaat het om hydroxychloroquine, eventueel in combinatie met andere middelen, zoals met azitromycine en zink. Voor de eerste lijn gaat het om de effectiviteit en veiligheid van hydroxychloroquine(combinatie)behandeling bij niet-gehospitaliseerde patiënten. Deze groep verschilt doorgaans van de gehospitaliseerde patiënten wat betreft leeftijd, comorbiditeit en ernst van de symptomen. We beschrijven daarom uitsluitend de momenteel beschikbare onderzoeken in de eerste lijn.
Methoden
Er is een systematische literatuurzoekactie naar systematische reviews (SR's), randomized controlled trials (RCT’s) en observationeel onderzoek uitgevoerd in PubMed, Embase, bioRxiv (biorxiv.org), Preprints (preprints.org), EuropePMC (europepmc.org), Medrxiv (medrxiv.org) op 22 juli 2020. Om geen recente onderzoeken te missen werd de zoekactie in januari 2022 herhaald.
Resultaten
Resultaat zoekactie
We vonden 1 SR over hydroxychloroquine voor de behandeling van milde COVID-19. Alle 4 geïncludeerde fase 3-RCT’s in deze SR voldeden aan onze inclusiecriteria. Daarnaast vonden we nog 2 RCT’s over hydroxychloroquine en 1 RCT over de effectiviteit van hydroxychloroquine plus azitromycine. We vonden geen RCT’s over hydroxychloroquine plus azitromycine plus zink voor de behandeling van milde/matige COVID-19 in de huisartsenpraktijk.
Onderzoekskarakteristieken
Hydrochloroquine
- Skipper (2020): RCT in de eerste lijn in de Verenigde Staten en Canada bij 491 niet-gehospitaliseerde patiënten met ≤ 4 dagen COVID-19-klachten met óf een recent bevestigde COVID-19-infectie (58%), óf hoog risico exposure aan iemand met bevestigde COVID-19 in de afgelopen 14 dagen. Patiënten werden gerandomiseerd naar hydroxychloroquine (eenmalig 800 mg, 6-8 uur later 600 mg, gevolgd door 1 dd 600 mg op dag 2-5) of placebo. Patiënten waren gemiddeld 40 jaar en 56% was vrouw. Follow-upduur was 14 dagen. Uitkomstmaten waren ernst van symptomen, ziekenhuisopname, overlijden en bijwerkingen.
- Mitjà (2021): open-label RCT in de eerste lijn in Spanje bij 293 niet-gehospitaliseerde patiënten met een recent bevestigde COVID-19-infectie en < 5 dagen klachten. Patiënten werden gerandomiseerd naar hydroxychloroquine (800 mg op dag 1, gevolgd met 1 dd 400 mg op dag 2-7) of geen antivirale behandeling. Patiënten waren gemiddeld 42 jaar en 69% was vrouw. Follow-upduur was 28 dagen. Uitkomstmaten waren: vermindering van virale RNA-load, ziekteprogressie, tijd tot aan verdwijnen van klachten en bijwerkingen.
- Omrani (2020): RCT (Q-PROTECT) waarin niet-gehospitaliseerde patiënten met asymptomatische of milde PCR-bevestigde COVID-19 (< 1 dag) werden gerandomiseerd naar 3 groepen: hydroxychloroquine (1 dd 600 mg), hydroxychloroquine (1 dd 600 mg) plus azitromycine (500 mg op dag 1, gevolgd door 1 dd 250 mg op dag 2-5) of placebo voor 1 week (n = 456; Qatar; gemiddeld 41 jaar; 2% vrouw; voornamelijk expats). Follow-upduur was 21 dagen. Uitkomstmaten waren ziekenhuisopname, overlijden en ernstige bijwerkingen.
- Reis (2021): RCT (TOGETHER) waarin niet-gehospitaliseerde patiënten met COVID-19-gerelateerde klachten of CT-scan van de thorax consistent met COVID-19 (< 8 dagen klachten) met hogere kans op complicaties (> 50 jaar, longziekte, diabetes, hypertensie, hartziekte, BMI ≥ 30, immuungecompromitteerde status of actieve maligniteit) werden gerandomiseerd naar 3 groepen: hydroxychloroquine (800 mg op dag 1, gevolgd door 1 dd 400 mg op dag 2-9), lopinavir-ritonavir of placebo gedurende 10 dagen (n = 685; Brazilië; mediane leeftijd 53 jaar; 55% vrouw). De trial is voortijdig gestopt; oorspronkelijk zouden 1476 patiënten worden gerandomiseerd. Follow-upduur was 90 dagen. Uitkomstmaten waren ziekenhuisopname, overlijden, duur van de klachten en bijwerkingen.
- Johnston (2021): RCT waarin niet-gehospitaliseerde patiënten met bevestigde COVID-19 (< 3 dagen) van wie de meerderheid een hogere kans op complicaties had (> 60 jaar, longziekte, diabetes, hypertensie, BMI ≥ 30) werden gerandomiseerd naar 3 groepen: (1) hydroxychloroquine (2 dd 400 mg op dag 1, gevolgd door 2 dd 200 mg op dag 2-9) plus foliumzuur, (2) hydroxychloroquine plus azitromycine (1 dd 500 mg op dag 1, gevolgd door 1 dd 250 mg op dag 2-5) of (3) placebo gedurende 10 dagen (n = 231; Verenigde Staten; mediane leeftijd 37 jaar; 57% vrouw; 56% hoog risico). De trial is voortijdig gestopt; oorspronkelijk zouden 330 hoogrisicopatiënten en 90 laagrisicopatiënten worden gerandomiseerd. Follow-upduur was 28 dagen. Uitkomstmaten waren COVID-19-gerelateerde ziekenhuisopname, overlijden, duur van de klachten en ernstige bijwerkingen.
- Schwartz (2021): RCT waarin niet-gehospitaliseerde patiënten met bevestigde COVID-19 (< 4 dagen) werden gerandomiseerd naar hydroxychloroquine (2 dd 400 mg op dag 1, gevolgd door 2 dd 200 mg op dag 2-4) of placebo voor 5 dagen (n = 148; Canada; gemiddeld 47 jaar; 45% vrouw; 63% hoog risico). De trial is voortijdig gestopt; oorspronkelijk zouden 1446 patiënten worden gerandomiseerd. Follow-upduur was 30 dagen. Uitkomstmaten waren ziekenhuisopname, overlijden, tijd tot aan herstel en ernstige bijwerkingen.
Hydroxychloroquine plus azitromycine
- Omrani (2020): zie onder Hydroxychloroquine
- Johnston 2021: zie onder Hydroxychloroquine
- Rodrigues 2021: RCT waarin niet-gehospitaliseerde patiënten met milde, bevestigde COVID-19 (< 5 dagen symptomen) werden gerandomiseerd naar hydroxychloroquine (2 dd 400 mg voor 7 dagen) plus azitromycine (1 dd 500 mg op dag 1, gevolgd door 1 dd 250 mg op dag 2-5) of placebo (n = 84; Brazilië; gemiddelde leeftijd 37 jaar; 40% vrouw). Follow-upduur was 14 dagen. Uitkomstmaten waren ziekenhuisopname, overlijden, duur van de klachten en bijwerkingen.
Effectiviteit
Zie tabel Hydroxychloroquine voor de samenvatting van de resultaten van de effectiviteit van hydroxychloroquine en tabel Hydroxychloroquine + azitromycine voor de samenvatting van de resultaten van de effectiviteit van hydroxychloroquine plus azitromycine.
Conclusies
- Hydroxychloroquine (met of zonder azitromycine) geeft waarschijnlijk niet of nauwelijks verschil in ziekenhuisopnames, overlijden en tijd tot aan verdwijnen van klachten bij niet-gehospitaliseerde COVID-19-patiënten (kwaliteit van bewijs: redelijk).
- Er is waarschijnlijk geen verschil in het effect van hydroxychloroquine op ziekenhuisopnames tussen hoogrisico- en laagrisicopatiënten.
- Hydroxychloroquine geeft mogelijk niet of nauwelijks verschil in vermindering van ernst symptomen (kwaliteit van bewijs: laag).
- We zijn onzeker over of hydroxychloroquine vaker bijwerkingen geeft (kwaliteit van bewijs: zeer laag).
- We vonden geen RCT’s naar de effectiviteit en veiligheid van hydroxychloroquine plus azitromycine plus zink voor de behandeling van milde/matige COVID-19 in de huisartsenpraktijk
Ivermectine
Naar Samenvatting ›We bevelen het off-label voorschrijven van ivermectine niet aan als behandeling voor patiënten met (een vermoeden van) COVID-19 in de huisartsenpraktijk.
Omdat ivermectine waarschijnlijk niet of nauwelijks effect heeft op de kans op ziekenhuisopname, overlijden en de duur van de klachten, geven we een sterke aanbeveling tegen ivermectine.
Voor- en nadelen
Ivermectine geeft waarschijnlijk niet of nauwelijks verschil in de kans op ziekenhuisopname of overlijden. Ivermectine geeft waarschijnlijk niet of nauwelijks verschil in de duur van de klachten of de duur van ziekenhuisopname. Er is mogelijk niet of nauwelijks verschil in bijwerkingen (kwaliteit van bewijs: laag).
Bijwerkingen van ivermectine bij geregistreerde indicaties
Bijwerkingen zijn afhankelijk van de behandelde indicatie/parasiet. Veelvoorkomende bijwerkingen (bij 1-10% van de patiënten) zijn huiduitslag, maag-darmklachten (zoals diarree, misselijkheid, braken), hoofdpijn, slapeloosheid, duizeligheid en stijging van transaminasewaarden. Zelden voorkomende bijwerkingen (bij 0,1-0,01% van de patiënten) zijn voorbijgaande hypereosinofilie, leverfunctiestoornissen, hematurie, en zeer zelden (bij ≤ 0,01% van de patiënten) toxische epidermale necrolyse (TEN) en Stevens Johnson syndroom (SJS) [Kennisbank geraadpleegd 21-1-2021 en SmPC Ivergalen 3 mg].
Kwaliteit van bewijs
Redelijk, er is afgewaardeerd voor ernstige onnauwkeurigheid.
Waarden en voorkeuren
We verwachten dat de meeste patiënten zullen afzien van een behandeling met ivermectine, omdat het middel waarschijnlijk geen effect heeft op het beloop van COVID-19 en wel bijwerkingen kan geven.
Kosten
De kosten voor behandeling met ivermectine hangen samen met de dosering en behandelduur en deze zijn niet bekend. Om een indruk te krijgen: ivermectine tablet 3 mg kost circa € 4,60, per dag komt dat neer op € 18,40 tot € 36,80 (www.medicijnkosten.nl, geraadpleegd 16-1-2021).
Aanvaardbaarheid
Ivermectine is voor de meeste patiënten waarschijnlijk een aanvaardbare behandeling, omdat het in de vorm van een tablet wordt ingenomen.
Haalbaarheid
Wij verwachten dat toepassing van ivermectine in de huisartsenpraktijk haalbaar is, aangezien ivermectine verkrijgbaar is bij de apotheek en de huisarts ervaring met dit middel heeft voor de behandeling van scabiës.
Uitgangsvraag/PICO
Is ivermectine naast de gebruikelijke symptomatische behandeling (I) vergeleken met alleen symptomatische behandeling (C) aan te bevelen voor de behandeling van patiënten met COVID-19 in de huisartsenpraktijk (P)?
| Patiënten | COVID-19-bevestigde volwassenen in de eerste lijn met klachten passend bij COVID-19 |
|---|---|
| Interventie | Symptomatische behandeling met ivermectine |
| Vergelijking | Symptomatische behandeling zonder ivermectine |
| Uitkomstmaten | Cruciaal Ziekenhuisopname Overlijden Belangrijk Bijwerkingen Duur ziekenhuisopname Complicaties bij de ziekenhuisopname Ernst van de klachten Tijd tot verdwijnen van klachten |
De NHG-werkgroep heeft de volgende grenzen voor klinisch relevante verschillen vastgesteld:
- Ziekenhuisopname: absolute daling 2%
- Overlijden: absolute daling 1%
- Duur van de klachten: 1 dag korter
- Bijwerkingen: absolute stijging van 10%
De grenzen van klinische relevantie kunnen verschillen tussen middelen onderling (zie Totstandkoming).
Achtergrond
Er wordt gezocht naar een veilige en effectieve medicamenteuze behandeling voor COVID-19 bij patiënten in de eerste lijn. In dit kader wordt onder meer onderzoek verricht naar ivermectine, een anthelminthicum.
Voor de eerste lijn is het van belang te weten wat de effectiviteit en veiligheid van ivermectine is bij niet in het ziekenhuis opgenomen patiënten. Deze groep verschilt doorgaans van de gehospitaliseerde patiënten wat betreft leeftijd, comorbiditeit en ernst van de symptomen. We beschrijven daarom uitsluitend beschikbare onderzoeken naar ivermectine in de eerste lijn.
Methoden
Er is een systematische literatuurzoekactie naar systematische reviews, randomized controlled trials (RCT’s) en observationeel onderzoek uitgevoerd in PubMed en Embase op 21 december 2020 . Daarnaast is via de WHO en Google scholar gezocht naar preprints. Om geen recente onderzoeken te missen werd de zoekactie in oktober 2021, januari 2022 en april 2022 en september 2022 herhaald.
Resultaten
Resultaat zoekactie
De zoekactie in december 2020 leverde geen geschikte SR's, RCT’s of observationeel onderzoek op over de effectiviteit van ivermectine bij COVID-19-patiënten in de eerste lijn. Bij de update van de zoekactie in oktober 2021 werd een cochranereview over ivermectine voor de behandeling van COVID-19 gevonden. In deze review zijn 4 RCT’s bij eerstelijnspatiënten geïncludeerd. Twee van de 4 geïncludeerde RCT’s in deze SR voldeden aan onze inclusiecriteria. Een aanvullende search na de zoekdatum van de cochranereview leverde nog 1 aanvullende RCT op. Tijdens de update van de literatuurzoekacties in januari en april 2022 vonden we nog drie aanvullende onderzoeken. Omdat de publicatie van Abbas et al. te veel inconsistenties bevat, hebben we dit onderzoek buiten beschouwing gelaten (zie Totstandkoming). Tijdens de update van de literatuurzoekactie in september 2022 vonden we een update van de cochranereview en drie aanvullende RCT's. Omdat de resultaten van de aanvullende onderzoeken in lijn zijn met eerdere onderzoeksresultaten en geen invloed hebben op de sterkte en richting van de aanbeveling, worden ze hier verder niet beschreven.
Onderzoekskarakteristieken
- Chaccour (2021): dubbelblind fase 2-RCT dubbelblind pilotonderzoek onder laagrisicopatiënten met bevestigde COVID-19 en < 3 dagen klachten die zich presenteerden op de spoedeisende hulp (n = 24, Spanje, mediane leeftijd 26 jaar, 50% vrouw, geen comorbiditeit). Patiënten werden gerandomiseerd naar ivermectine (eenmalig 400 microg/kg) of placebo. Follow-upduur was 28 dagen. Uitkomstmaten waren: ziekteprogressie, tijd tot aan verdwijnen van klachten en bijwerkingen.
- López-Medina (2021): dubbelblinde fase 2/3-RCT bij volwassenen met bevestigde COVID-19 en ≤ 7 dagen klachten (n = 400, Colombia, mediane leeftijd 37 jaar, 58% vrouw, 1% opgenomen in ziekenhuis, 41% niet opgenomen, maar zuurstofbehoeftig). Patiënten werden gerandomiseerd naar ivermectine (300 microg/kg gedurende 5 dagen) of placebo. Follow-upduur was 21 dagen. Uitkomstmaten waren: tijd tot aan verdwijnen van klachten, escalatie van zorg (gedefinieerd als ziekenhuisopname of zuurstofbehoefte) en bijwerkingen.
- Vallejos (2021): dubbelblinde fase 2/3-RCT bij volwassenen met bevestigde COVID-19 ≤ 48 uur (n = 501, Argentinië, gemiddelde leeftijd 42 jaar, 47% vrouw, 96% symptomatisch, 0% opgenomen in ziekenhuis of zuurstofbehoeftig bij aanvang studie). Patiënten werden gerandomiseerd naar ivermectine (patiënt ≤ 80 kg 12 mg; 80-110 kg 18 mg; > 110 kg 24 mg gedurende 2 dagen) of placebo. Follow-upduur was 30 dagen. Uitkomstmaten waren: ziekenhuisopname, overlijden en bijwerkingen.
- Buonfrate (2022): dubbelblinde fase 2-RCT (COVER) bij volwassenen met een recent bevestigde COVID-19 (n = 93, Italië, mediane leeftijd 43 jaar, 42% vrouw, 86% symptomatisch, 20% bij aanvang opgenomen in ziekenhuis of zuurstofbehoeftig, 2% gevaccineerd). Patiënten werden gerandomiseerd naar 3 groepen: ivermectine (600 microg/kg gedurende 5 dagen), ivermectine (1200 microg/kg gedurende 5 dagen) of placebo. De follow-upduur was 30 dagen. Uitkomstmaten waren ziekenhuisopname en ernstige bijwerkingen. Het onderzoek werd voortijdig gestaakt omdat de inclusie sterk terugliep. Oorspronkelijk zouden 102 patiënten worden gerandomiseerd.
- Reis (2022): dubbelblinde fase 3-RCT (TOGETHER) bij volwassenen met bevestigde COVID-19, ≤ 7 dagen klachten en verhoogde kans op een ernstig beloop (> 50 jaar, diabetes, hypertensie, hartziekte, COPD, roken, chronische nierziekte of kanker). Patiënten werden gerandomiseerd naar ivermectine (400 microg/kg gedurende 3 dagen) of placebo (n = 1358, Brazilië, mediane leeftijd 49 jaar, 58% vrouw). De follow-upduur was 28 dagen. Uitkomstmaten waren ziekenhuisopname, overlijden en bijwerkingen.
Effectiviteit en bijwerkingen
Bekijk de tabel voor de samenvatting van de resultaten.
Conclusie
- Ivermectine geeft waarschijnlijk niet of nauwelijks verschil in de kans op ziekenhuisopname of overlijden (kwaliteit van bewijs: redelijk).
- Ivermectine geeft waarschijnlijk niet of nauwelijks verschil in de duur van de klachten of de duur van ziekenhuisopname (kwaliteit van bewijs: redelijk).
- Er is mogelijk niet of nauwelijks verschil in bijwerkingen (kwaliteit van bewijs: laag).
Vitamine C
Naar Samenvatting ›Er is onvoldoende bewijs voor de werkzaamheid van vitamine C voor de behandeling van patiënten met COVID-19.
Op theoretische gronden is er geen reden om vitamine C voor te schrijven aan patiënten met mild tot matig ernstige klachten van COVID-19, omdat er bij deze patiënten waarschijnlijk geen sprake is van oxidatieve stress. Daarnaast is de orale opname van vitamine C beperkt en zijn de beoogde doseringen en daardoor intraveneuze toedieningswijze minder geschikt voor eerstelijnspatiënten. Een kleine RCT naar gebruik van hooggedoseerd vitamine C bij niet in het ziekenhuis opgenomen COVID-19-patiënten liet geen verschil zien tussen de groepen ten aanzien van de duur van symptomen.
Vitamine D
Naar Samenvatting ›- Er is onvoldoende bewijs voor de werkzaamheid van vitamine D voor de behandeling of preventie van patiënten met COVID-19.
- Wijs patiënten met vragen over vitamine D op de reguliere adviezen ter preventie van vitamine D-deficiëntie voor groepen met een verhoogd risico. In de LESA Laboratoriumdiagnostiek Vitamine D-deficiëntie staat bij welke personen de vitamine D-suppletie, ongeacht de vitamine D-spiegel, wordt aanbevolen. Verwijs patiënten zo nodig naar Thuisarts: ‘Ik heb misschien extra vitamine D nodig’
Er zijn veel onderzoeken gepubliceerd naar de rol van vitamine D bij COVID-19. Het betreffen grotendeels observationele studies en een groot deel heeft forse methodologische beperkingen. In enkele onderzoeken is de relatie tussen de hoogte van vitamine D en het risico op het krijgen van (een ernstig beloop van) COVID-19 onderzocht. Op basis van deze onderzoeken kan niet geconcludeerd worden of een vitamine D-deficiëntie een verhoogd risico geeft op het krijgen van een ernstiger beloop van COVID-19. In een aantal gerandomiseerde onderzoeken is het gebruik van vitamine D als behandeling van COVID-19 onderzocht. De onderzoeken laten zich echter om verschillende redenen niet goed vergelijken met de populatie in Nederland.
Controles
Naar Samenvatting ›- Monitor het beloop. Vraag de patiënt alert te zijn op achteruitgang.
- Overleg met de patiënt hoe vaak contactmomenten nodig zijn. Dit hangt af van de ernst van de klachten, comorbiditeit en persoonsgebonden factoren.
- Overweeg proactief (eventueel dagelijks) contact te hebben met COVID-19-patiënten die tot een risicogroep behoren (zie Risicogroepen).
- Instrueer de patiënt in ieder geval contact op te nemen bij:
- toename klachten of achteruitgang
- kortademigheid/benauwdheid, extreme vermoeidheid of verminderde inspanningstolerantie
- aanhoudende klachten, terugkerende koorts en/of andere klachten, zoals verwardheid
Consultatie en verwijzing
Naar Samenvatting ›- Overleg bij twijfel met een longarts/internist, bijvoorbeeld bij patiënten met toename klachten of bij patiënten uit een risicogroep.
- De volgende criteria zijn reden tot overleg met een longarts/internist en waarschijnlijk ziekenhuisopname:
- ernstig zieke patiënt
- ademfrequentie in rust > 24/min
- saturatie < 92-94%
- klinische achteruitgang, zoals progressieve dyspneu of inspanningsintolerantie
- Neem hierbij de volgende factoren in overweging:
- patiënten met een lage saturatie lijken geregeld niet benauwd.
- er kan snelle klinische verslechtering optreden.
- een ziekenhuisopname biedt mogelijkheid voor medicatie en ondersteuning door toediening van intraveneus vocht, zuurstof en/of beademing.
- de voor- en nadelen van ziekenhuisopname bij kwetsbare patiënten (zie Evaluatie meerwaarde verwijzing tweede lijn bij kwetsbare patiënten).
- Bij verwijzen per ambulance: informeer de ambulancedienst over (een vermoeden van) COVID-19.
Als patiënten toenemend kortademig worden tijdens het beloop van de ziekte, kan dit berusten op hyperinflammatie als gevolg van het virus (de tweede fase van de ziekte), maar het kan ook het gevolg zijn van bijvoorbeeld een secundaire bacteriële infectie, decompensatio cordis of een veneuze trombo-embolie. Een (toename) van kortademigheid zal meestal een indicatie zijn voor verwijzing naar de tweede lijn.
Evaluatie meerwaarde verwijzing tweede lijn bij kwetsbare patiënten
Naar Samenvatting ›- Weeg bij kwetsbare patiënten de volgende zaken af om te beoordelen of ziekenhuisopname meerwaarde heeft.
- houd rekening met de voor- en nadelen/risico’s van ziekenhuisopname.
- bepaal of ziekenhuisopname met eventueel IC-opname meerwaarde heeft. De Clinical Frailty Score kan hierbij behulpzaam zijn.
- bepaal of aanvullend onderzoek naar en/of behandeling van andere ziektes in het ziekenhuis nodig is.
- bespreek de wensen en doelen van de patiënt.
- Gebruik zo nodig de leidraad Triage thuisbehandeling versus verwijzen naar het ziekenhuis bij oudere patiënt met (verdenking op) COVID-19 bij de keuze om patiënten al dan niet in te sturen en het verdere beleid.
Beleid bij zuurstofbehoeftige, niet-terminale patiënten die niet opgenomen willen worden
Naar Samenvatting ›Patiënten met een ademfrequentie > 24/min in rust of een saturatie < 92-94% hebben een verwijsindicatie. Als ziekenhuisopname niet gewenst is (zie Evaluatie meerwaarde verwijzing tweede lijn bij kwetsbare patiënten), maar herstel nog wel het uitgangspunt is:
- Overweeg of het toegevoegde waarde heeft om de patiënt te verwijzen naar het ziekenhuis voor aanvullende diagnostiek of voor behandeling van andere (behandelbare) aandoeningen waarvoor thuis onvoldoende diagnostische mogelijkheden zijn en bespreek dit met de patiënt.
- Consulteer laagdrempelig een longarts/internist/geriater met het oog op differentiaaldiagnostische overwegingen en ten aanzien van de (zuurstof)behandeling.
- Overweeg thuisbehandeling met zuurstof bij een saturatie < 92% en/of ademfrequentie > 24/min in rust. Bij patiënten met COPD geldt een saturatie < 88-90%, afhankelijk van de uitgangssaturatie. Bespreek de voor- en nadelen met de patiënt. Neem hierin mee of thuisbehandeling praktisch haalbaar is.
- Indien in overleg met de patiënt wordt gekozen voor thuisbehandeling met zuurstof, dan zijn dexamethason (zie Dexamethason) en profylactisch LMWH (zie Tromboseprofylaxe) in het algemeen ook aanbevolen. Voor de indicatie antibiotica, zie Antibiotica.
- Wees alert op (het voorkomen van een) delier (zie NHG-Standaard Delier).
Praktische toepassing zuurstofbehandeling
- Geef zuurstofbehandeling thuis bij een saturatie < 92% en/of ademfrequentie > 24/min in rust (ook zonder klachten van dyspneu en/of vermoeidheid). Houd bij patiënten met COPD een saturatie < 88-90% aan, afhankelijk van de uitgangssaturatie.
- Het doel van zuurstoftoediening is het beperken van de kans op orgaanschade door hypoxie. Mogelijk draagt zuurstof bij aan het comfort van de patiënt.
- Geef zuurstof bij voorkeur via een neusbril. Bij een verstopte neus kan een mondmasker gebruikt worden.
- Start met 2 L/min, draag er zorg voor dat minimaal 30 minuten na start de saturatie in rust gecontroleerd wordt. Streefwaarde zuurstofsaturatie 92-96% (bij patiënten met COPD 88-92%, afhankelijk van de uitgangssaturatie).
- Hoog zo nodig de dosering op met 1 L/min tot maximaal 5 L/min.
- LET OP: Bespreek met patiënt, naasten en wijkverpleging dat snelle achteruitgang mogelijk is en tref voorbereidingen voor de dan benodigde zorg en medicatie (zie Palliatieve zorg).
- Zie voor meer informatie de leidraad zuurstofgebruik thuis bij (verdenking op / bewezen) COVID-19.
Praktische toepassing Dexamethason
Naar Samenvatting ›- Geef een patiënt die thuis behandeld wordt met zuurstof dexamethason 1 dd 6 mg (volwassen dosering, of een equivalente dosering van prednisolon 1 dd 40 mg). Geef het middel maximaal 10 dagen, of korter bij eerder herstel.
- Houd rekening met hyperglykemische ontregeling:
- Volg bij diabetespatiënten het beleid volgens de bijlagen bij de NHG-Standaard Diabetes mellitus type 2: Beleid bij gebruik van corticosteroïden bij patiënten met diabetes mellitus type 2 en Beslisboom Hyperglykemie in de acute fase.
Meer praktische informatie is te vinden in het Protocol Dexamethason en diabetes bij COVID-19. - Verricht bij overige patiënten alleen een glucosemeting bij klachten die passen bij hyperglykemie.
- Volg bij diabetespatiënten het beleid volgens de bijlagen bij de NHG-Standaard Diabetes mellitus type 2: Beleid bij gebruik van corticosteroïden bij patiënten met diabetes mellitus type 2 en Beslisboom Hyperglykemie in de acute fase.
- Er zijn geen gerandomiseerde onderzoeken naar het effect van systemische corticosteroïden bij patiënten met COVID-19 in de eerste lijn.
- In de tweede lijn worden alleen patiënten met COVID-19 bij wie zuurstoftoediening geïndiceerd is behandeld met dexamethason (of een equivalente dosis hydrocortison/prednis(ol)on). Bij opgenomen patiënten met milde COVID-19 zonder indicatie voor zuurstoftoediening wordt dexamethason niet aanbevolen.
- Patiënten met COVID-19 die zuurstofbehoeftig zijn, hebben in het algemeen een opname-indicatie. In enkele gevallen zal gekozen worden om COVID-19-patiënten met een indicatie voor zuurstoftoediening niet op te nemen in het ziekenhuis maar om in de thuissetting zuurstofondersteuning te bieden. Over het behandelen met dexamethason bij deze groep patiënten zijn geen gegevens uit de eerste lijn beschikbaar, maar aangenomen wordt dat deze groep vergelijkbaar is met zuurstofbehoeftige patiënten met COVID-19 op de verpleegafdeling in het ziekenhuis. De verwachting is dat dexamethason ook voor deze specifieke groep patiënten in de eerste lijn effectief is.
Voor- en nadelen
Het is onzeker wat de voor- en nadelen zijn van het gebruik van dexamethason of andere systemische corticosteroïden bij patiënten met COVID-19 in de eerste lijn. Voor patiënten met COVID-19 in het ziekenhuis wordt het gebruik van dexamethason of een equivalente dosis hydrocortison/prednis(ol)on alleen aanbevolen bij patiënten bij wie zuurstofbehandeling geïndiceerd is, omdat systemische corticosteroïden waarschijnlijk de kans op sterfte verlagen.
Patiënten met een indicatie voor zuurstofondersteuning die opgenomen zijn op de verpleegafdeling van een ziekenhuis zijn qua ernst van de ziekte te vergelijken met COVID-19-patiënten met indicatie voor zuurstoftoediening die behandeld worden in de thuissituatie omdat ze niet meer opgenomen willen worden in het ziekenhuis. Wat betreft leeftijd en comorbiditeit zijn thuis behandelde patiënten over het algemeen echter de kwetsbaarste patiënten, waardoor het onzeker is of ze als groep helemaal vergelijkbaar zijn met patiënten die in het ziekenhuis zijn opgenomen.
Vaker voorkomende bijwerkingen (1-10%) van dexamethason zijn maag-darmklachten, verhoogde kans op infecties, hoofdpijn en duizeligheid, spierklachten, veranderingen in gevoel en stemming, toename van bloedglucose en hartritmestoornissen (Bijwerkingencentrum lareb, geraadpleegd juni 2023).
Kwaliteit van bewijs
Er zijn geen onderzoeken beschikbaar over het effect van systemische corticosteroïden bij patiënten met COVID-19 in de eerste lijn.
Waarden en voorkeuren
We zijn onzeker over hoe patiënten de voor- en nadelen van behandeling met systemische corticosteroïden afwegen. Aangezien de middelen uitsluitend geïndiceerd zijn bij zuurstofbehoeftige en dus ernstig zieke patiënten, verwachten we dat een meerderheid van deze patiënten veel waarde zal toekennen aan het voorkómen van overlijden en daarom bereid zal zijn te kiezen voor behandeling met systemische corticosteroïden.
Kosten
De kosten van dexamethason 6 mg 1 dd gedurende 10 dagen zijn ongeveer € 4,40 (www.medicijnkosten.nl, geraadpleegd augustus 2023).
Aanvaardbaarheid
Het betreft kortdurende orale behandeling waarbij wij weinig problemen verwachten met de aanvaardbaarheid.
Haalbaarheid
Dexamethason is een geregistreerd geneesmiddel. Er zijn geen problemen op het gebied van de haalbaarheid.
Uitgangsvraag
Is dexamethason (I) aan te bevelen bij de behandeling van patiënten met milde tot matige COVID-19-klachten in de huisartspraktijk (P)?
|
PICO |
|
|
Patiënten |
Patiënten met milde tot matige COVID-19-klachten in de huisartsenpraktijk |
|
Interventie |
Dexamethason |
|
Vergelijking |
Geen dexamethason |
|
Uitkomstmaten |
Cruciaal:
Belangrijk:
|
Achtergrond
Systemische corticosteroïden zijn waarschijnlijk effectief in het verlagen van de kans op sterfte bij patiënten met COVID-19 die in het ziekenhuis opgenomen zijn met een indicatie voor zuurstoftoediening. FMS en SWAB concluderen dit in hun richtlijn op basis van 11 RCT’s over systemische corticosteroïden bij patiënten met COVID-19 die opgenomen waren in het ziekenhuis. Het grootste effect van systemische corticosteroïden werd gevonden bij de meest ernstig zieke patiënten met COVID-19. In de tweede lijn wordt daarom aanbevolen om patiënten met COVID-19 bij wie zuurstoftoediening geïndiceerd is te behandelen met dexamethason of een equivalente dosis hydrocortison/prednisolon.
De FMS/SWAB-richtlijn concludeert over in het ziekenhuis opgenomen patiënten met milde COVID-19 (zonder zuurstofondersteuning) dat behandeling met dexamethason bij deze groep patiënten de kans op sterfte mogelijk juist verhoogt. Dit concluderen zij op basis van 1 groot onderzoek bij ruim 6000 geïncludeerde patiënten. Behandeling met systemische corticosteroïden bevelen ze daarom niet aan bij opgenomen patiënten met COVID-19 zonder indicatie voor zuurstofbehandeling.
Patiënten in de huisartsenpraktijk verschillen doorgaans van gehospitaliseerde patiënten wat betreft leeftijd, comorbiditeit en ernst van de symptomen. Het is daarom onduidelijk of systemische corticosteroïden aan te bevelen zijn bij patiënten met COVID-19 in de eerste lijn.
Methoden
Er is een systematische literatuurzoekactie naar systematische reviews (SR´s), randomized controlled trials (RCT’s) en observationeel onderzoek uitgevoerd in PubMed en Embase op 18 augustus 2020. Daarnaast is via bioRxiv (biorxiv.org), Preprints (preprints.org), EuropePMC (europepmc.org) en Medrxiv (medrxiv.org) gezocht naar preprints.
Om geen recente onderzoeken te missen werd de zoekactie maandelijks herhaald; de laatste zoekactie was in augustus 2023.
Resultaten
Resultaat zoekactie
De oorspronkelijke zoekactie leverde geen geschikte SR´s, RCT’s of observationele onderzoeken op over de effectiviteit van dexamethason bij COVID-19-patiënten in de eerste lijn. Bij diverse updates van de zoekactie werd alleen een cochranereview over systemische corticosteroïden voor de behandeling van COVID-19 gevonden. In deze SR is gezocht naar RCT’s bij zowel patiënten die in het ziekenhuis waren opgenomen als RCT’s bij niet-opgenomen patiënten. Over de laatste categorie vonden de auteurs geen gepubliceerd onderzoek.
Conclusies
Er zijn geen onderzoeken beschikbaar over het effect van systemische corticosteroïden bij patiënten met COVID-19 in de eerste lijn.
Praktische toepassing Tromboseprofylaxe
Naar Samenvatting ›- Bespreek de voor- en nadelen van profylactisch LMWH met de patiënt als deze thuis behandeld wordt met zuurstof, en betrek de patiënt bij de keuze. Mogelijk voorkomt behandeling met LMWH een veneuze trombo-embolische complicatie bij COVID-19. Wel neemt het risico op bloedingen bij LMWH-gebruik toe, vooral bij kwetsbare ouderen. Daarnaast wordt de patiënt belast met injecties.
- Schrijf geen profylactisch LMWH voor als de patiënt al anticoagulantia (vitamine K-antagonisten, DOAC’s) gebruikt.
- Bij keuze voor profylaxe bij volwassenen:
- geef, zolang de patiënt behandeld wordt met zuurstof, enoxaparine subcutaan 1 dd 4000 IE (= 40 mg) (voorkeur op basis van kosten), nadroparine subcutaan 1 dd 2850 IE of dalteparine subcutaan 1 dd 5000 IE.
- verdubbel de dosering bij patiënten met een BMI ≥ 40.
- bij een verminderde nierfunctie is aanpassing van de dosering niet nodig.
- instrueer de patiënt of mantelzorger hoe de injecties zelf toe te dienen.
Op basis van het huidige bewijs lijkt tromboseprofylaxe geen effect te hebben in het voorkomen van ziekenhuisopname, overlijden en trombo-embolische complicaties bij niet-opgenomen patiënten met COVID-19. De werkgroep geeft daarom een sterk negatieve aanbeveling voor tromboseprofylaxe.
Voor COVID-19-patiënten die thuis behandeld worden met zuurstof en dexamethason geeft de werkgroep een zwak-positieve aanbeveling. Hoewel zuurstofbehoeftige COVID-19-patiënten een opname-indicatie hebben, wenst een klein deel van deze patiënten geen ziekenhuisopname en zij worden thuis behandeld (zie Beleid bij zuurstofbehoeftige, niet-terminale patiënten die niet opgenomen willen worden). Voor hen lijkt het risico op een veneuze trombo-embolische complicatie verhoogd, overeenkomstig met patiënten op de verpleegafdeling van het ziekenhuis. Voor zuurstofbehoeftige COVID-19-patiënten die thuis behandeld worden met zuurstof heeft de werkgroep daarom besloten om aan te sluiten bij de richtlijnmodule van de NIV waarin profylactisch LMWH wordt aanbevolen aan patiënten die in verband met COVID-19 worden opgenomen in het ziekenhuis.
Gewenste en ongewenste effecten
Op basis van meerdere onderzoeken die allemaal voortijdig zijn gestopt, lijkt tromboseprofylaxe bij niet-opgenomen COVID-19-patiënten niet effectief in het voorkomen van een veneuze trombo-embolische complicatie, ziekenhuisopname of overlijden. Daarentegen kan tromboseprofylaxe wel bijwerkingen veroorzaken.
Vaker voorkomende bijwerkingen van rivaroxaban zijn bloedingen, anemie, verminderde nierfunctie, duizeligheid, hoofdpijn, hypotensie, jeuk, huiduitslag, ecchymose, maagdarmklachten, pijn in de extremiteiten, perifeer oedeem, koorts, vermoeidheid, asthenie en stijging van ASAT en ALAT. Zeer vaak voorkomende bijwerkingen van enoxaparine zijn bloedingen en stijging van ASAT en ALAT. Vaker voorkomende bijwerkingen van enoxaparine zijn trombocytose, trombocytopenie, overgevoeligheidsreacties, jeuk, erytheem, pijn en reacties op de toedieningsplaats (KNMP Kennisbank, geraadpleegd augustus 2023).
Tromboseprofylaxe lijkt wel effectief bij patiënten met COVID-19 die dermate ziek zijn dat zij opgenomen liggen in het ziekenhuis. Patiënten met COVID-19 die zuurstofbehoeftig zijn maar niet naar het ziekenhuis willen, zijn vergelijkbaar wat betreft de mate van ziek zijn met patiënten opgenomen in het ziekenhuis. Voor deze groep patiënten kan tromboseprofylaxe wel een voordeel hebben.
Kwaliteit van bewijs
De kwaliteit van bewijs is laag wegens een ernstig risico op bias (alle onderzoeken zijn voortijdig gestopt) en door onnauwkeurigheid (laag aantal events).
Waarden en voorkeuren
We verwachten dat de meeste patiënten de nadelen van behandeling met tromboseprofylaxe zwaarder vinden wegen dan de mogelijke voordelen, aangezien het middel enkel van meerwaarde lijkt te zijn bij ernstig zieke patiënten. We verwachten dat alleen ernstig zieke patiënten waarde zullen toekennen aan behandeling met tromboseprofylaxe.
Kosten
De kosten van enoxaparine 4000 IE zijn € 2,88 per dag; de kosten van rivaroxaban 10 mg (de dosering in de onderzoeken) is € 2,15 per dag (www.medicijnkosten.nl, geraadpleegd oktober 2023).
Aanvaardbaarheid
Het betreft kortdurende orale behandeling of in het geval van LMWH een behandeling met dagelijks 1 injectie waarbij sommige patiënten mogelijk problemen ervaren met de aanvaardbaarheid.
Haalbaarheid
Voor het plaatsen van een injectie LMWH moet de patiënt en/of mantelzorger(s) geïnstrueerd worden of moet er thuiszorg zijn. Er kunnen daarom problemen zijn op het gebied van de haalbaarheid.
Uitgangsvraag
Is tromboseprofylaxe (acetylsalicylzuur, LMWH, directe orale anticoagulantia (DOAC)) aan te bevelen bij (een specifieke groep) patiënten met COVID-19 in de huisartsenpraktijk?
| Patiënten | Volwassen patiënten met bevestigde COVID-19 met klachten in de huisartsenpraktijk |
|---|---|
| Interventie | Tromboseprofylaxe (acetylsalicylzuur, LMWH, DOAC) |
| Vergelijking | Placebo, gebruikelijke zorg |
| Uitkomstmaten |
Cruciaal:
Belangrijk:
|
De NHG-werkgroep heeft de volgende grenzen voor klinisch relevante verschillen vastgesteld:
- ziekenhuisopname: absolute daling ≥ 2%
- overlijden: absolute daling ≥ 1%
- bijwerkingen: absolute stijging 10%
De grenzen van klinische relevantie kunnen verschillen tussen middelen onderling (zie Totstandkoming).
Achtergrond
De incidentie van trombo-embolische complicaties is substantieel verhoogd bij opgenomen patiënten met COVID-19. In de richtlijnmodule van de Nederlandse Internisten Vereniging (NIV) wordt aanbevolen om tromboseprofylaxe te geven aan alle patiënten die opgenomen zijn in het ziekenhuis met COVID-19, waarbij voor COVID-19-patiënten op de verpleegafdeling zowel de lage als de intermediaire dosering profylactisch LMWH overwogen kan worden. Een therapeutische dosering wordt niet aanbevolen. De arteriële en veneuze trombose die bij ernstige COVID-19 gezien wordt, bestaat vaak uit microvasculaire trombose in de longvaten, een ander type trombose dan gewoonlijk gezien wordt bij een diepveneuze trombose (DVT) of longembolie.
Patiënten in de huisartsenpraktijk verschillen doorgaans van gehospitaliseerde patiënten wat betreft leeftijd, comorbiditeit en ernst van de symptomen. Voor de eerste lijn is het van belang te weten of gebruik van tromboseprofylaxe bij COVID-19-patiënten in de huisartsenpraktijk beschermt tegen trombo-embolische complicaties. Uit onderzoek blijkt dat de incidentie van een veneuze trombo-embolie (VTE) bij COVID-19-patiënten die in de thuissetting behandeld worden zeer laag is.
Het is onbekend of patiënten met een verhoogd risico op een DVT of longembolie op basis van hun voorgeschiedenis (doorgemaakte VTE of vanwege een actieve maligniteit), een extra verhoogd risico hebben op een VTE als complicatie bij COVID-19.
Methoden
Er werd een literatuuronderzoek verricht met bovenstaande zoekvraag op 18 februari 2022. Om geen recente onderzoeken te missen werd de zoekactie maandelijks herhaald; de laatste zoekactie was in augustus 2023.
Resultaten
Resultaat zoekactie
De oorspronkelijke zoekactie leverde 2 RCT’s op naar de effectiviteit van tromboseprofylaxe bij COVID-19. Bij diverse updates van de zoekactie vonden we een cochranereview over profylactische anticoagulantia bij niet-opgenomen patiënten met COVID-19. In deze review voldeden 4 geïncludeerde RCT’s aan onze inclusiecriteria. Daarnaast vonden we 2 aanvullende RCT’s. Alle onderzoeken werden voortijdig gestopt vanwege futiliteit bij tussentijdse analyse, vanwege tegenvallende werving van deelnemers en/of vanwege een lager dan verwacht aantal events.
Onderzoekskarakteristieken
- Ananworanich 2021: fase 2b-RCT over rivaroxaban in vergelijking met placebo ter voorkoming van ziekteprogressie in niet-opgenomen patiënten met milde klachten van COVID-19 en een verhoogd risico op een ernstig beloop (n = 497, Verenigde Staten).
- Barco 2022: open-label RCT over enoxaparine in vergelijking met gebruikelijke zorg bij niet-opgenomen patiënten met COVID-19 ≥ 50 jaar ter voorkoming van trombo-embolische complicaties, ziekenhuisopname of overlijden (n = 472, Zwitserland en Duitsland).
- Connors 2021: dubbelblind placebogecontroleerde RCT over acetylsalicylzuur en apixaban in vergelijking met placebo bij niet-opgenomen patiënten met klachten van COVID-19 ter voorkoming van trombo-embolische complicaties, ziekenhuisopname en overlijden (n = 657, Verenigde Staten).
- Cools 2022: open-label RCT over enoxaparine in vergelijking met gebruikelijke zorg bij niet-opgenomen patiënten met een verhoogd risico op een ernstig beloop ter voorkoming van trombo-embolische complicaties, ziekenhuisopname of overlijden (n = 219, meerdere landen).
- Avezum 2023: open-label RCT over rivaroxaban in vergelijking met gebruikelijke zorg bij niet-opgenomen patiënten met waarschijnlijk of bevestigd COVID-19 en minimaal twee risicofactoren voor een gecompliceerd beloop ter voorkoming van trombo-embolische complicaties of overlijden (n = 660, Brazilië).
- Piazza 2023: dubbelblind placebogecontroleerde RCT over rivaroxaban in vergelijking met placebo bij niet-opgenomen patiënten met een risicofactor voor trombose ter voorkoming van trombo-embolische complicaties, ziekenhuisopname of overlijden (n = 1284, Verenigde Staten).
Effectiviteit en bijwerkingen
Zie de tabel voor de samenvatting van de resultaten. Vaker voorkomende bijwerkingen van rivaroxaban (onderzochte tromboseprofylaxe bij meerderheid van de onderzoeken) zijn bloedingen (na de ingreep, gastro-intestinaal, rectaal, van het tandvlees, urogenitaal, van de ogen), neusbloeding, hematoom, anemie, verminderde nierfunctie, duizeligheid, hoofdpijn, hypotensie, jeuk, huiduitslag, ecchymose, dyspepsie, buikpijn, misselijkheid, braken, diarree, obstipatie, pijn in de extremiteiten, perifeer oedeem, koorts, vermoeidheid, asthenie en stijging van ASAT en ALAT (KNMP Kennisbank, geraadpleegd augustus 2023).
Conclusie
- Tromboseprofylaxe verlaagt waarschijnlijk niet of nauwelijks de kans op ziekenhuisopname (kwaliteit van bewijs: redelijk).
- Tromboseprofylaxe verlaagt mogelijk niet of nauwelijks de kans op overlijden of veneuze trombo-embolie (kwaliteit van bewijs: laag).
- Er is mogelijk niet of nauwelijks verschil in het optreden van een ernstige bloeding (kwaliteit van bewijs: laag).
Palliatieve zorg
Naar Samenvatting ›- Bespreek met de patiënt en eventuele naasten dat COVID-19 in de terminale fase een grillig, plots en lastig te voorspellen beloop kent. Als terminale patiënten komen te overlijden, is het sterfbed vaak zeer kort.
- Voor de medicamenteuze behandeling per symptoom, zie:
Organisatie van de zorg
Naar Samenvatting ›Infectiepreventie
Naar Samenvatting ›Voor algemene adviezen over infectiepreventie, zie de richtlijn Infectiepreventie in de praktijk; voor specifieke adviezen over infectiepreventie ten aanzien van luchtweginfecties, zie de adviezen in het NHG-dossier Infectieziekten.
Referenties
- LCI. Handreiking maatregelen bij clusters en regionale verspreiding van COVID-19; Bijlage bij LCI-richtlijn COVID-19. Geraadpleegd november 2020a. Ga naar bron: LCI. Handreiking maatregelen bij clusters en regionale verspreiding van COVID-19; Bijlage bij LCI-richtlijn COVID-19. Geraadpleegd november 2020a.
- RIVM. Epidemiologische situatie van SARS-CoV-2 in Nederland 23-2-2021b. Ga naar bron: RIVM. Epidemiologische situatie van SARS-CoV-2 in Nederland 23-2-2021b.
- LCI. Richtlijn COVID-19. Geraadpleegd maart 2021a. Ga naar bron: LCI. Richtlijn COVID-19. Geraadpleegd maart 2021a.
- FMS. Leidraad Medische procedures die een infectieuze aerosol genereren (IAGP) met SARS-CoV-2. 2020a. Ga naar bron: FMS. Leidraad Medische procedures die een infectieuze aerosol genereren (IAGP) met SARS-CoV-2. 2020a.
- LCI. Heroverweging mondneusmaskerbeleid in de zorg vanwege de Britse variant van SARS-CoV-2; Onderbouwing en achtergrond bij LCI-richtlijn COVID-19. Geraadpleegd maart 2021c. Ga naar bron: LCI. Heroverweging mondneusmaskerbeleid in de zorg vanwege de Britse variant van SARS-CoV-2; Onderbouwing en achtergrond bij LCI-richtlijn COVID-19. Geraadpleegd maart 2021c.
- Neumann-Podczaska A, Al-Saad SR, Karbowski LM, Chojnicki M, Tobis S, Wieczorowska-Tobis K. COVID-19 - Clinical picture in the elderly population: a qualitative systematic review. Aging Dis 2020;11:988-1008.
- Olde Rikkert MG, Vingerhoets RW, Van Geldorp N, De Jong E, Maas HA. Atypisch beeld van COVID-19 bij oudere patiënten. Ned Tijdschr Geneeskd 2020;164:D5004
- Viner RM, Ward JL, Hudson LD, Ashe M, Patel SV, Hargreaves D, Whittaker E. Systematic review of reviews of symptoms and signs of COVID-19 in children and adolescents. Arch Dis Child 2020-320972. Online ahead of print.
- LCI. Inhoudelijke onderbouwing ten behoeve van symptomatologie COVID-19 en consequenties voor testen en maatregelen; Onderbouwing en achtergrond bij LCI-richtlijn COVID-19. Geraadpleegd december 2020b Ga naar bron: LCI. Inhoudelijke onderbouwing ten behoeve van symptomatologie COVID-19 en consequenties voor testen en maatregelen; Onderbouwing en achtergrond bij LCI-richtlijn COVID-19. Geraadpleegd december 2020b
- Conforti C, Dianzani C, Agozzino M, Giuffrida R, Marangi GF, Meo ND, et al. Cutaneous manifestations in confirmed COVID-19 patients: a systematic review. Biology (Basel) 2020;9:449.
- Mirza FN, Malik AA, Omer SB, Sethi A. Dermatologic manifestations of COVID-19: a comprehensive systematic review. Int J Dermatol 2021;60:418-50.
- Piazza G, Campia U, Hurwitz S, Snyder JE, Rizzo SM, Pfeferman MB, et al. Registry of arterial and venous thromboembolic complications in patients with COVID-19. J Am Coll Cardiol 2020;76:2060-72.
- Aktaa S, Wu J, Nadarajah R, Rashid M, De Belder M, Deanfield J, et al. Incidence and mortality due to thromboembolic events during the COVID-19 pandemic: multi-sourced population-based health records cohort study. Thromb Res. 2021;202:17-23.
- Giannis D, Barish MA, Goldin M, Cohen SL, Kohn N, Gianos E, et al. Incidence of Venous Thromboembolism and Mortality in Patients with Initial Presentation of COVID-19. J Thromb Thrombolysis. 2021:1–5.
- Middeldorp S, Coppens M, Van Haaps TF, Foppen M, Vlaar AP, Müller MCA, et al. Incidence of venousthromboembolism in hospitalized patients with COVID-19. J Thromb Haemost 2020;18:1995-2002.
- Kahn SR, Lim W, Dunn AS, Cushman M, Dentali F, Akl EA, et al. Prevention of VTE in nonsurgical patients: antithrombotic therapy and prevention of thrombosis, 9th ed: American college of chest physicians evidence-based clinical practice guidelines. Chest 2012;141(2 Suppl):e195S-e226S.
- Thachil J, Tang N, Gando S, Falanga A, Cattaneo M, Levi M, et al. ISTH interim guidance on recognition and management of coagulopathy in COVID-19. J Thromb Haemost 2020;18:1023-6.
- Klok FA, Kruip MJHA, Van der Meer NJM, Arbous MS, Gommers D, Kant KM, et al. Confirmation of the high cumulative incidence of thrombotic complications in critically ill ICU patients with COVID-19: an updated analysis. Thromb Res 2020;191:148-50.
- Wynants L, Van Calster B, Collins GS, Riley RD, Heinze G, Schuit E, et al. Prediction models for diagnosis and prognosis of COVID-19 infection: systematic review and critical appraisal. BMJ 2020;369:m1328.
- Clift AK, Coupland CAC, Keogh RH, Diaz-Ordaz K, Williamson E, Harrison EM, et al. Living risk prediction algorithm (QCOVID) for risk of hospital admission and mortality from coronavirus 19 in adults: national derivation and validation cohort study. BMJ 2020;371:m3731.
- Gezondheidsraad. Strategieën voor COVID-19-vaccinatie. 2020. Ga naar bron: Gezondheidsraad. Strategieën voor COVID-19-vaccinatie. 2020.
- Sze S, Pan D, Nevill CR, Gray LJ, Martin CA, Nazareth J, et al. Ethnicity and clinical outcomes in COVID-19: a systematic review and meta-analysis. E Clinical Medicine 2020;29:100630.
- Raharja A, Tamara A, Kok LT. Association between ethnicity and severe COVID-19 disease: a systematic review and meta-analysis. J Racial Ethn Health Disparities 2020;12:1-10.
- NVOG 2022a. Richtlijnmodule COVID-19 en zwangerschap, bevalling en kraambed Ga naar bron: NVOG 2022a. Richtlijnmodule COVID-19 en zwangerschap, bevalling en kraambed
- LCI. Zwangerschap, (werk) en COVID-19; Bijlage bij de LCI-richtlijn COVID-19. Geraadpleegd april 2022. Ga naar bron: LCI. Zwangerschap, (werk) en COVID-19; Bijlage bij de LCI-richtlijn COVID-19. Geraadpleegd april 2022.
- NVOG 2022b. Standpunt Vaccinatie tegen COVID-19 rondom kinderwens, zwangerschap en kraambed Ga naar bron: NVOG 2022b. Standpunt Vaccinatie tegen COVID-19 rondom kinderwens, zwangerschap en kraambed
- RIVM. Kinderen, school en COVID-19. Geraadpleegd april 2021. Ga naar bron: RIVM. Kinderen, school en COVID-19. Geraadpleegd april 2021.
- Badal S, Thapa Bajgain K, Badal S, Thapa R, Bajgain BB, Santana MJ. Prevalence, clinical characteristics, and outcomes of pediatric COVID-19: a systematic review and meta-analysis. J Clin Virol 2020;135:104715.
- Blink M, Buddingh EP, Willems A, Brouwer CNM, Brinkman DMC, Hahurij ND, Klein RH. Handreiking COVID-19 geassocieerd multisysteem inflammatoir syndroom (MIS-C). NVK 2021. Ga naar bron: Blink M, Buddingh EP, Willems A, Brouwer CNM, Brinkman DMC, Hahurij ND, Klein RH. Handreiking COVID-19 geassocieerd multisysteem inflammatoir syndroom (MIS-C). NVK 2021.
- World Health Organization. Multisystem inflammatory syndrome in children and adolescents with COVID-19. Geraadpleegd maart 2021b. Ga naar bron: World Health Organization. Multisystem inflammatory syndrome in children and adolescents with COVID-19. Geraadpleegd maart 2021b.
- Blink M, Buddingh EP, Filippini LHPM, Brinkman DMC, Joosten SA, Klein RH. Covid-19-geassocieerde hyperinflammatie. Hyperinflammatoire status met perimyocarditis bij een 15-jarig meisje. Ned Tijdschr Geneeskd 2020;164:D5348.
- Luks AM, Swenson ER. Pulse oximetry for monitoring patients with COVID-19 at Home. Potential pitfalls and practical guidance. Ann Am Thorac Soc 2020;17:1040-6.
- Watson J, Whiting PF, Brush JE. Interpreting a covid-19 test result. BMJ 2020;369:m1808.
- LCI. COVID-19: Welke (groepen) personen kunnen met welke test(en) worden getest? Onderbouwing en achtergrond bij LCI-richtlijn COVID-19. Geraadpleegd maart 2021b. Ga naar bron: LCI. COVID-19: Welke (groepen) personen kunnen met welke test(en) worden getest? Onderbouwing en achtergrond bij LCI-richtlijn COVID-19. Geraadpleegd maart 2021b.
- RIVM. Status validatie SARS-CoV-2 antigeen sneltesten, status per 27 mei 2021a. Ga naar bron: RIVM. Status validatie SARS-CoV-2 antigeen sneltesten, status per 27 mei 2021a.
- RIVM. OMT Advies antigeen(snel)testen. 2020. Ga naar bron: RIVM. OMT Advies antigeen(snel)testen. 2020.
- RIVM. Verschillende type testen. Geraadpleegd maart 2021c. Ga naar bron: RIVM. Verschillende type testen. Geraadpleegd maart 2021c.
- Møller IJB, Utke AR, Rysgaard UK, Østergaard LJ, Jespersen S. Diagnostic performance, user acceptability, and safety of unsupervised SARS-CoV-2 rapid antigen-detecting tests performed at home. Int J Infect Dis. 2022;116:358-364.
- Nikolai O, Rohardt C, Tobian F, Junge A, Corman VM, Jones TC, et al. Anterior nasal versus nasal mid-turbinate sampling for a SARS-CoV-2 antigen-detecting rapid test: does localisation or professional collection matter? Infect Dis (Lond). 2021;53(12):947-952.
- Cassuto NG, Gravier A, Colin M, Theillay A, Pires-Roteira D, Pallay S, et al. Evaluation of a SARS-CoV-2 antigen-detecting rapid diagnostic test as a self-test: diagnostic performance and usability. J Med Virol. 2021;93(12):6686-6692.
- Stohr JJJM, Zwart VF, Goderski G, Meijer A, Nagel-Imming CRS, Kluytmans-van den Bergh MFQ, et al. Self-testing for the detection of SARS-CoV-2 infection with rapid antigen tests for people with suspected COVID-19 in the community. Clin Microbiol Infect. 20214:S1198-743X(21)00434-1.
- LCI. Richtlijn COVID-19. Geraadpleegd februari 2022
- Taskforce serologie. Report status of the validation of ELISA and auto-analyser antibody tests for SARS-CoV-2 diagnostics: considerations for use. RIVM 15 juli 2020a. Ga naar bron: Taskforce serologie. Report status of the validation of ELISA and auto-analyser antibody tests for SARS-CoV-2 diagnostics: considerations for use. RIVM 15 juli 2020a.
- Taskforce serologie. Report status of the validation of point-of-care serology tests for SARS-CoV-2 diagnostics: considerations for use. RIVM 15 juli 2020b. Ga naar bron: Taskforce serologie. Report status of the validation of point-of-care serology tests for SARS-CoV-2 diagnostics: considerations for use. RIVM 15 juli 2020b.
- EMA. EMA gives advice on the use of non-steroidal anti-inflammatories for COVID-19. 2020a. Ga naar bron: EMA. EMA gives advice on the use of non-steroidal anti-inflammatories for COVID-19. 2020a.
- Kennisbank KNMP. Geraadpleegd op 30-04-2021.
- Halpin DM, Faner R, Sibila O, Badia JR, Agusti A. Do chronic respiratory diseases or their treatment affect the risk of SARS-CoV-2 infection? Lancet Respir Med 2020;8:436-38.
- Ramakrishnan S, Nicolau DV, Jr., Langford B, Mahdi M, Jeffers H, Mwasuku C, et al. Inhaled budesonide in the treatment of early COVID-19 (STOIC): a phase 2, open-label, randomised controlled trial. Lancet Respir Med 2021;9:763-72.
- Yu LM, Bafadhel M, Dorward J, Hayward G, Saville BR, Gbinigie O, et al. Inhaled budesonide for COVID-19 in people at high risk of complications in the community in the UK (PRINCIPLE): a randomised, controlled, open-label, adaptive platform trial. Lancet 2021;398:843-55.
- Ezer N, Belga S, Daneman N, Chan A, Smith BM, Daniels SA, et al. Inhaled and intranasal ciclesonide ort he treatment of covid-19 in adult outpatients: CONTAIN phase II randomised controlled trial. BMJ. 2021;375:e068060.
- Clemency BM, Varughese R, Gonzalez-Rojas Y, Morse CG, Phipatanakul W, Koster DJ, et al. Efficacy of Inhaled Ciclesonide for Outpatient Treatment of Adolescents and Adults With Symptomatic COVID-19: A Randomized Clinical Trial. JAMA Intern Med. 2022;182(1):42-49.
- SWAB. Addendum recommendations for antibacterial therapy in adults with COVID-19. 2020. Ga naar bron: SWAB. Addendum recommendations for antibacterial therapy in adults with COVID-19. 2020.
- Karami Z, Knoop BT, Dofferhoff ASM, Blaauw MJT, Janssen NA, Van Apeldoorn M, et al. Few bacterial co-infections but frequent empiric antibiotic use in the early phase of hospitalized patients with COVID-19: results from a multicentre retrospective cohort study in The Netherlands. Infect Dis (Lond) 2021;53:102-10.
- Langford BJ, So M, Raybardhan S, Leung V, Westwood D, MacFadden DR, et al. Bacterial co-infection and secondary infection in patients with COVID-19: a living rapid review and meta-analysis. Clin Microbiol Infect 2020;26:1622-9.
- SWAB. Management of community-acquired pneumonia in adults: 2016 Guideline update from the Dutch working party on antibiotic policy (SWAB) and Dutch association of chest physicians (NVALT). 2016. Ga naar bron: SWAB. Management of community-acquired pneumonia in adults: 2016 Guideline update from the Dutch working party on antibiotic policy (SWAB) and Dutch association of chest physicians (NVALT). 2016.
- Arbel R, Wolff Sagy Y, Hoshen M, Battat E, Lavie G, Sergienko R, et al. Nirmatrelvir Use and Severe Covid-19 Outcomes during the Omicron Surge. N Engl J Med. 2022;387:790-798.
- RIVM. Gedragswetenschappelijk onderzoek COVID-19; Resultaten onderzoek gedragsregels en welbevinden; Draagvlak. Geraadpleegd 16-02-2022. Draagvlak | RIVM
- Owen DR, Allerton CMN, Anderson AS, Aschenbrenner L, Avery M, Berritt S, et al. An oral SARS-CoV-2 M(pro) inhibitor clinical candidate for the treatment of COVID-19. Science. 2021;374(6575):1586-1593.
- Hammond J, Leister-Tebbe H, Gardner A, Abreu P, Bao W, Wisemandle W, et al; EPIC-HR Investigators. Oral Nirmatrelvir for High-Risk, Nonhospitalized Adults with Covid-19. N Engl J Med. 2022;386(15):1397-1408.
- Lareb. Overview hydroxychloroquine. 2020. Geraadpleegd op 30 juli 2020. Ga naar bron: Lareb. Overview hydroxychloroquine. 2020. Geraadpleegd op 30 juli 2020.
- SWAB. Leidraad medicamenteuze behandeling voor patiënten met COVID-19 (infectie met SARS–CoV-2). Geraadpleegd maart 2021 Ga naar bron: SWAB. Leidraad medicamenteuze behandeling voor patiënten met COVID-19 (infectie met SARS–CoV-2). Geraadpleegd maart 2021
- Cavalcanti AB, Zampieri FG, Rosa RG, Azevedo LCP, Veiga VC, Avezum A, et al. Coalition Covid-19 Brazil I Investigators. Hydroxychloroquine with or without azithromycin in mild-to-moderate Covid-19. N Engl J Med 2020;383:2041-52.
- Tenforde MW, Billig Rose E, Lindsell CJ, Shapiro NI, Files DC, Gibbs KW, et al. CDC COVID-19 response team. Characteristics of adult outpatients and inpatients with COVID-19 - 11 Academic medical centers, United States, March-May 2020. MMWR Morb Mortal Wkly Rep 2020;69:841-6.
- Guyatt GH, Oxman AD, Kunz R, Woodcock J, Brozek J, Helfand M, et al. GRADE Working Group. GRADE guidelines: 8. Rating the quality of evidence--indirectness. J Clin Epidemiol 2011;64:1303-10.
- Tanni SE, Bacha HA, Naime A, Bernardo WM. Use of hydroxychloroquine to prevent SARS-CoV-2 infection and treat mild COVID-19: a systematic review and meta-analysis. J Bras Pneumol. 2021;47(5):e20210236.
- Skipper CP, Pastick KA, Engen NW, Bangdiwala AS, Abassi M, Lofgren SM, et al. Hydroxychloroquine in nonhospitalized adults with early COVID-19 : a randomized trial. Ann Intern Med 2020;173:623-31.
- Mitjà O, Corbacho-Monné M, Ubals M, Tebe C, Peñafiel J, Tobias A, et al. BCN PEP-CoV-2 research group. Hydroxychloroquine for early treatment of adults with mild Covid-19: a randomized-controlled trial. Clin Infect Dis 2020:ciaa1009. Published online ahead of print, 2020 Jul 16.
- Omrani AS, Pathan SA, Thomas SA, Harris TRE, Coyle PV, Thomas CE, et al. Randomized double-blinded placebo-controlled trial of hydroxychloroquine with or without azithromycin for virologic cure of non-severe Covid-19. EClinicalMedicine. 2020;29:100645.
- Reis G, Moreira Silva EA, Medeiros Silva DC, Thabane L, Singh G, Park JJ, et al. Effect of early treatment with hydroxychloroquine or lopinavir and ritonavir on risk of hospitalization among patients with COVID-19: the TOGETHER Randomized Clinical Trial. JAMA Netw Open 2021;4:e216468.
- Johnston C, Brown ER, Stewart J, Karita HCS, Kissinger PJ, Dwyer J, et al. Hydroxychloroquine with or without azithromycin for treatment of early SARS-CoV-2 infection among high-risk outpatient adults: a randomized clinical trial. E Clin Med 2021;33:100773.
- Schwartz I, Boesen ME, Cerchiaro G, Doram C, Edwards BD, Ganesh A, et al.; ALBERTA HOPE COVID-19 Collaborators. Assessing the efficacy and safety of hydroxychloroquine as outpatient treatment of COVID-19: a randomized controlled trial. CMAJ Open. 2021 Jun 18;9(2):E693-E702.
- Rodrigues C, Freitas-Santos RS, Levi JE, Senerchia AA, Lopes ATA, Santos SR, et al. Hydroxychloroquine plus azithromycin early treatment of mild COVID-19 in an outpatient setting: a randomized, double-blinded, placebo-controlled clinical trial evaluating viral clearance. Int J Antimicrob Agents. 2021;58(5):106428.
- Kennisbank KNMP. Geraadpleegd op 21-1-2021.
- Popp M, Stegemann M, Metzendorf MI, Gould S, Kranke P, Meybohm P, et al. Ivermectin for preventing and treating COVID-19. Cochrane Database Syst Rev. 2021;7(7):CD015017.
- Chaccour C, Casellas A, Blanco-Di Matteo A, Pineda I, Fernandez-Montero A, Ruiz-Castillo P, et al. The effect of early treatment with ivermectin on viral load, symptoms and humoral response in patients with non-severe COVID-19: A pilot, double-blind, placebo-controlled, randomized clinical trial. E Clin Med 2021;32:100720.
- López-Medina E, López P, Hurtado IC, Dávalos DM, Ramirez O, Martínez E, et al. Effect of ivermectin on time to resolution of symptoms among adults with mild COVID-19: a Randomized Clinical Trial. JAMA 2021;325:1426-35.
- Vallejos J, Zoni R, Bangher M, Villamandos S, Bobadilla A, Plano F, et al. Ivermectin to prevent hospitalizations in patients with COVID-19 (IVERCOR-COVID19) a randomized, double-blind, placebo-controlled trial. BMC Infect Dis 2021;21:635.
- Buonfrate D, Chesini F, Martini D, Roncaglioni MC, Ojeda Fernandez ML, Alvisi MF, et al. High-dose ivermectin for early treatment of COVID-19 (COVER study): a randomised, double-blind, multicentre, phase II, dose-finding, proof-of-concept clinical trial. Int J Antimicrob Agents. 2022;59(2):106516.
- Reis G, Silva EASM, Silva DCM, Thabane L, Milagres AC, Ferreira TS, et al; TOGETHER Investigators. Effect of Early Treatment with Ivermectin among Patients with Covid-19. N Engl J Med. 2022;386(18):1721-1731.
- Abbas KU, Muhammad S, Ding SF. The Effect of Ivermectin on Reducing Viral Symptoms in Patients with Mild COVID-19. Indian J Pharm Sci 2022;84(1) Spl Issue 87-91.
- Popp M, Reis S, Schießer S, Hausinger RI, Stegemann M, Metzendorf MI, et al. Ivermectin for preventing and treating COVID-19. Cochrane Database Syst Rev. 2022;6:CD015017.
- Bramante CT, Huling JD, Tignanelli CJ, Buse JB, Liebovitz DM, Nicklas JM, et al; COVID-OUT Trial Team. Randomized Trial of Metformin, Ivermectin, and Fluvoxamine for Covid-19. N Engl J Med. 2022;387:599-610.
- Mirahmadizadeh A, Semati A, Heiran A, Ebrahimi M, Hemmati A, Karimi M, et al. Efficacy of single-dose and double-dose ivermectin early treatment in preventing progression to hospitalization in mild COVID-19: A multi-arm, parallel-group randomized, double-blind, placebo-controlled trial. Respirology. 2022;27:758-766.
- Rezai MS, Ahangarkani F, Hill A, Ellis L, Mirchandani M, Davoudi A, et al. Non-effectiveness of Ivermectin on Inpatients and Outpatients With COVID-19; Results of Two Randomized, Double-Blinded, Placebo-Controlled Clinical Trials. Front Med (Lausanne). 2022;9:919708.
- Chaudhary SM, Wright RM, Patarroyo-Aponte G. Role of vitamin C in critically ill patients with COVID-19: is it effective? Acute Crit Care 2020;35:307–8.
- Thomas S, Patel D, Bittel B, Wolski K, Wang Q, Kumar A, et al. Effect of high-dose zinc and ascorbic acid supplementation vs usual care on symptom length and reduction among ambulatory patients with SARS-CoV-2 infection: the COVID A to Z randomized clinical trial. JAMA Netw Open. 2021;4:e210369.
- EMA. EMA advises continued use of medicines for hypertension, heart or kidney disease during COVID-19 pandemic. 2020b. Ga naar bron: EMA. EMA advises continued use of medicines for hypertension, heart or kidney disease during COVID-19 pandemic. 2020b.
- Deenstra DD, Nijziel MR, Aldenkamp AF, Van Balkom RH, Smeenk FW. Toename van dyspneu bij covid-19-patiënten. Ned Tijdschr Geneeskd 2020;164:D5116.
- World Health Organization. Living Guidance Corticosteroids for COVID-19. Geraadpleegd februari 2021a. Ga naar bron: World Health Organization. Living Guidance Corticosteroids for COVID-19. Geraadpleegd februari 2021a.
- FMS. Leidraad Corticosteroïden bij de behandeling van COVID-19. 2020b. Ga naar bron: FMS. Leidraad Corticosteroïden bij de behandeling van COVID-19. 2020b.
- Horby P, Lim WS, Emberson JR, Mafham M, Bell JL, Linsell L, et al. RECOVERY Collaborative Group. Dexamethasone in hospitalized patients with Covid-19. N Engl J Med 2021;384:693-704.
- Jenner WJ, Gorog DA. Incidence of thrombotic complications in COVID-19 : On behalf of ICODE: The International COVID-19 Thrombosis Biomarkers Colloquium. J Thromb Thrombolysis. 2021;52(4):999-1006.
- NIV. Richtlijnmodule Tromboseprofylaxe op de verpleegafdeling bij COVID-19. 2022. Ga naar bron: NIV. Richtlijnmodule Tromboseprofylaxe op de verpleegafdeling bij COVID-19. 2022.
- Ackermann M, Verleden SE, Kuehnel M, Haverich A, Welte T, Laenger F, et al. Pulmonary vascular endothelialitis, thrombosis, and angiogenesis in Covid-19. N Engl J Med. 2020;383:120-128.
- Barbar S, Noventa F, Rossetto V, Ferrari A, Brandolin B, Perlati M, et al. A risk assessment model for the identification of hospitalized medical patients at risk for venous thromboembolism: the Padua Prediction Score. J Thromb Haemost 2010;8:2450-7.
- Talasaz AH, Sadeghipour P, Kakavand H, Aghakouchakzadeh M, Kordzadeh-Kermani E, Van Tassell BW, et al. Recent Randomized Trials of Antithrombotic Therapy for Patients With COVID-19: JACC State-of-the-Art Review. J Am Coll Cardiol. 2021;77(15):1903-1921.
- Connors JM, Brooks MM, Sciurba FC, Krishnan JA, Bledsoe JR, Kindzelski A, et al.; ACTIV-4B Investigators. Effect of Antithrombotic Therapy on Clinical Outcomes in Outpatients With Clinically Stable Symptomatic COVID-19: The ACTIV-4B Randomized Clinical Trial. JAMA. 2021;326(17):1703-1712.
- Ananworanich J, Mogg R, Dunne MW, Bassyouni M, David CV, Gonzalez E, et al. Randomized study of rivaroxaban vs. placebo on disease progression and symptoms resolution in high-risk adults with mild Covid-19. Clin Infect Dis. 2021:ciab813.
- KNMP Kennisbank, geraadpleegd 4-4-2022.
- Avezum Á, Oliveira Junior HA, Neves PDMM, Alves LBO, Cavalcanti AB, Rosa RG, et al; Coalition VIII COVID-19 Brazil Investigators. Rivaroxaban to prevent major clinical outcomes in non-hospitalised patients with COVID-19: the CARE –COALITION VIII randomized clinical trial. EclinicalMedicine. 2023;60:102004.
- Barco S, Voci D, Held U, Sebastian T, Bingisser R, Colucci G, et al; OVID investigators. Enoxaparin for primary thromboprophylaxis in symptomatic outpatients with COVID-19 (OVID): a andomized, open-label, parallel-group, multicentre, phase 3 trial. Lancet Haematol 2022;9:e585-e593.
- Cools F, Virdone S, Sawhney J, Lopes RD, Jacobson B, Arcelus JI, et al; ETHIC investigators. Thromboprophylactic low-molecular-weight heparin versus standard of care in unvaccinated, at-risk outpatients with COVID-19 (ETHIC): an open-label, multicentre, randomised, controlled, phase 3b trial. Lancet Haematol 2022;9:e594-e604.
- Duvignaud A, Lhomme E, Onaisi R, Sitta R, Gelley A, Chastang J, et al; Coverage Study Group. Inhaled ciclesonide for outpatient treatment of COVID-19 in adults at risk of adverse outcomes: a randomised controlled trial (COVERAGE). Clin Microbiol Infect 2022;28:1010-1016.
- Gezondheidsraad. Toepassingskader revaccinatie tegen COVID-19. 2022. Ga naar bron: Gezondheidsraad. Toepassingskader revaccinatie tegen COVID-19. 2022.
- Hippisley-Cox J, Coupland CA, Mehta N, Keogh RH, Diaz-Ordaz K, Khunti K, et al. Risk prediction of covid-19 related death and hospital admission in adults after covid-19 vaccination: national prospective cohort study. BMJ. 2021;374:n2244.
- Li H, Xiang H, He B, Zhang Q, Peng W. Nirmatrelvir plus ritonavir remains effective in vaccinated patients at risk of progression with COVID-19: A systematic review and meta-analysis. J Glob Health. 2023;13:06032.
- OpenSAFELY Collaborative; Green A, Curtis H, Hulme W, Williamson E, McDonald H, Bhaskaran K, et al. Describing the population experiencing COVID-19 vaccine breakthrough following second vaccination in England: a cohort study from OpenSAFELY. BMC Med. 2022;20:243.
- Piazza G, Spyropoulos AC, Hsia J, Goldin M, Towner WJ, Go AS, et al; PREVENT-HD Investigators. Rivaroxaban for Prevention of Thrombotic Events, Hospitalization, and Death in Outpatients With COVID-19: A Randomized Clinical Trial. Circulation. 2023;147:1891-1901.
- RIVM. PIENTER Corona onderzoek. 2022. Geraadpleegd in april 2023. Ga naar bron: RIVM. PIENTER Corona onderzoek. 2022. Geraadpleegd in april 2023.
- Santos BC, Flumignan RLG, Civile VT, Atallah ÁN, Nakano LCU. Prophylactic anticoagulants for non-hospitalised people with COVID-19 (Review). Cochrane Database Syst Rev 2023:8: CD015102.
- Wagner C, Griesel M, Mikolajewska A, Metzendorf MI, Fischer AL, Stegemann M, et al. Systemic corticosteroids for the treatment of COVID-19: Equity-related analyses and update on evidence. Cochrane Database Syst Rev 2022;11:CD014963.
- Yek C, Warner S, Wiltz JL, Sun J, Adjei S, Mancera A, et al. Risk Factors for Severe COVID-19 Outcomes Among Persons Aged ≥18 Years Who Completed a Primary COVID-19 Vaccination Series - 465 Health Care Facilities, United States, December 2020-October 2021. MMWR Morb Mortal Wkly Rep. 2022; 71: 19-25.
- FMS/SWAB-richtlijn COVID-19. Geraadpleegd in juni 2023. Behandeling bij COVID-19 - Richtlijn - Richtlijnendatabase Ga naar bron: FMS/SWAB-richtlijn COVID-19. Geraadpleegd in juni 2023. Behandeling bij COVID-19 - Richtlijn - Richtlijnendatabase
- LCI-richtlijn COVID-19. Geraadpleegd mei 2023a.
- NICE guideline [NG191] 2022: COVID-19 rapid guideline: managing COVID-19. Recommendations | COVID-19 rapid guideline: managing COVID-19 | Guidance | NICE. Geraadpleegd op 22 februari 2023. Ga naar bron: NICE guideline [NG191] 2022: COVID-19 rapid guideline: managing COVID-19. Recommendations | COVID-19 rapid guideline: managing COVID-19 | Guidance | NICE. Geraadpleegd op 22 februari 2023.
- RIVM. Adviesnota Vaststelling volwassen medische risicogroepen COVID-19-vaccinatiecampagne. 2023. Adviesnota-vaststelling-volwassen-medische-risicogroepen-covid-19-vaccinatiecampagne.pdf (rivm.nl) Ga naar bron: RIVM. Adviesnota Vaststelling volwassen medische risicogroepen COVID-19-vaccinatiecampagne. 2023. Adviesnota-vaststelling-volwassen-medische-risicogroepen-covid-19-vaccinatiecampagne.pdf (rivm.nl)